SQLITE NOT INSTALLED
Диагностика фокальной эпилепсии
Если парциальный пароксизм возник впервые, то пациенту необходимо детальное обследование, так как данный симптом может быть проявлением серьезной церебральной патологии. Во время консультации врач-невролог просит полностью описать длительность, характер, последовательность развития эпилептического приступа. Выявленные отклонения помогают установить расположение очага патологии.
Эпилептическая активность диагностируется с помощью ЭЭГ. Эпи-активность фокальной эпилепсии можно зафиксировать на ЭЭГ даже в межприступный период. Если ЭЭГ без приступа малоинформативна, то следует провести электроэнцефалоскопию с провокационными пробами и/или во время приступа. Субдуральная кортикография – это электроэнцефалоскопия с установлением электродов под твердой мозговой оболочкой. Помогает точно определить локализацию патологического очага.
Из инструментальных методов исследований наиболее эффективным для выяснения морфологических основ ФЭ является МРТ. Толщина срезов должна составлять около 1-2 мм, чтобы как можно точнее обнаружить мельчайшие дефекты вещества головного мозга. В случае симптоматической эпилепсии МРТ даёт возможность выявить первопричину: очаговые поражения, атрофии, дисплазии. В ряде случаев обнаружить подобные изменения не удается и тогда диагноз — идиопатическая или криптогенная ФЭ. В качестве дополнительного, но необязательного исследования может быть назначена ПЭТ головного мозга. ПЭТ зафиксирует эпилептогенный участок как зону повышенной метаболической активности. ОФЭКТ также применяется в качестве дополнительного метода диагностики, в ходе которого специалист способен отслеживать динамику перфузии церебрального вещества: в течение припадка будет наблюдаться картина гиперперфузии эпилептогенного очага, а в отрезок времени между пароксизмами — гипоперфузия.
Течение болезни
Огромным плюсом патологии безусловно является факт, что приступы очень редкие, а их продолжительность не превышает 2-3 минут. Известно много случаев, когда они были единичными и повторялись не больше, чем несколько раз за год. Конечно, приступы могут возникать более часто, но с течением временем и взрослением ребенка, они гарантированно будут случаться реже и реже.
Если сравнивать доброкачественную роландическую эпилепсию с Джексоновской, то первая не оказывает абсолютно никакого влияния на развитие ребенка, в том числе психомоторное и физическое, и не вызовет олигофрению.
Однако, полностью безопасным данное заболевание назвать нельзя. У небольшого количества носителей болезни, а именно у 3%, эпилепсия приводит к неполному параличу половины лица, который имеет название преходящий гемипарез.
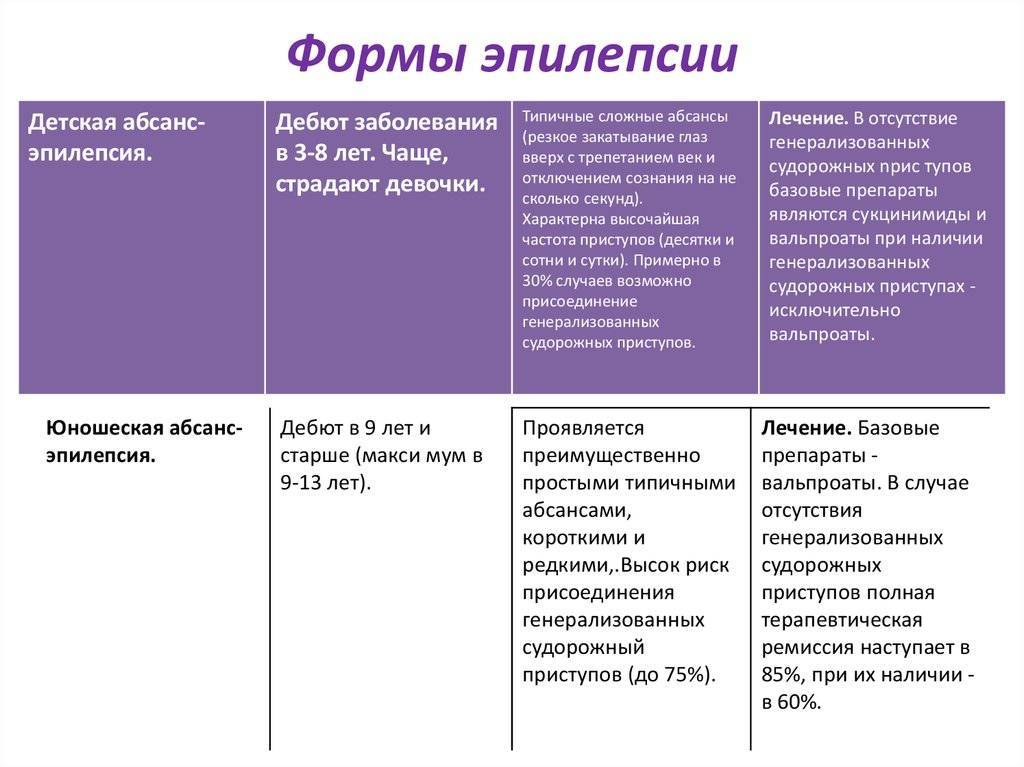
Эпилепсия с миоклоническими абсансами.
Эпилепсия с миоклоническими абсансами (ЭМА) – форма абсансной эпилепсии, характеризующаяся частыми приступами абсансов, протекающих с массивными миоклониями мышц плечевого пояса и рук, и резистентностью к терапии.
Дебют приступов при ЭМА варьирует от 1 до 7 лет (в среднем, 4 года); преобладают по полу мальчики. Миоклонические абсансы у большинства больных являются первым видом приступов. В некоторых случаях заболевание может начинаться с ГСП с последующим присоединением абсансов. Сложные абсансы с массивным миоклоническим компонентом составляют “ядро” клинической картины ЭМА. Типичны абсансы с интенсивными миоклоническими подергиваниями плечевого пояса, плеч и рук, носящими, обычно, билатерально-синхронный и симметричный характер. При этом может наблюдаться легкий наклон туловища и головы кпереди (пропульсия), отведение и приподнимание плеч (тонический компонент). У большинства пациентов также отмечаются миоклонические подергивания мышц шеи (короткие серийные кивки), синхронно с подергиваниями плеч и рук. Характерна высокая частота абсансов, достигающая 10 приступов в час и более. Продолжительность приступов составляет от 5 до 30 сек, причем, характерны длительные абсансы – более 10 сек. Приступы нередко учащаются в утренние часы. Основным фактором, провоцирующим возникновение абсансов при ЭМА, является гипервентиляция.
В большинстве случаев (80%) абсансы сочетаются с генерализованными судорожными приступами. Характерна редкая частота ГСП, обычно, не превышающая 1 раза в мес.
Изменения ЭЭГ в межприступном периоде выявляются практически во всех случаях. Замедление основной активности фоновой записи отмечается нечасто, главным образом, у пациентов с интеллектуальным дефицитом. Типичный ЭЭГ-паттерн – генерализованная пик- (или, реже, полипик- ) волновая активность с частотой 3 Гц. Достоверным для установления диагноза ЭМА является появление разрядов при электромиографии в ответ на миоклонические сокращения мышц, возникающих синхронно с пик-волновой активностью на ЭЭГ (полиграфическая запись).
Лечение. Стартовое лечение осуществляется с монотерапии препаратами, производными вальпроевой кислоты. Средняя дозировка 50-70 мг/кг/сут; при хорошей переносимости – постепенное увеличение до 80-100 мг/кг/сут. В большинстве случаев монотерапия уряжает приступы, но не приводит к достаточному контролю над ними. В этом случае рекомендуется сочетать прием вальпроатов с сукцинимидами или ламотриджином.
Практически у всех больных при применении политерапии в адекватно высоких дозировках удается добиться хорошего контроля над приступами, однако, ремиссия возникает лишь в 1/3 случаев. У большинства пациентов имеются серьезные проблемы с социальной адаптацией.
Причины эпилепсии у детей
Мнение о том, что эпилепсия – исключительно наследственное заболевание, современными врачами не поддерживается. Некоторые ее формы не наследуются, некоторые являются следствием структурного поражения головного мозга (фокальные корковые дисплазии, врожденные аномалии развития головного мозга, туберозный склероз, ганглиомы и др.). Также нельзя однозначно утверждать, что к эпилепсии приводят какие-либо перенесенные человеком заболевания, однако они могут ускорить наступление болезни. Таковыми факторами являются:
- родовые травмы, возникновение кислородной недостаточности при рождении;
- черепно-мозговые травмы;
- кровоизлияния в мозг;
- новообразования в головном мозге (кисты, гематомы, опухоли);
- абсцесс мозга;
- инфекционные, паразитарные, вирусные заболевания;
- менингит, энцефалит.
Чем опасна эпилепсия у детей
- Во время приступа ребенок может получить серьезную травму, задохнуться рвотными массами, прикусить язык или щеку.
- Кроме этого, у детей бывают частые и тяжелые приступы с малым интервалом, когда они попросту не могут прийти в себя.
- Из-за постоянных приступов может сформироваться хроническая пневмония, развиться умственная отсталость.
2 группа инвалидности
Выраженные нарушения психических функций
Жалобы (субъективные симптомы) выраженные и стабильные:
Резкая слабость и повышенная утомляемость при незначительных физических и нервно-психических нагрузках, постоянные головные боли, выраженные нарушения сна (бессонница, дневная сонливость).
Астенический синдром сочетается с ипохондрическими, тревожными, депрессивными нарушениями.
Экспериментально-психологические методы исследования выявляют значительное ухудшение показателей внимания (концентрации, устойчивости, переключения), умеренное снижение памяти.
Частота эпиприступов при II группа инвалидности:
Частые эпилептические приступы первично и вторично-генерализованные: частые — 4 раза в месяц и более.
Частые фокальные приступы без нарушения сознания: частые -5 и более раз в день.
Психомоторные приступы: средней частоты — 1 раз в месяц и более;
Эпилептический статус: 1 и более раз в 2-3 месяца.
Выраженные нарушения психических функций: выраженные жалобы, частые эпиприступы приводят к ограничению способности контролировать свое поведение 2-й степени, к ориентации 2-й степени, самообслуживанию 2-й степени, трудовой деятельности 2-й степени; обучению 2-й степени. Устанавливается II группа инвалидности.
Лечение Лобной эпилепсии у детей:
Лечение лобной эпилепсии направлено на полное избавление от эпилептических приступов. Лобная эпилепсия одна из самых сложных форм для терапии. Препараты медикаментозного лечение и дозировка подбираются индивидуально. Для лечения используются карбамазепин, вольпроат, гексамидин, дифенин. Препараты направлены на уменьшение возбудимости нервных клеток головного мозга, что позволяет мозгу нормально функционировать. Если при монотерапии не добиваются результатов, тогда применяется политерапия – применение 2 или более лекарственных вышеперечисленных препаратов одновременно – а также симптоматическая терапия. Даже после прекращения приступов дети продолжают принимать препараты на протяжении ещё 2 лет. Только в крайних случаях используется хирургический метод лечения. К нему прибегают только, когда наблюдается большое количество эпилептических приступов, неэффективность медикаментозного лечения, фокальные приступы. После удаления очага, вызывающего приступы, больной полностью от них избавляется. Операция может быть назначена ребенку в любом возрасте – будь то грудничок, ребенок дошкольного или школьного возраста. Чем младше ребенок, тем легче ему перенести операцию.
Прогноз зависит от локализации очага в лобной доле, структурного поражения мозга и ранней диагностики
Частые приступы ухудшают социальную адаптацию больных, поэтому очень важно начать своевременное обследование и незамедлительное лечение
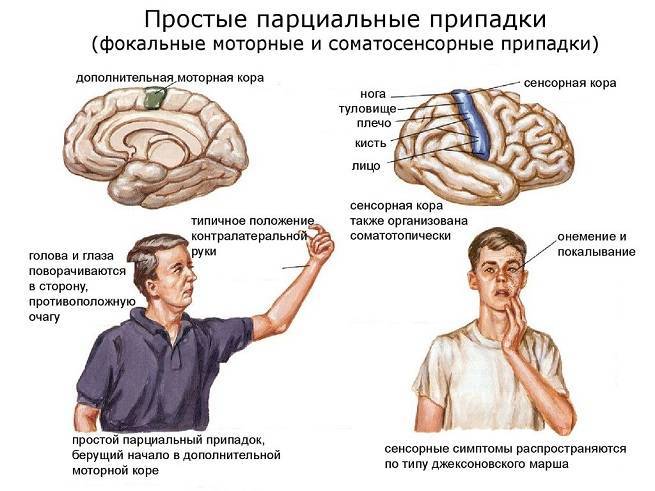
Симптоматическая парциальная эпилепсия
При симптоматических парциальных формах эпилепсии выявляются структурные изменения в коре головного мозга. Причины, детерминирующие их развитие, многообразны и могут быть представлены двумя основными группами: перинатальными и постнатальными факторами. Верифицированное перинатальное поражение ЦНС в анамнезе констатируется у 35% пациентов (внутриутробные инфекции, гипоксия, эктомезодермальные дисплазии, кортикальные дисплазии, родовая травма и пр.). Среди постнатальных факторов следует отметить нейроинфекции, черепно-мозговые травмы, опухоли коры головного мозга.
Дебют приступов при симптоматической парциальной эпилепсии варьирует в широком возрастном диапазоне, с максимумом в предшкольном возрасте. Для этих случаев характерно наличие изменений в неврологическом статусе, нередко в сочетании со снижением интеллекта; появление региональных паттернов на ЭЭГ, резистентность приступов к АЭП и возможность хирургического лечения. Выделяют симптоматические парциальные формы эпилепсии: височную, лобную, теменную и затылочную. Две первых – наиболее частые и составляют до 80% всех случаев.
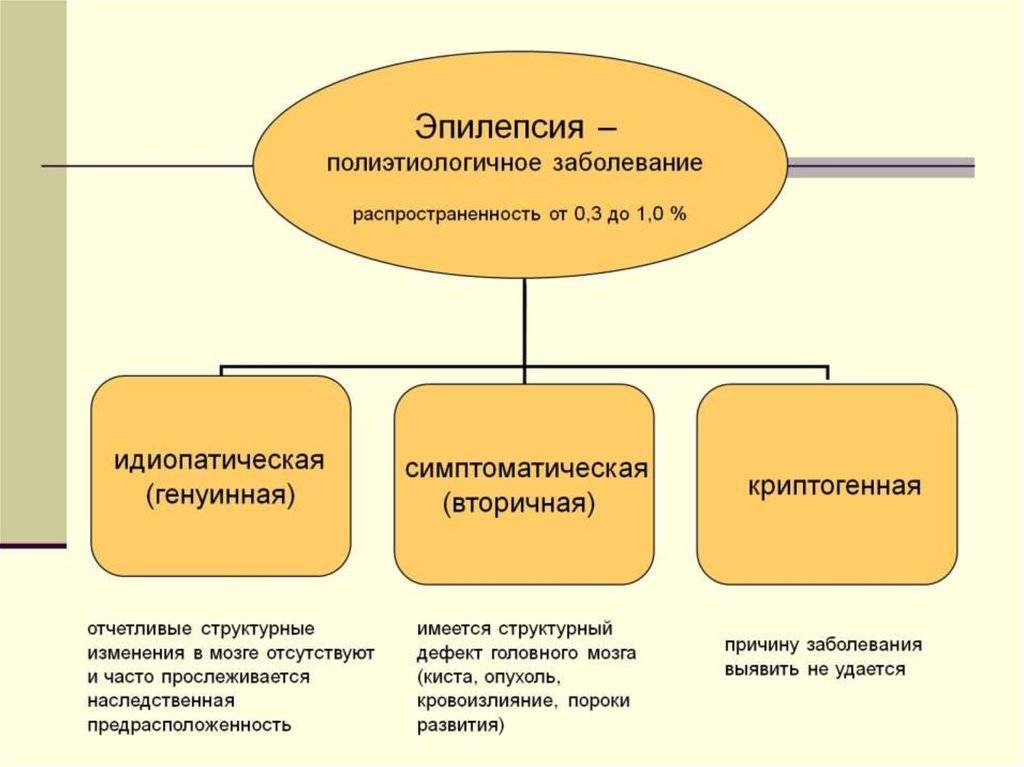
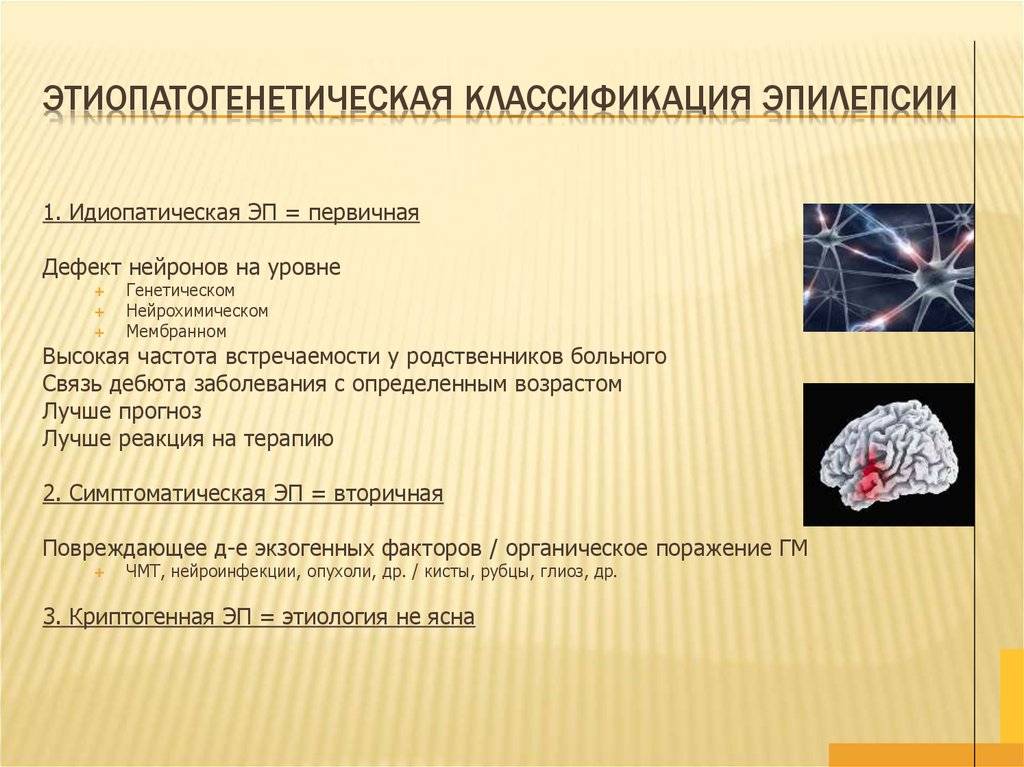
Причины эпилепсии
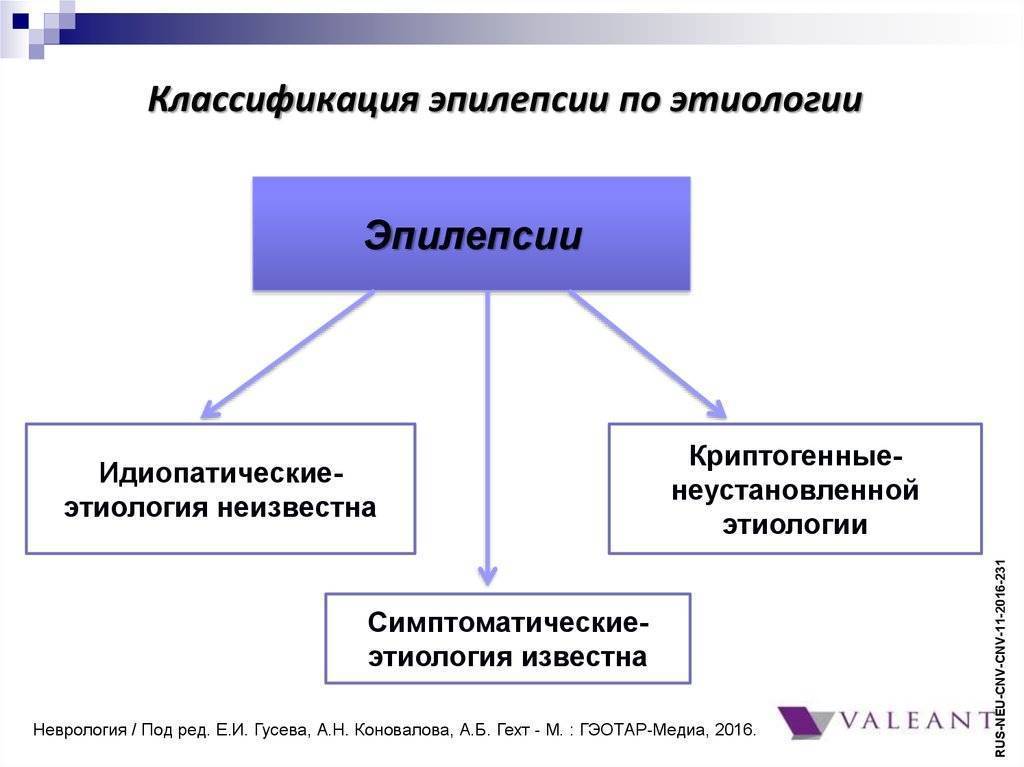
Примерно в половине случаев причину заболевания установить не удается. Тогда говорят о первичной или идиопатической эпилепсии. Считается, что этот вид эпилепсии может передаваться по наследству.
Во многих случаях причину эпилепсии не получается установить из-за несовершенства медицинского оборудования, которое не может определить некоторые типы поражений головного мозга. Кроме того, многие исследователи полагают, что заболевание могут вызывать генетические дефекты в головном мозге. В настоящее время предпринимаются попытки определить, какие поломки в генах способны нарушить передачу электрических импульсов в клетках головного мозга. Пока не удалось выявить однозначной зависимости между отдельными генами и развитием эпилепсии.
Остальные случаи эпилепсии, как правило, связаны с различными изменениями в головном мозге. Это называются вторичной (симптоматической) эпилепсией. Головной мозг — это сложный и очень чувствительный механизм, в работе которого участвуют нервные клетки, электрические импульсы и химические вещества — нейромедиаторы. Любое повреждение потенциально может нарушать работу мозга и вызывать припадки.
Возможные причины симптоматической эпилепсии:
- нарушение мозгового кровообращения, например, в результате инсульта или субарахноидального кровоизлияния;
- опухоль головного мозга;
- тяжелая черепно-мозговая травма;
- злоупотребление алкоголем или употребление наркотиков;
- инфекционные заболевания, поражающие головной мозг, например, менингит;
- родовые травмы, вызывающие кислородную недостаточность у ребенка, например, когда во время родов происходит пережатие или обвитие пуповины;
- внутриутробное нарушение развития определенных участков головного мозга.
Некоторые из этих причин могут вызывать эпилепсию в раннем возрасте, однако симптоматическая эпилепсия более распространена у пожилых людей, особенно в возрасте старше 60 лет.
Факторы, способствующие появлению эпилептических припадков
У многих людей припадки возникают под воздействием определенного фактора — триггера. Наиболее распространенные из них:
- стресс;
- нехватка сна;
- употребления алкоголя;
- некоторые лекарственные препараты и наркотики;
- месячные у женщин;
- вспышки света (малораспространенный фактор, который вызывает припадки только у 5% людей — т. н. фотогенная эпилепсия).
Определить триггеры приступов поможет дневник, в который нужно записывать каждый приступ и описание предшествовавших ему событий. Со временем можно определить раздражители, вызывающие припадки, чтобы впоследствии избегать их.
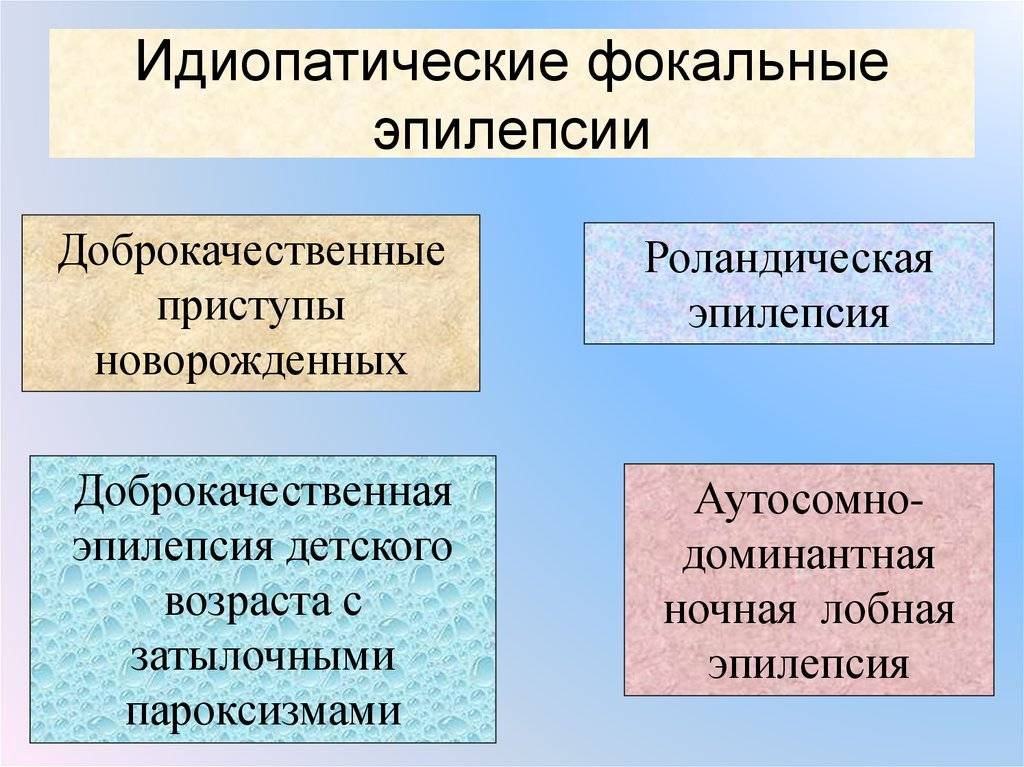
3.1. Доброкачественная эпилепсия детского возраста с центрально-височными спайками (роландическая эпилепсия)
Общая характеристика
Роландическая эпилепсия — одна из форм идиопатической локально обусловленной эпилепсии детского возраста, проявляющаяся преимущественно ночными короткими гемифациальными моторными приступами и имеющая благоприятный прогноз.
Роландическая эпилепсия проявляется в возрасте 2–14 лет. Приступы могут быть парциальными и вторично-генерализованными. Большинство парциальных приступов являются моторными. Типичные приступы, возникающие как в состоянии бодрствования, но все чаще во время сна (преимущественно первая половина ночи), протекают обычно при сохранном сознании и начинаются с соматосенсорной ауры, характеризующейся парестезией щеки, мышц глотки и гортани, ощущением булавочных уколов, онемения в щеке, деснах, языке на стороне, противоположной фокусу. Затем появляются моторные феномены в виде односторонних гемифациальных (с вовлечением лицевой мускулатуры) клонических или тонико-клонических судорог, которые могут распространяться на гомолатеральную руку (фацио-брахиальные приступы) и ногу (унилатеральные приступы).
В начале приступа или в процессе его развития возникают затруднения речи, выражающиеся в полной невозможности говорить или произносить отдельные звуки. Наряду с анартрией отмечается гиперсаливация, характеризющаяся обильной продукцией и выделением изо рта слюны, что способствует возникновению хлюпающих, хрюкающих звуков.
Длительность приступов, как правило, не более 2–3 мин, частота в среднем — 2–6 раз в год .
При роландической эпилепсии в единичных случаях возможно развитие эпилептического статуса .
Для больных с роландической эпилепсии характерен нормальный интеллект и неврологический статус, хотя ряд современных исследователей все же указывают на наличие у таких детей нейропсихологической недостаточности .
Ряд авторов отмечают возможность возникновения при роландической эпилепсии приступов, характеризующихся болями в животе, головокружением, зрительными феноменами (вспышки света, слепота, мелькание предметов перед глазами), которые обычно отмечаются у детей моложе 5 лет; сложных парциальных приступов или типичных абсансов .
К атипичной роландической эпилепсии (синдром псевдоленнокса) относят группу больных в возрасте 2–8 лет, у которых отмечаются простые парциальные гемифациальные и гемиклонические ночные приступы, сочетающиеся с миоклонически-астатическими, атоническими пароксизмами и в ряде случаев с абсансами , но никогда в отличие от истинного синдрома Леннокса-Гасто не бывает тонических судорог . Частота приступов обычно высокая. До дебютирования приступов у детей не отмечается нарушений в нервно-психическом развитии.
Электроэнцефалографические паттерны
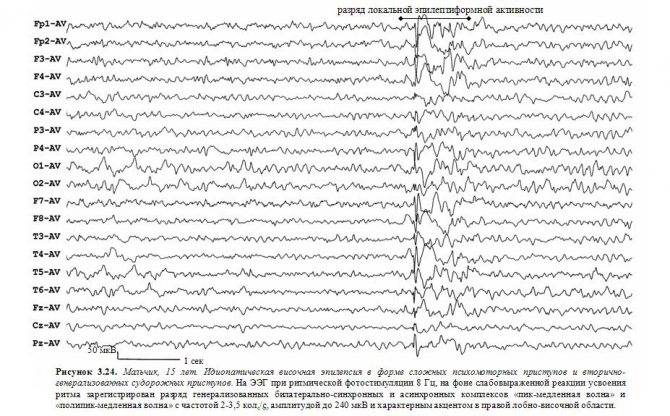
Приступная и межприступная ЭЭГ у больных с роландической эпилепсией характеризуется нормальной основной активностью и обычно дифазными спайками, за которыми следует медленная волна. Спайки или острые волны появляются одиночно или группами в средне-височной и центральной области или височно-центрально-теменной области . Они могут наблюдаться как унилатерально (обычно контралатерально гемифациальным приступам), так и билатерально (синхронно или асинхронно). «Роландические» комплексы обычно наиболее отчетливо выражены при открытых глазах (рис. 3.1).
В ряде случаев на ЭЭГ регистрируются генерализованные комплексы «спайк-волна», типичные для абсансов. Острые волны также могут располагаться в затылочной области . Также во время ночного приступа на ЭЭГ может регистрироваться низкоамплитудная быстрая активность в центрально-височной области, переходящая в роландические комплексы с распространением на всю гемисферу и с последующей генерализацией .
При атипичной роландической эпилепсии (синдром псевдоленнокса) фоновая ЭЭГ не изменена либо слегка замедлена и дизорганизована (рис. 3.2а), в ряде случаев, преимущественно в лобных отделах. Типичные роландические спайки могут сочетаться с медленными комплексами «острая-медленная волна», характерными для синдрома Леннокса-Гасто, или нерегулярной диффузной пик-волновой активностью частотой около 2,5 кол./с и амплитудным региональным преобладанием в лобных отделах; могут определяться фокальные спайки или медленные волны в центрально-височной области или центрально-височно-теменной области (рис. 3.2б).
В приступной ЭЭГ может отмечаться асинхронное появление разрядов высокоамплитудных нерегулярных диффузных комплексов «пик-волна» или «острая-медленная волна» частотой 1.5–4 кол./с длительностью 3–10 с, синхронно с пароксизмом атипичных абсансов .
Эпидемиология детской эпилепсии в России
Эпидемиологические исследования проводимые в Москве (1980 – 1981 гг.) показали, что у 4,4% детей прослеживалось наличие хотя бы одного судорожного эпизода, в 5,4% случаев эпилепсия сопровождалась задержкой психического развития и умственной отсталостью. Дебют заболевания в 29,3% случаев у детей приходится на возраст до 3 лет, в том числе до 1 года – 20,3%. При злокачественном течении заболевания у больных с умственной отсталостью припадки в возрасте до 3 лет возникали в 44,9% случаев (до 1 года – 37,3%). В 95,78% случаев ФС наблюдались у детей первых 5 лет жизни, из них 41,4% приходился на возраст до 1 года .
Заболеваемость эпилепсией в Санкт–Петербурге составила 1,56 на 1000 детского населения. У детей с эпилепсией в 81,9% случаев установлена генетическая природа заболевания .
В Новосибирской области показана высокая заболеваемость эпилепсии среди детей младшего и среднего школьного возраста: 14,8 на 1000 детского населения в возрасте от 7 до 13 лет. Частота встречаемости среди мальчиков, превалировала над девочками (61,1% против 38,9%). Заболеваемость идиопатическими эпилепсиями составила 3,4 на 1000 детского населения. ФС зарегистрированы у 7,5% детей, чаще у мальчиков. Отмечено превалирование криптогенных и симптоматических форм .
Распространенность детской эпилепсии в г. Саратове составила 2,7 на 1000 детского населения. Фокальные формы эпилепсии диагностированы в 55% случаев, генерализованные – в 45% случаев. Среди симптоматических фокальных форм преобладали височная (23,8%) и лобная (16,7%) эпилепсии. Среди идиопатических фокальных – роландическая эпилепсия (60%). Ведущими факторами риска эпилепсии у детей являлись: наследственная отягощенность, перинатальное гипоксически-ишемическое поражение, церебральные дисгенезии. Криптогенные формы составили 57,3% .
Распространенность эпилепсии в сельских районах Волгоградской области составила 2,84 на 1000 детского населения (среди лиц мужского пола — 3,4 на 1000, среди лиц женского пола — 2,36 на 1000). Этиологические факторы: перинатальная патология (46%), черепно-мозговая травма (20,7%), отягощенная наследственность по эпилепсии (11,%), нейроинфекции (6,7%). Фокальные припадки регистрировались в 56,0% случаев, генерализованные — 39,4% .
Заболеваемость эпилепсией в Республике Татарстан составила 1,0 на 1000 населения детей от 0 до 14 лет и 1,1 на 1000 подростков от 15 до 18 лет. Распространенность эпилепсии составила среди детей от 0 до 14 лет 5,4 на 1000 населения соответствующего возраста и 7,0 среди подростков. В структуре эпилепсии и эпилептических синдромов преобладали фокальные — 55,5%; генерализованные — 43%, неклассифицированные формы эпилепсии – 1,5%. Идиопатические эпилепсии зарегистрированы в 21,25%, симптоматические — 32,0%, криптогенные — 46,75 % .
В Красноярском крае распространенность эпилепсии составляет – 2,8 случая на 1000 населения: среди детей – 5,1 на 1000, подростков – 6,1 на 1000, а среди взрослых – 2,3 на 1000. Этиологические формы эпилепсии: криптогенная эпилепсия (46,2%), симптоматическая (42,5%), и идиопатическая (7,4%) эпилепсии .
По результатам научно-исследовательской работы проведенной в Республике Тыва, которая относится к зоне с высокой распространенностью эпилепсии и эпилептических синдромов у детей и подростков, выявлено, что частота случаев дебюта эпилептических припадков приходилось в основном, на возраст от новорожденности до 5 лет. Средняя стандартизированная распространенность эпилепсии среди детского населения Республики Тыва составила – 3,2 ± 2,9 на 1000. Среди факторов риска детской эпилепсии наиболее значимыми были: перинатальная патология, отягощенная наследственность, нейроинфекции .
Патогенез (что происходит?) во время Лобной эпилепсии у детей:
Эпилептический припадок при этой форме может проявляться короткими приступами либо длительными, при которых ребенок может находиться без сознания более получаса.
Для лобной эпилепсии свойственны простые, сложные (психомоторные) парциальные и вторично-генерализованные приступы. Наиболее часто наблюдаются психомоторные лобные приступы. Лобная эпилепсия локализуется в дополнительной моторной зоне, оперкулярной, дорсолатеральной в моторной коре. Однако определение четкой локализации эпилептогенной зоны в лобной доле клинически и даже при применении специальных методов исследования крайне затруднено.
Обзор
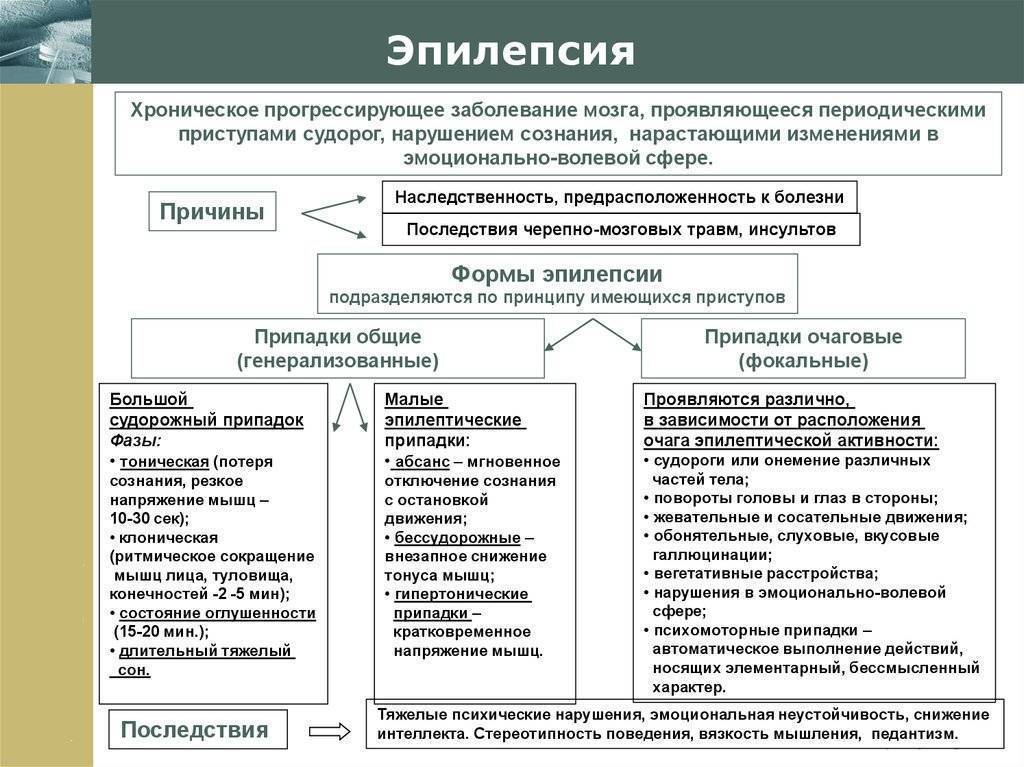
Эпилепсия — это заболевание, которое поражает головной мозг и сопровождается повторяющимися приступами судорог — эпилептическими припадками.
Приблизительно 5-10 человек из 1000 болеют эпилепсией. Это самое распространенное хроническое заболевание нервной системы. Один раз в жизни эпилептический припадок переносят 5% населения.
Эпилепсия может развиться в любом возрасте, хотя чаще всего она появляется у детей. Определить конкретную причину заболевания удается не всегда, однако в некоторых случаях (особенно у взрослых) развитие эпилептических припадков бывает связано с повреждением головного мозга. Например, эпилепсия может появиться после инсульта, опухоли мозга или тяжелой черепно-мозговой травмы. В некоторых случаях заболевание может быть вызвано генетическими изменениями мозга, унаследованными от родителей.
Клетки головного мозга (нейроны) передают друг другу электрические сигналы с помощью химических соединений — нейромедиаторов. Во время припадка нейроны генерируют большое количество электрических импульсов, в головном мозге формируется зона повышенного возбуждения — очаг эпилепсии, что сопровождается появлением симптомов в виде судорог, нарушения чувствительности, восприятия окружающего мира или потери сознания.
У некоторых людей за всю жизнь случается всего один припадок. Если при обследовании не находят причин или факторов риска для развития заболевания, диагноз эпилепсии не ставится. Зачастую заболевание диагностируется после нескольких припадков, так как однократные эпилептические приступы весьма распространены
Самое важное для постановки диагноза — описание припадка самим человеком и свидетелями произошедшего. Помимо этого, проводится исследование функции головного мозга, поиск возможного очага эпилепсии и вероятных причин болезни