SQLITE NOT INSTALLED
Есть ли альтернатива?
Инъекции гормонов уменьшают боль при артрозе голеностопа, колена, бедра, но оказывают и негативное влияние на организм. Особенно опасны они при сахарном диабете, артериальной гипертензии, язве желудка, а также если у пациента нарушена работа почек. К тому же кортикостероиды лишь на время избавляют от боли, значит, человеку с каждым разом будет необходима все бОльшая доза.
Вместо вредных для здоровья кортикостероидов, которые к тому же не лечат, можно выбрать другие терапевтические методы:
- инъекции хондропротекторов, которые направлены на восстановление поврежденной хрящевой ткани и нормализуют обмен веществ в суставе (курс составляет от 3 до 15 уколов);
- инъекции протеза синовиальной жидкости, например «Нолтрекс», который раздвигает поврежденные хрящевые поверхности, смешивается с суставной жидкостью и возвращает суставу нормальное функционирование.
Курс инъекций протеза синовиальной жидкости составляет 2-5 процедур. После этого об артрозе можно будет забыть на 1-1,5 года. Препарат на основе гиалуроновой кислоты или синтетический Noltrex безопасен для ЖКТ и других систем организма, не нанесет вреда диабетикам и людям с повышенным артериальным давлением.
Если вас беспокоят сильные боли в суставе, не спешите купировать их гормонами. Рассмотрите вариант лечения с перспективой на будущее, вместо того чтобы долго травить свой организм кортикостероидами.
РОЛЬ ГЛЮКОКОРТИКОИДОВ
Доказательства важной роли глюкокортикоидных гормонов в эмбриональном программировании системных заболеваний, развивающихся во взрослом возрасте, были получены из нескольких источников. Интерес к этим соединениям был вызван убедительными данными о том, что глюкокортикоиды могут непосредственно приводить к повышению артериального давления и формированию инсулинорезистентности во взрослом возрасте, а воздействие глюкокортикоидов во время беременности может замедлять развитие плода и перенастраивать состояние функциональной системы ГГГН во взрослом возрасте
Кроме того, в экспериментах на небеременных животных было отмечено, что недостаточное питание приводит к повышению активности гиппокамп-гипоталамо-гипофизарно-надпочечниковой системы. Дальнейшие исследования, включающие использование карбеноксолона (препарата, приводящего к подавлению плацентарной инактивации глюкокортикоидов), показали замедление внутриутробного развития потомства и повышение артериального давления во взрослом возрасте. Удаление надпочечников у беременных животных с использованием во время беременности только физраствора (0,9% NaCl) вместо питьевой воды, приводит к снижению веса потомства при рождении, но не к повышению артериального давления. При добавлении карбеноксолона к солевому раствору дальнейшего снижения веса при рождении не отмечалось, также не было отмечено повышения артериального давления. Использование метирапона у крыс в течение срока беременности 0-14 дней в сочетании с низко-белковой диетой привело к рождению потомства со сниженным весом, но с нормальным артериальным давлением в течение 7 недель после рождения. Замена метирапона на кортикостерон привела к повышению артериального давления после рождения только у женских особей.
Во многих исследованиях использовался синтетический стероид дексаметазон. Это было связано с тем, что дексаметазон не подвергается инактивации ферментом 11 -гидроксистероиддегидрогеназы 2-го типа (11 -HSD2). Данные исследования представляют интерес с точки зрения определения времени критического периода «программирования». Назначение беременным крысам дексаметазона только в течение последней трети гестационного периода привела к повышению кровяного давления у потомства через 16 недель после рождения. Назначение дексаметазона беременным овцам в течение всего лишь двух дней в конце первого месяца беременности (которая продолжается 5 месяцев) приводило к повышению кровяного давления у ягнят с 3-х месячного возраста. Повышение кровяного давления не было, если дексаметазон назначался в начале 3-го месяца беременности. Период назначения дексаметазона был настолько коротким, что снижения веса при рождении не происходило. Это согласуется с данными Hawkins, которые показали, что недостаточное питание овец только в первой половине беременности приводит к программированию ягнят на повышение кровяного давления к трехмесячному возрасту. Таким образом, полученные результаты показывают, что критические периоды «программирования» возможны как на ранних, так и на поздних этапах гестационного периода. Ранее это было показано для влияния андрогенов на формирование специфического для пола созревания нейро-эндокринной системы, но в отношении глюкокортикоидов это действие тогда не считалось заслуживающим внимания.
ДЕКСАМЕТАЗОН И НЕЙРОСТЕРОИДЫ
Хотя дексаметазон широко используется, как глюкокортикоид, его эффекты не ограничиваются действием только на классические глюкокортикоидные рецептор . В исследованиях, проводимых много лет назад, было обнаружено, что рецептор, связывающий дексаметазон в тканях быка, не является классическим рецептором глюкокортиоидов. Не так давно был открыт Х рецептор прегнана (PXR), который не связывал естественные глюкокортикоиды (кортизол, кортикостерон), но связывал дексаметазон, прогестерон, прегненолон и некоторые их производные. В виде димера с рецептором 9-цис-ретиноевой кислоты, PXR связываетсясо специфическими сайтами ДНК, состоящими из двух повторяющихся последовательностей. Потенциально активные нейростероиды, такие как аллопрегнанолон и тетрагидродеоксикортикостерон, образуются в организме под действием 5 -редуктаз, особенно под действием гидроксистероид-дегидрогеназ типов 2 и 3 . Ген 5 -редуктазы типа 2 транзиторно экспрессируется в мозге крысы в поздние сроки беременности и в раннем постнатальном периоде. Экспрессия 3 -редуктаз индуцируется дексаметазоном, действующим не на классические рецепторы глюкокортикоидов. Образующиеся после индукции данных ферментов нейростероиды могут влиять на многие аспекты дифференцировки и созревания головного мозга, связанные со становлением эндокринных и поведенческих функций, взаимодействуя с рецепторами ГАБА, никотиновыми рецепторами ацетилхолина, рецепторами N-метиласпартата и, возможно, с мембранными стероидными рецепторами. Нейростероиды типа аллопрегненолона оказывают влияние на становление барорефлекса. Эти данные открывают новые горизонты для дальнейших исследований влияния приема глюкокортикоидов на созревание функциональных систем плода.
Фармакологические свойства
Фармакодинамика
Синтетический глюкокортикостероид — метилированное производное фторпреднизолона. Оказывает противовоспалительное, противоаллергическое десенсибилизирующее, противошоковое, антитоксическое и иммунодепрессивное действие.
Взаимодействует со специфическими цитоплазматическими рецепторами и образует комплекс, проникающий в ядро клетки и стимулирует синтез мРНК; последняя индуцирует образование белков, в том числе липокортина, опосредующих клеточные эффекты. Липокортин угнетает фосфолипазу А2, подавляет высвобождение арахидоновой кислоты и ингибирует биосинтез эндоперекисей, простагландинов, лейкотриенов, способствующих процессам воспаления, аллергии и другие.
Белковый обмен: уменьшает количество белка в плазме (за счёт глобулинов) с повышением коэффициента альбумин/глобулин, повышает синтез альбуминов в печени и почках; усиливает катаболизм белка в мышечной ткани.
Липидный обмен: повышает синтез высших жирных кислот и триглицеридов, перераспределяет жир (накопление жира преимущественно в области плечевого пояса, лица, живота), приводит к развитию гиперхолистеринемии.
Углеводный обмен: увеличивает абсорбцию углеводов из желудочно-кишечного тракта; повышает активность глюкозо-6-фосфатазы, приводящей к повышению поступления глюкозы из печени в кровь; повышает активность фосфоэнолпируваткарбоксилазы и синтез аминотрансфераз, приводящих к активации глюконеогенеза.
Антагонистическое действие по отношению к витамину D: «вымывание» кальция из костей и повышение его почечной экскреции.
Противовоспалительный эффект связан с угнетением высвобождения эозинофилами медиаторов воспаления; индуцированием образования липокортинов и уменьшения количества тучных клеток, вырабатывающих гиалуроновую кислоту; с уменьшением проницаемости капилляров; стабилизацией клеточных мембран и мембран органелл (особенно лизосомальных).
Противоаллергический эффект обусловлен снижением количества циркулирующих эозинофилов, что приводит к снижению выделения медиаторов немедленной аллергии; снижает влияние медиаторов аллергии на эффекторные клетки.
Иммунодепрессивный эффект обусловлен торможением высвобождения цитокинов (интерлейкина) и интерлейкина2, гамма-интерферона) из лимфоцитов и макрофагов.
Подавляет синтез и секрецию адренокортикотропного гормона и вторично — синтез эндогенных глюкокортикостероидов. Особенность действия — значительное ингибирование функции гипофиза и практически полное отсутствие минералокортикостероидной активности.
Дозы 1-1,5 мг/сут угнетают функцию коры надпочечников; биологический период полувыведения — 32-72 ч (продолжительность угнетения системы гипоталамус-гипофиз-корковое вещество надпочечников).
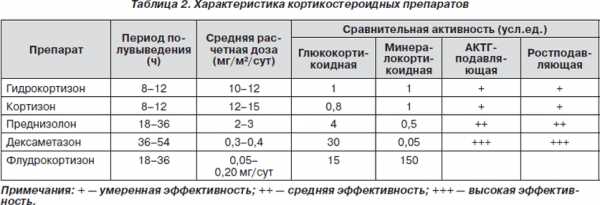
По силе глюкокортикостероидной активности 0,5 мг дексаметазона соответствуют примерно 3,5 мг преднизона (или преднизолона), 15 мг гидрокортизона или 17,5 мг кортизона.
В каких случаях назначают гормоны
На поздних стадиях артроза тазобедренного сустава или любого другого, когда боли беспокоят пациента почти всегда и обезболивающие таблетки не помогают, могут назначить более сильное средство. Это экстренная мера терапии, способная быстро снять боль и улучшить самочувствие. К сожалению, есть у этой медали и обратная сторона, особенно если прибегать к такому методу чаще, чем это необходимо.
Кеналог, дипроспан и другие препараты кортикостероидной группы быстро купируют воспаление, убирают отек и опухание. Однако они вовсе не излечивают от артроза, не восстанавливают питание хряща и не улучшают состояние сустава. Это только скорая помощь – мощный удар по организму, особенно если прибегать к такому лечению остеоартроза слишком часто.
Частые инъекции гормональных препаратов не выдержит ни один организм
РЕНИН-АНГИОТЕНЗИНОВАЯ СИСТЕМА
Функциональная система ренин-ангиотензин (ренин, ангиотензин, ангиотензинпревращающий фермент, рецепторы 1-го и 2-го типов) участвует в регуляции кровяного давления и представлена во многих органах плода (почки, головной мозг, сердечно-сосудистая система). Очевидна взаимосвязь между ренин-ангиотензиновой системой и функциональной системой поддержания уровня глюкозы в плазме крови. Было показано, что замедление внутриутробного развития плода особенно неблагоприятно влияет на развитие почек, а именно в виде уменьшения количества нефронов в активный период нефрогенеза и более высокими, чем в норме, концентрациями ренина и ангиотензина II в крови пуповины. Вследствие уменьшения количества нефронов повышается риск развития почечной недостаточности, что приводит к активизации ренин-ангиотензиновой системы с целью сохранения скорости клубочковой фильтрации. Предварительные данные участия ренин-ангиотензиновой системы получены в исследованиях L.G.Edwards и соавт., указывающих на то, что у ягнят, родившихся с низким весом в состоянии гипоксии, кровяное давление поддерживается на нормальном уровне за счет увеличения активности системы ренин-ангиотензин. Кратковременное (в течение 4 часов) введение каптоприла, приводящего к снижению продукции ангиотензина II, вызывает понижение кровяного давления у ягнят, родившихся с низким весом, но не у нормальных ягнят. У потомства крыс, получавших во время беременности недостаточное количество питательных веществ, использование каптоприла в период от 2 до 4 недель после рождения предотвращало развитие артериальной гипертензии. В исследованиях M. Dodic и соавт. у ягнят с артериальной гипертензией, развившейся вследствие применения дексаметазона на ранних сроках беременности, не было зарегистрировано сосудистой реактивности к экзогенному ангиотензину II в возрасте 5 — 19 месяцев. Тем не менее, тот факт, что ренин-ангиотензиновая система играет важную роль в установке барорефлекса, необходимого для поддержания нормального кровяного давления, не подвергается сомнению. В исследованиях M. Dodic у овец с артериальной гипертонией, развившейся в результате назначения дексаметазона в ранние сроки беременности, не было повышенной сосудистой реактивности на экзогенное введение ангиотензина II в возрасте 5—19 месяцев. Однако, ренин-ангиотензиновая система участвовует в настройке барорефлекса, обеспечивающего пределы колебаний артериального давления. M. Dodic и соавт. показали, что различие в значениях кровяного давления между группами ягнят, подвергавшихся и не подвергавшихся внутриутробному действию дексаметазона, увеличивается с увеличением возраста ягнят, и барорефлекс в основной группе перенастраивается. Предварительные результаты, показывающие, что показатели сердечного выброса у этих овец выше, чем в контрольной группе, хорошо согласуются с данной концепцией динамики барорефлекса.
| Рис 2. Влияние пренатального использования глюкокортикоидов на цифры среднего артериального давления (САД) у потомства женского рода контрольной группы (n=7, светлый фон); ягнят, подвергшихся воздействию дексаметазона (0,48 мг в час в течение 48 часов при сроке беременности 27 дней (n=6, серый фон) и ягнят, подвергшихся воздействию дексаметазона (0,48 мг в час в течение 48 часов при сроке беременности 64 дня (n=7, темный фон) в возрасте 4, 10, 19 и 40 месяцев. (M.Dodic и соавт.) |
Фармакологическое действие
Фармакодинамика
Дексаметазон — метилированное производное фторпреднизолона. Оказывает противовоспалительное, противоаллергическое, десенсибилизирующее и иммунодепрессивное действие.
Взаимодействует со специфическими цитоплазматическими рецепторами ГКС с образованием комплекса, проникающего в ядро клетки и стимулирующего синтез матричной рибонуклеиновой кислоты, последняя индуцирует образование белков, в том числе липокортина, опосредующих клеточные эффекты. Липокортин угнетает фосфолипазу A2, подавляет высвобождение арахидоновой кислоты и подавляет синтез эндоперекисей, простагландинов, лейкотриенов, способствующих процессам воспаления, аллергии и другим.
Белковый обмен: уменьшает количество белка в плазме крови (за счёт глобулинов) с повышением коэффициента альбумин/глобулин, повышает синтез альбуминов в печени и почках, усиливает катаболизм белка в мышечной ткани.
Липидный обмен: повышает синтез высших жирных кислот и триглицеридов, перераспределяет жир (накопление жира происходит преимущественно в области плечевого пояса, лица, живота), приводит к развитию гиперхолестеринемии.
Углеводный обмен: увеличивает абсорбцию углеводов из желудочно-кишечного тракта (ЖКТ); повышает активность глюкозо-6-фосфатазы, что приводит к повышению поступления глюкозы из печени в плазму крови; повышает активность фосфоенолпируваткарбоксилазы и синтез аминотрансфераз, что приводит к активации глюконеогенеза.
Водно-электролитный обмен: задерживает ионы натрия (Na+) и воду в организме, стимулирует выведение ионов калия (K+) (минералокортикоидная активность), снижает абсорбцию ионов кальция (Ca2+) из ЖКТ, «вымывает» ионы Ca2+ из костей, повышает выведение ионов Ca2+почками.
Противовоспалительный эффект связан с угнетением высвобождения эозинофилами медиаторов воспаления; индуцированием образования липокортина и уменьшением количества тучных клеток, вырабатывающих гиалуроновую кислоту; с уменьшением проницаемости капилляров; стабилизацией клеточных мембран и мембран органелл (особенно лизосомальных).
Противоаллергический эффект развивается в результате подавления синтеза и секреции медиаторов аллергии, торможения высвобождения из сенсибилизированных тучных клеток и базофилов гистамина и других биологически активных веществ, уменьшения числа циркулирующих базофилов, подавления развития лимфоидной и соединительной ткани, снижения количества T- и B-лимфоцитов, тучных клеток, снижения чувствительности эффекторных клеток к медиаторам аллергии, угнетения антителообразования, изменения иммунного ответа организма.
При хронической обструктивной болезни лёгких действие основывается главным образом на торможении воспалительных процессов, угнетении развития или предупреждении отёка слизистых оболочек, торможении эозинофильной инфильтрации подслизистого слоя эпителия бронхов, отложении в слизистой оболочке бронхов циркулирующих иммунных комплексов, а также торможении эрозирования и десквамации слизистой оболочки.
Повышает чувствительность бета-адренорецепторов бронхов мелкого и среднего калибра к эндогенным катехоламинам и экзогенным симпатомиметикам, снижает вязкость слизи за счёт угнетения или сокращения её продукции.
Иммунодепрессивный эффект обусловлен торможением высвобождения цитокинов (интерлейкина-1 и интерлейкина-2, гамма- интерферона) из лимфоцитов и макрофагов.
Подавляет синтез и высвобождение гипофизом адренокортикотропного гормона (АКТГ) и вторично — синтез эндогенных ГКС. Угнетает секрецию тиреотропного гормона и фолликулостимулирующего гормона (ФСГ). Подавляет высвобождение бета-липотропина, но не снижает содержание циркулирующего бета-эндорфина.
Повышает возбудимость центральной нервной системы, снижает количество лимфоцитов и эозинофилов, а также увеличивает количество эритроцитов (путём стимуляции выработки эритропоэтинов).
Особенность действия дексаметазона — значительное ингибирование функции гипофиза и практически полное отсутствие минералокортикоидной активности. Дозы 1–1,5 мг в сутки угнетают кору надпочечников; биологический период полувыведения (T½) — 32–72 часа (продолжительность угнетения гипоталамо-гипофизарно-надпочечниковой системы).
По силе глюкокортикостероидной активности 0,5 мг дексаметазона соответствуют примерно 3,5 мг преднизона (или преднизолона), 15 мг гидрокортизона или 17,5 мг кортизона.
ИСПОЛЬЗОВАНИЕ ГЛЮКОКОРТИКОИДОВ ВО ВРЕМЯ БЕРЕМЕННОСТИ
За последние 20 лет значительно снизилась смертность среди недоношенных новорожденных (24-26 недель), что во многом связано с использованием в терапии глюкокортикоидов при возникновении угрозы преждевременных родов назначением сурфактанта после рождения. Если удавалось избежать преждевременных родов, то часто проводились повторные курсы введения глюкокортикоидов. Возникают сомнения, не оказывают ли повторяющиеся инъекции глюкокортикоидов неблагоприятного побочного действия на плод. Опыты на животных (овца) показали, то повторные курсы глюкокортикоидов могут приводить к задержке миелинизации аксонов зрительного нерва. Это позволяет заподозрить возможное повреждающее действие глюкокортикоидов на центральную нервную систему плода. У детей, матери которых во время беременности длительно получали низкие дозы глюкокортикоидов, с целью снижения риска развития проявлений врожденного адреногенитального синдрома отмечались определенные нарушения поведения. Даже при условии, что пренатальное лечение ГК эффективно в устранении вирилизации у плодов женского пола с врожденной надпочечниковой гиперплазией, только в одном из восьми случаев можно расчитывать на возможный положительный эффект от такого лечения. Учитывая материал данного обзора, рекомендуются ограничить до минимума использование ГК во время беременности.
Какая шейка матки во время беременности?
В течение всего периода вынашивания наблюдается множество изменений шейки матки. На это влияют такие факторы, как:
- индивидуальные особенности строения половых органов конкретной женщины;
- гормональный баланс (концентрация женских половых гормонов – эстриола и прогестерона);
- вес плода (или плодов при многоплодной беременности), осуществляющего давление на шейку матки;
- наличие маточных патологий, травм и других дефектов.
Рассмотрим, как изменяются характеристики шейки матки во время беременности при условии, что женщина абсолютно здорова:
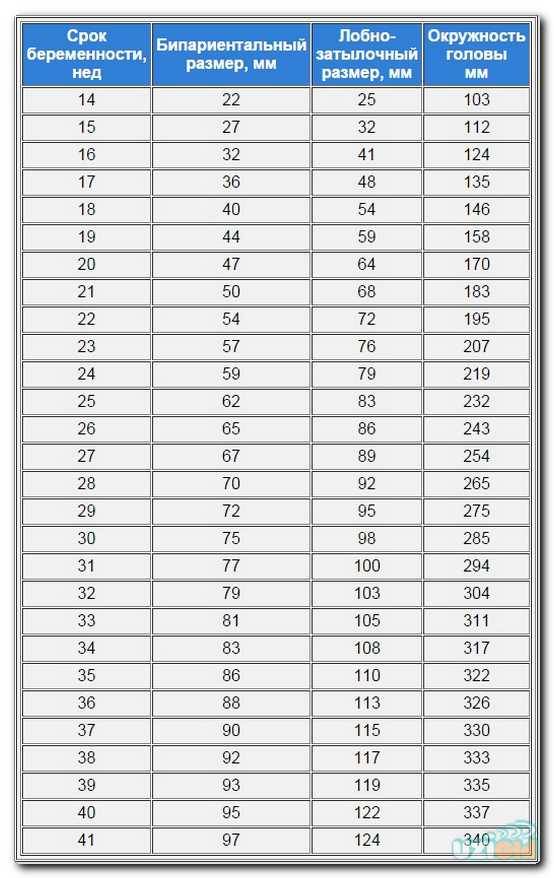
- Размер. Сразу после зачатия и примерно до второй половины беременности шейка матки удлиняется. Так, на 24-й неделе в норме ее длина составляет около 3,5-5 см. Однако, затем по мере роста плода она укорачивается — на 28 неделе до 3,5-4 см, а на 32 неделе – до 3-3,5 см. Помочь отследить эти изменения позволяет ультразвуковое сканирование длины шейки матки. Если женщина здорова, то эта процедура не проводится. Однако, если она имеет осложненную беременность или у нее были выкидыши в прошлом, ей назначается УЗИ, так как чрезмерно короткая шейка матки может спровоцировать преждевременные роды. Также в ходе вынашивания изменяется диаметр цервикального канала. В норме на всем протяжении беременности он остается полностью сомкнутым, и раскрывается лишь непосредственно перед родами. Благодаря этому маточная полость и плод надежно защищены от проникновения инфекций. Слишком раннее раскрытие шейки матки также может спровоцировать выкидыш. Такой риск обусловлен слишком малой длиной органа, слабостью мышц или слишком большим весом плода (а также многоплодием).
- Цвет. До беременности при условии отсутствия у женщины патологий (например, эрозии) шейка матки имеет розовый оттенок. После зачатия в ней увеличивается количество кровеносных сосудов, из-за чего цвет меняется на синеватый. Оценка окраса является одним из дополнительных критериев, позволяющих установить наличие беременности при гинекологическом осмотре (гистероскопии).
- Консистенция. Шейка матки до беременности имеет плотную фактуру, после зачатия под влиянием половых гормонов она становится более мягкой. Железы в цервикальном канале начинают вырабатывать большое количество слизи, которая образует «пробку», надежно запечатывающую матку и плод на весь период вынашивания. Незадолго до родов, когда шейка матки начинает расширяться, это образование отделяется и выходит естественным путем, освобождая проход для плода.
Нормальные физиологические изменения шейки матки варьируются в зависимости от индивидуальных особенностей организма женщины. Например, у некоторых из них может наблюдаться пониженное выделение слизи цервикальными железами, у других – малое изменение длины в процессе вынашивания. Если какие-то изменения происходят в не слишком выраженной степени, это еще не означает наличия какой-либо патологии или высокого риска для самой матери и плода. Однако, по усмотрению врача он может назначить более частое наблюдение шейки матки, чтобы исключить такую возможность.
Сделайте первый шагзапишитесь на прием к врачу!
Записаться на прием к врачу
Предисловие
Предлагаем вашему вниманию перевод статьи по проблеме применения глюкокортикоидных гормонов во время беременности. Даже кратковременное назначение глюкокортикоидов может на несколько десятилетий вперед «перепрограммировать» работу функциональных систем плода и оказать отрицательное воздействие на формирование поведения, контроль артериального давления и на регуляцию обмена веществ. Синтетический гормон «обманывает» организм плода, имитируя стрессовый сигнал со стороны организма матери, заставляя плод раньше времени форсировать мобилизацию резервов. В этом суть отрицательного действия этих препаратов. Это действие еще более усиливается в результате того, что современные «долгоиграющие» глюкокортикоиды (дексаметазон, метипред) не поддаются инактивирующему действию ферментных систем плаценты и оказывают продолжительное воздействие на органы и ткани-мишени. Оказывая иммуносупрессивное действие, эти препараты ослабляют организм беременной женщины по отношению к вирусным инфекциям.
Глюкокортикоидные гормоны должны применяться при беременности только тогда, когда польза от их применения значительно превышает возможный риск долговременных отрицательных последствий. К таким показаниям относится угроза преждевременных родов (глюкокортикоиды назначаются однократно или в виде очень короткого курса и позволяют значительно улучшить готовность недоношенного ребенка к самостоятельному существованию), активные аутоиммунные и ревматические заболевания (глюкокортикоиды позволяют резко снизить риск тяжелых осложнений у женщины) и врожденная внутриутробная гиперплазия коры надпочечников у плода (это наследственное заболевание, которое требует специальной антенатальной диагностики; применение глюкокортикоидов позволяет избежать вирилизации плода женского пола).
Авторы ничего не пишут о назначении глюкокортикостероидов с целью сохранения беременности. И это не случайно. На Западе подобное «лечение» было отвергнуто еще в конце 1950-х — начале 1960-х годов, поскольку не существует веских доказательств его эффективности. Развитие современных методов диагностики и лечения невынашивания беременности, в частности, в рамках иммунологии репродукции, не оставляет места подобной устаревшей практике.
ЭКСПЕРИМЕНТЫ НА ЖИВОТНЫХ
Эксперименты, проводимые на животных (морские свинки, крысы, овцы), подтвердили взаимосвязь между задержкой внутриутробного развития и формированием артериальной гипертензии или обменных нарушений во взрослом возрасте. Независимо от причины, приводящей к нарушению внутриутробного развития у животных (нарушение маточного кровотока, анемия у матери, недостаточно калорийное питание, либо низкобелковая диета во время беременности), результат получался один и тот же. Потомство крыс, получавших низкобелковую диету во время беременности и лактации, имело существенные изменения в морфометрии печени и значительное снижение активности глюкокиназы в перивенозных областях. В полученном потомстве морских свинок, имевших при рождении низкую массу тела, у молодых взрослых самцов развивалась артериальная гипертензия, отмечалось уменьшение объема мышечной ткани и увеличение жировой ткани, нарушение толерантности к глюкозе, нарушенный гомеостаз холестерина. Интереснее всего, что недостаточное питание в первой половине беременности у животных с большой продолжительностью беременности, как, например, овцы, приводило к рождению потомства, у которого к 3-х месячному возрасту развивалась артериальная гипертония.