SQLITE NOT INSTALLED
Как попасть на лечение в Израиле
Принимая решение о лечении в Израиле, пациент с дефектами развития внутренних органов, в том числе и межпредсердной перегородки, получает множество преимуществ, среди которых — применение последних научных рекомендаций и инновационного оборудования, приемлемая стоимость, быстрое выздоровление прооперированных детей.
Благодаря слаженной работе специалистов разного профиля хирурги справляются с патологией даже в очень сложных случаях. Незнание языка не станет помехой в общении — каждого больного сопровождает русскоязычный консультант.
Чтобы попасть в «Хадассу», нужно заполнить электронную анкету. С вами свяжется сотрудник международного отдела, предоставит нужную информацию и ответит на дополнительные вопросы. Воспользовавшись нашими услугами, вам не придется переплачивать посредникам — вся оплата производится только в кассу медцентра перед госпитализацией в стационар..
9.2. ТЕТРАДА ФАЛЛО
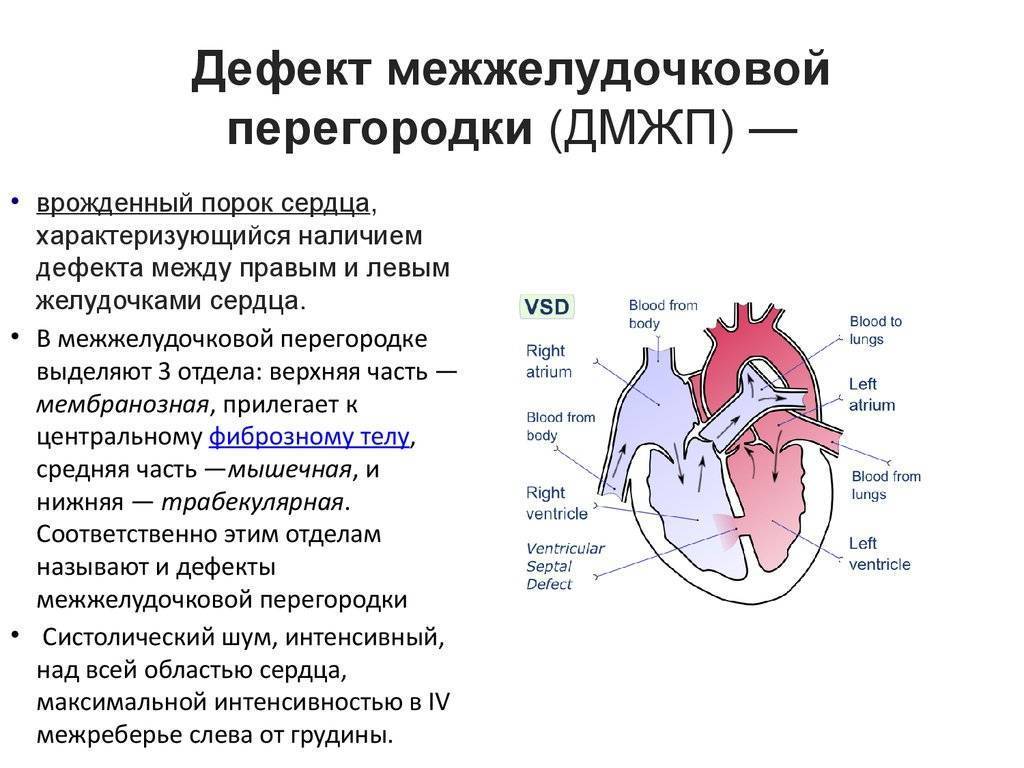
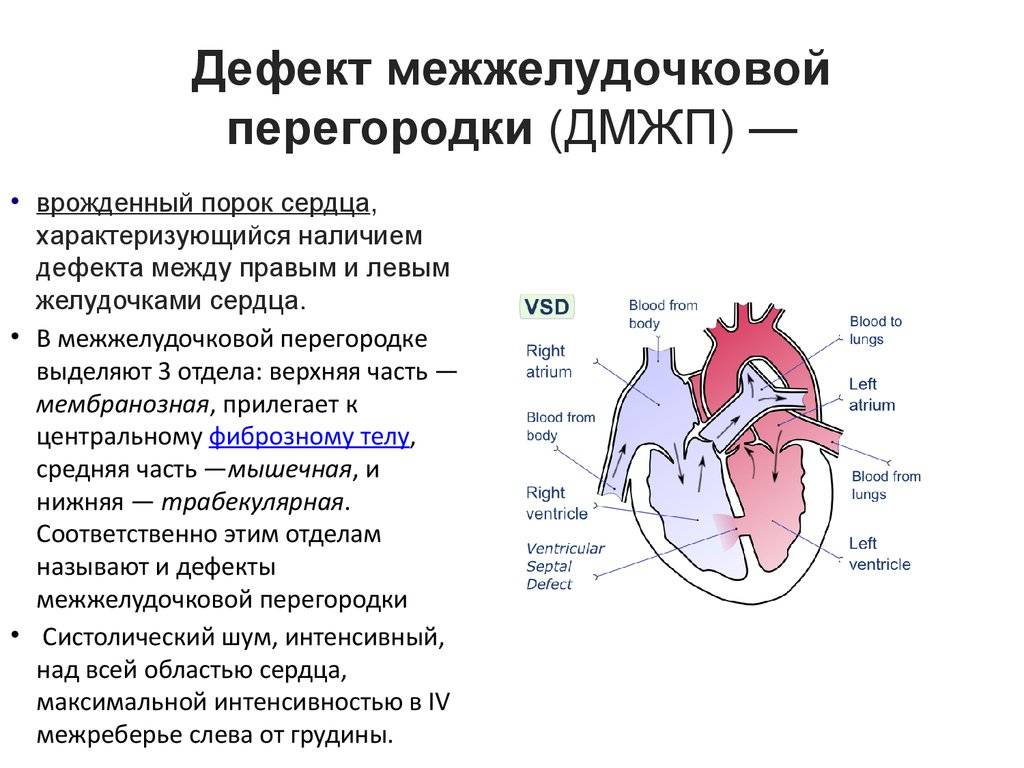
Тетрада Фалло — врождённый порок сердца, характеризующийся наличием четырёх компонентов: 1) большого высокорасположенного ДМЖП; 2) стеноза лёгочной артерии; 3) декстропозиции аорты; 4) компенсаторной гипертрофии правого желудочка.
Распространённость
Тетрада Фалло составляет 12-14% всех врождённых пороков сердца.
ГЕМОДИНАМИКА
При тетраде Фалло аорта располагается над большим ДМЖП и над обоими желудочками, в связи с чем систолическое давление в правом и левом желудочках одинаковое (рис. 9-2). Главный гемодинамический фактор — отношение между сопротивлением кровотоку в аорте и в стенозированной лёгочной артерии.
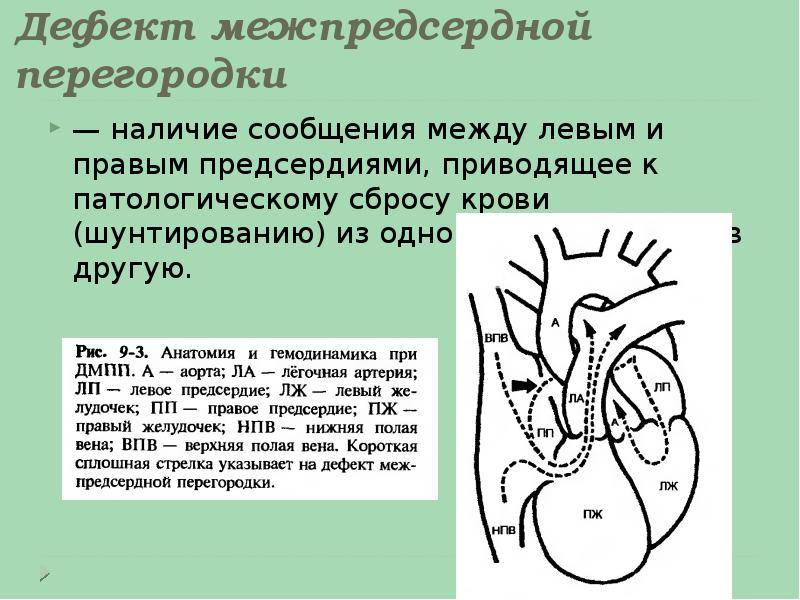
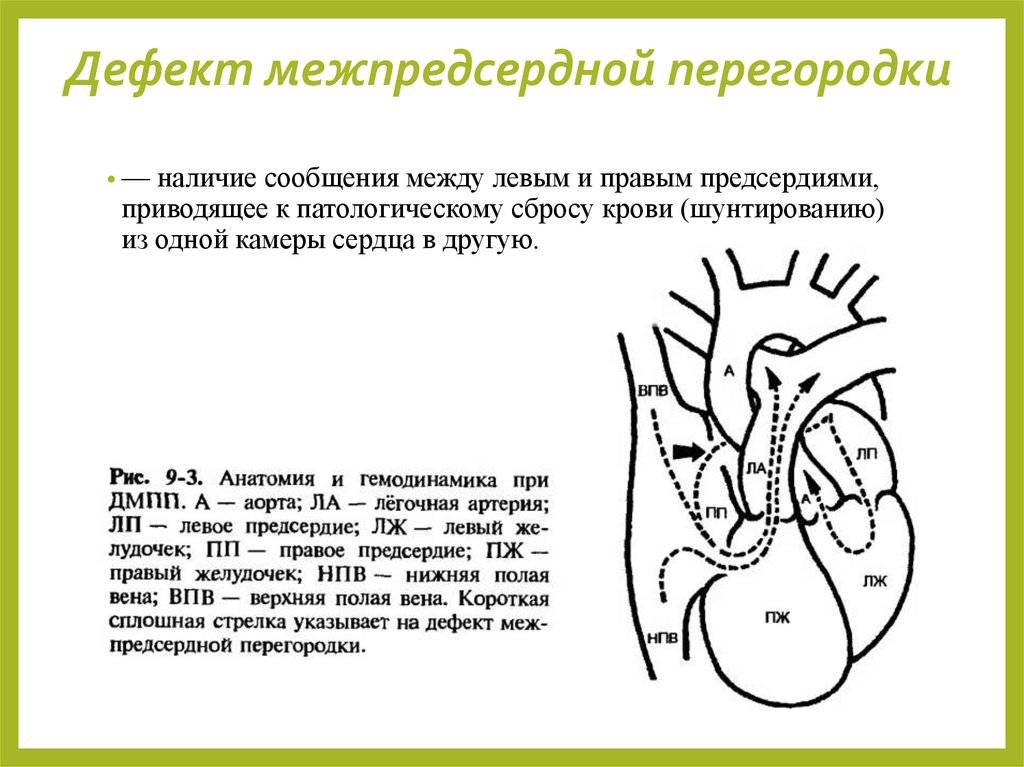
Рис. 9-2. Анатомия и гемодинамика при тетраде Фалло. А — аорта; ЛА — лёгочная артерия; ЛП — левое предсердие; ЛЖ — левый желудочек; ПП — правое предсердие; ПЖ — правый желудочек; НПВ — нижняя полая вена; ВПВ — верхняя полая вена. Короткая стрелка указывает на дефект межжелудочковой перегородки, длинная — на подклапанный стеноз лёгочной артерии.
• При небольшом сопротивлении в лёгочных сосудах лёгочный кровоток может быть вдвое больше кровотока в большом круге кровообращения, и насыщение артериальной крови кислородом может быть нормальным (ацианотичная тетрада Фалло).
• При значительном сопротивлении лёгочному кровотоку возникает сброс крови справа налево, в результате чего возникают цианоз и полицитемия.
Стеноз лёгочной артерии может быть инфундибулярным или комбинированным, реже клапанным (подробнее об этом см. в главе 8 «Приобретённые пороки сердца»).
При физической нагрузке происходит увеличение притока крови к сердцу, но кровоток через малый круг кровообращения не возрастает из-за стенозированной лёгочной артерии, и избыточное количество крови сбрасывается в аорту через ДМЖП, поэтому цианоз усиливается. Возникает гипертрофия, что приводит к усилению цианоза. Гипертрофия правого желудочка развивается вследствие постоянного преодоления препятствия в виде стеноза лёгочной артерии. В результате гипоксии развивается компенсаторная полицитемия — увеличивается количество эритроцитов и гемоглобина. Развиваются анастомозы между бронхиальными артериями и ветвями лёгочной артерии. У 25% больных обнаруживают правостороннее расположение дуги аорты и нисходящей аорты.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА
Жалобы
Основной жалобой взрослых больных тетрадой Фалло является одышка. Кроме того, могут беспокоить боли в сердце без связи с физической нагрузкой, сердцебиение. Больные склонны к лёгочным инфекциям (бронхиты и пневмонии).
Осмотр
Отмечают цианоз, степень выраженности которого может быть различной. Иногда цианоз настолько выражен, что синеют не только кожные покровы и губы, но также слизистая оболочка полости рта, конъюнктива. Характерно отставание в физическом развитии, изменение пальцев («барабанные палочки»), ногтей («часовые стёкла»).
Пальпация
Обнаруживают систолическое дрожание во II межреберье слева от грудины над участком стеноза лёгочной артерии.
Аускультация сердца
Выслушивают грубый систолический шум стеноза лёгочной артерии во II-III межреберьях слева от грудины. II тон над лёгочной артерией ослаблен.
Лабораторные исследования
Общий анализ крови: высокий эритроцитоз, повышение содержания гемоглобина, СОЭ резко снижена (до 0-2 мм/ч).
Электрокардиография
Электрическая ось сердца обычно смещена вправо (угол α от +90° до +210°), отмечают признаки гипертрофии правого желудочка.
Эхокардиография
ЭхоКГ позволяет обнаружить анатомические составляющие тетрады Фалло.
Рентгенологическое исследование
Отмечают повышенную прозрачность лёгочных полей из-за уменьшения кровенаполнения лёгких. Контуры сердца имеют специфическую форму «деревянного башмака сабо»: уменьшенная дуга лёгочной артерии, подчёркнутая «талия сердца», закруглённая и приподнятая над диафрагмой верхушка сердца. Дуга аорты может быть справа.
ОСЛОЖНЕНИЯ
Наиболее часто возникают инсульты, ТЭЛА, выраженная сердечная недостаточность, инфекционный эндокардит, абсцессы мозга, разнообразные аритмии.
ЛЕЧЕНИЕ
Единственный метод лечения — хирургический (радикальная операция — пластика дефекта, устранение стеноза лёгочной артерии и смещение аорты). Иногда хирургическое лечение состоит из двух этапов (первым этапом ликвидируют стеноз лёгочной артерии, а вторым проводят пластику ДМЖП).
Современные виды операций при ДМЖП
Каждая из операций имеет свои показания и предпочтительна в определенных клинических ситуациях. Решение о выборе вмешательства принимается коллегиально с учетом всех обстоятельств. Выполняется:
- Традиционная торакотомическая операция с вскрытием грудной клетки и подключением аппарата искусственного кровообращения. Продолжается около 6 часов и требует довольно длительной реабилитации. Но позволяет одновременно устранить другие аномалии сердца и ликвидировать ДМЖП при любом расположении дефекта. В зависимости от положения и размеров его ушивают или накладывают «заплату» из тканей сердечной сумки (перикарда) пациента или синтетического материала.
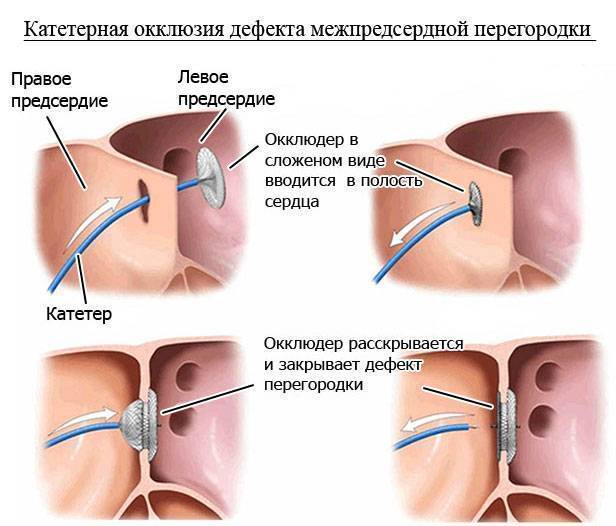
- Рентгенхирургическая эндоваскулярная (внутрисосудистая) операция показана в шести случаях из десяти. Может быть выполнена, если ДМЖП – единственный порок сердца у ребенка, дефект расположен не ближе нескольких миллиметров от края перегородки, и вес пациента не менее 5 кг. У совсем маленьких детей настолько узкие сосуды, что не позволяют ввести в них катетер и доставить с его помощью к сердцу окклюдер для закрытия дефекта. Это синтетическое приспособление подбирается в соответствии с размером и расположением дефекта, доставляется в катетере к месту назначения в сложенном виде и там расправляется, перекрывая патологический кровоток. На протяжении полугода, пока окклюдер врастает в окружающие ткани, небольшое просачивание крови сохраняется, но оно не имеет существенного значения. А через шесть месяцев отверстие оказывается уже герметично закрытым, и ребенок становится практически здоровым.
- Гибридная операция проводится кардиохирургом и эндоваскулярным хирургом. Выполняется у маленьких детей с узкими для катетера сосудами, на работающем сердце, без аппарата искусственного кровообращения. Кардиохирург вскрывает грудную клетку, делает прокол в сердце для катетера. Далее эндоваскулярный хирург вводит его и устанавливает окклюдер, как при эндоваскулярной операции.
Факторы развития
Заболевание встречается, как самостоятельная патология, так и совмещенная с иными дефектами развития органа. Нарушения появляются уже в эмбриональном периоде, когда происходит формирование системы кровообращения в первом триместре беременности матери. Повлиять на естественный механизм нормального развития способны любые неблагоприятные факторы внешней и внутренней природы:
- генетическая предрасположенность, семейственность сердечных пороков, наличие старших родственников с синдромом Холта-Орама;
- вирусные болезни матери;
- эндокринные нарушения в организме женщины (особенно диабетический синдром);
- систематическое отравление плода запрещенными медикаментами, алкоголем;
- проживание и работа в экологически неблагоприятных местностях;
- повышенный радиационный фон в местах постоянного пребывания;
- осложнения беременности (угрозы прерывания, патологические токсикозы).
В перегородке между предсердиями может быть одно или несколько отверстий разного диаметра. От размеров просвета зависит скорость развития сердечно-легочных нарушений в работе органов, развитие дыхательной недостаточности и цианоза (посинения кожных покровов даже в состоянии покоя). Из-за неправильного распределения давления в предсердиях происходит выбухание правой стороны сердца, что приводит к сужению легочной артерии, повышению давления, дыхательной недостаточности.
Тромбы в левых отделах сердца
Чаще всего тромбы в левых полостях сердца встречаются на фоне трех заболеваний.
В зоне риска находятся люди:
- со стенозом митрального клапана;
- с мерцательной аритмией (фибрилляцией предсердий):
- с постинфарктной аневризмой левого желудочка.
Тромбы в левых отделах сердца – риск возникновения артериальных тромбоэмболий, ишемических атак или инфарктов мозга! При локализации тромбов в левых полостях сердца также могут поражаться артерии почек, верхних и нижних конечностей, артерии кишечника.
Инфаркты и инсульты
Если тромб отрывается, он может распространиться с током крови и закрыть просвет сосуда! При перекрытии сосуда нарушается кровообращение, что приводит к кислородному голоданию и некрозу тканей. Это может вызвать такие осложнения, как инфаркт миокарда, ТЭЛА и даже смерть.
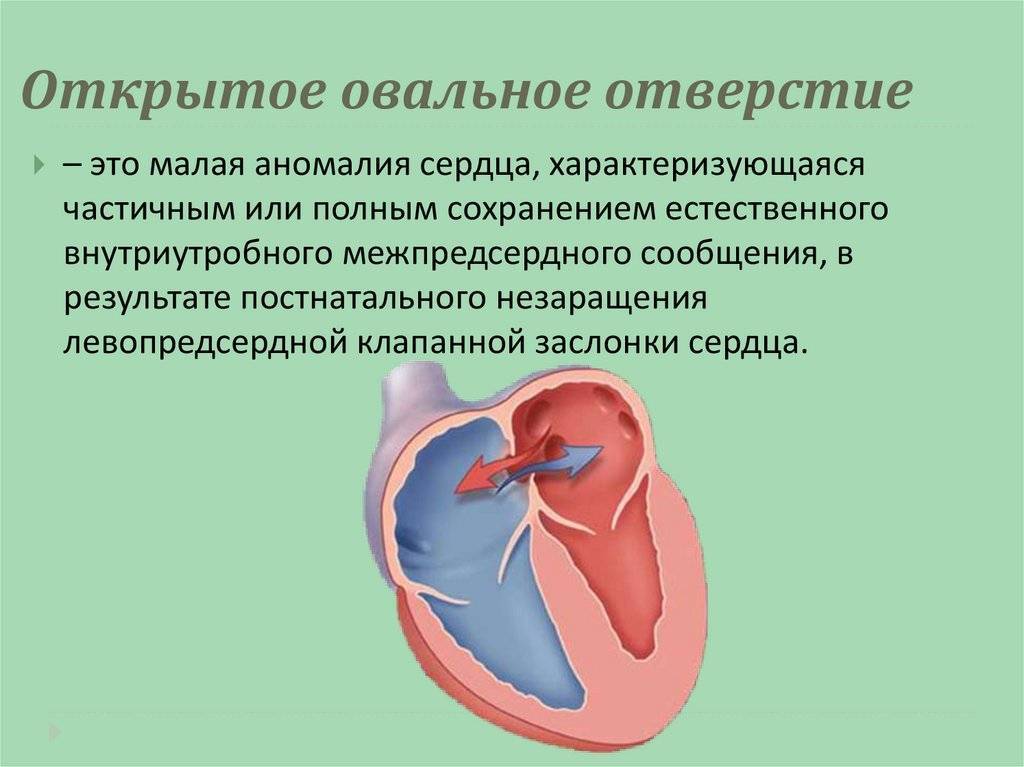
При наличии открытого овального окна в межсердечной перегородке тромбы из вен нижних конечностей, таза могут переместиться из правого предсердия в левое и далее с током крови попасть в мозг. В результате также наступает инсульт.
Тромбы, образующиеся при аневризме сердца
После перенесенного инфаркта в левом желудочке могут образоваться пристеночные тромбы. Их видят специалисты с помощью эхокардиографии. Это основной вид диагностики для обнаружения тромбов в полостях сердца. В случае их обнаружения специалист может назначить антикоагулянты (при отсутствии противопоказаний).
Тромбы, образующиеся при стенозе митрального клапана
Бывает особая разновидность — шаровидный тромб в левом предсердии. Такой тромб образуется при стенозе митрального клапана, при котором нарушается отток из левого предсердия в левый желудочек.
При мерцательной аритмии тромбы обычно локализуются в ушках левых предсердий. Ушко представляет собой выпячивание предсердия (оно похоже на мешочек). Тромбы ушка левого предсердия можно выявить чаще всего только при чреспищеводной Эхо-КГ. С помощью эхокардиографии их обнаружить очень трудно.
Часто задаваемые вопросы
Каким способом производится обезболивание при операции?
Анестезия может быть как местной, так и общей. Выбор зависит от решения врачей, которые будут проводить эту операцию. Если пациент хорошо переносит общий наркоз, то вполне возможен этот вариант, чтобы исключить волнение и неприятные ощущения.
Как осуществляется контроль за выполнением эндоваскулярного вмешательства?
Достаточно часто требуется уточнение строения дефекта, тогда на этом этапе выполняют ангиографию – рентгеноконтрастное исследование сосудов. Окклюдер подбирают индивидуально, его помещают в катетер и доводят до сердца. Затем, под контролем с помощью видеоизображений, производится установка и раскрытие окклюдера.
Если требуется дополнительный контроль над работой сердца, то используют эхокардиограф с датчиком, помещаемым в пищевод. Чреспищеводная Эхокардиография позволяет наблюдать за состоянием сердечной мышцы в режиме реального времени.
Как проводится реабилитация после манипуляции?
Общий срок проведения операции – не более 1,5-2 часов. Обычно процедура занимает около часа. Госпитализация производится на срок от суток до недели – зависит от индивидуального состояния пациента. После операции назначают прием антикоагулянтов – препаратов, препятствующих образованию тромба, а также антибиотиков, которые позволяют избежать бактериальной инфекции сердца.
Если в послеоперационном периоде не возникает осложнений, то требуется контрольное обследование через 3-4 недели. Иногда возникают такие симптомы, как боли и одышка. При появлении осложнений необходимо обратиться к лечащему врачу – при правильно проведенной операции побочные эффекты не развиваются.
Преимущества эндоваскулярной операции
Это относительно молодой метод лечения – эндоваскулярные операции на сердце стали возможны в 21 веке. Эндоваскулярным называют лечение, которое не требует хирургического полостного вмешательства. Операцию выполняют с помощью специального устройства, которое называется окклюдер.
Эндоваскулярное лечение подходит большей части пациентов с дефектом межжелудочковой перегородки. Операцию можно проводить для детей, если они достигли веса в 5 кг – у тех, кто меньше, недостаточный просвет сосудов. Если позволяет состояние пациента, то процедуру лучше провести как можно быстрее. Для детей рекомендованный интервал – от 1 года до 3.
Для проведения манипуляций требуется рентгенооперационная – это стерильное помещение, оснащенное специальным оборудованием для контроля над манипуляциями хирурга. Окклюдер – это устройство, которое раскрывается и выполняет функцию заплатки. Его помещают в катетер, который проводят к сердцу через крупный сосуд. Таким образом, не требуется никаких разрезов или повреждений. Достаточно одного прокола в месте введения катетера – обычно это бедро или верхняя конечность. Правильно установленный окклюдер перекрывает патологический сброс крови из одного желудочка в другой. Если он установлен неправильно или смещается после операции, достаточно повторить все манипуляции снова и установить его в нужное положение.
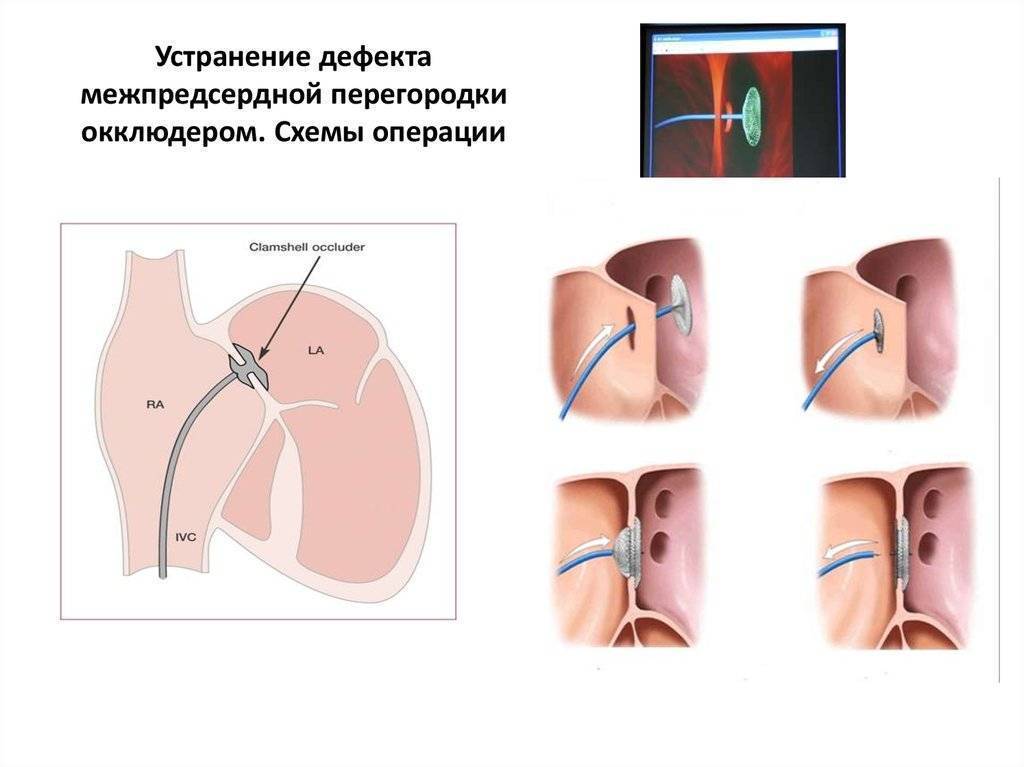
Эндоваскулярный (внутрисосудистый) метод закрытия ДМПП
Схема имплантацииокклюдера
Эндоваскулярный (внутрисосудистый) метод закрытия дефекта межпредсердной пререгородки (ДМПП) начал развиваться с 1975 года. Устройство для эндоваскулярного закрытия дефекта получило название окклюдер. В последующие годы было испытано несколько поколений окклюдеров, но только с 2001 года устройства получили международное одобрение для использования в повседневной медицинской практике.
Современные окклюдеры обладают необходимыми качествами для использования:
- имеют легкую и удобную систему доставки непосредственно к дефекту,
- полностью выполняют отверстие дефекта,
- обладают способностью к репозиционированию и извлечению в сложных анатомических случаях.
Этапы эндоваскулярной имплантации окклюдера ДМПП
В мировой медицинской практике эндоваскулярное закрытие ДМПП стало операцией выбора, то есть первоочерёдным и оптимальным методом лечения. Закрытие вторичного ДМПП с помощью эндоваскулярной технологии с использованием окклюдера возможно в 80% случаев. Возможность эндоваскулярного метода лечения определяется анатомо-морфологическими характеристиками дефекта.
Преимущества методики:
- отсутствие разрезов и швов на теле;
- проведение операции через прокол бедренной вены;
- без наркоза, под местным обезболиванием;
- отсутствие длительной реабилитации после проведения операции;
- возможность вернуться к повседневной жизни через несколько дней после операции.
Для определения возможности выполнения операции эндоваскулярного закрытия ДМПП проводится трансторакальное Эхо-Кг и чреспищеводное Эхо-Кг.
После оценки показателей данных исследований принимается решение об анатомической и морфологичсекой возможности выполнения операции.
Статистика и прогноз лечения дефекта межпредсердной перегородки у детей в Израиле
Согласно статистически данным, до 20 % всех врожденных пороков сердца приходится на долю аномалий межпредсердной перегородки. Порок не способен самостоятельно пропасть в процессе роста ребенка, поэтому это еще и самое частое врожденное нарушение сердца, которое диагностируют после 3 лет.
Прогноз заболевания зависит от выраженности изменений. Небольшие отклонения совместимы с жизнью и нередко обнаруживаются в после 45 – 50 лет.
|
При крупных дефектах перегородки и отсутствии терапии длительность жизни не превышает 40 лет. |
Патологические изменения затрагивают такие органы и структуры:
- миокард;
- кровеносные сосуды;
- легкие;
- печень;
- почки.
Смерть наступает от хронической правожелудочковой недостаточности, нарушений проводимости сердечного импульса, аритмий. Реже пациент умирает от легочной гипертензии.
Врачи «Хадассы» успешно устраняют врожденные пороки кардиоваскулярной системы. Главные факторы, определяющие исход операции, — возраст и интенсивность изменений в миокарде.
|
При своевременном обращении в наш центр вероятность благополучного исхода приближается к 100 %. Практически все больные после операции возвращаются к полноценной жизни. |
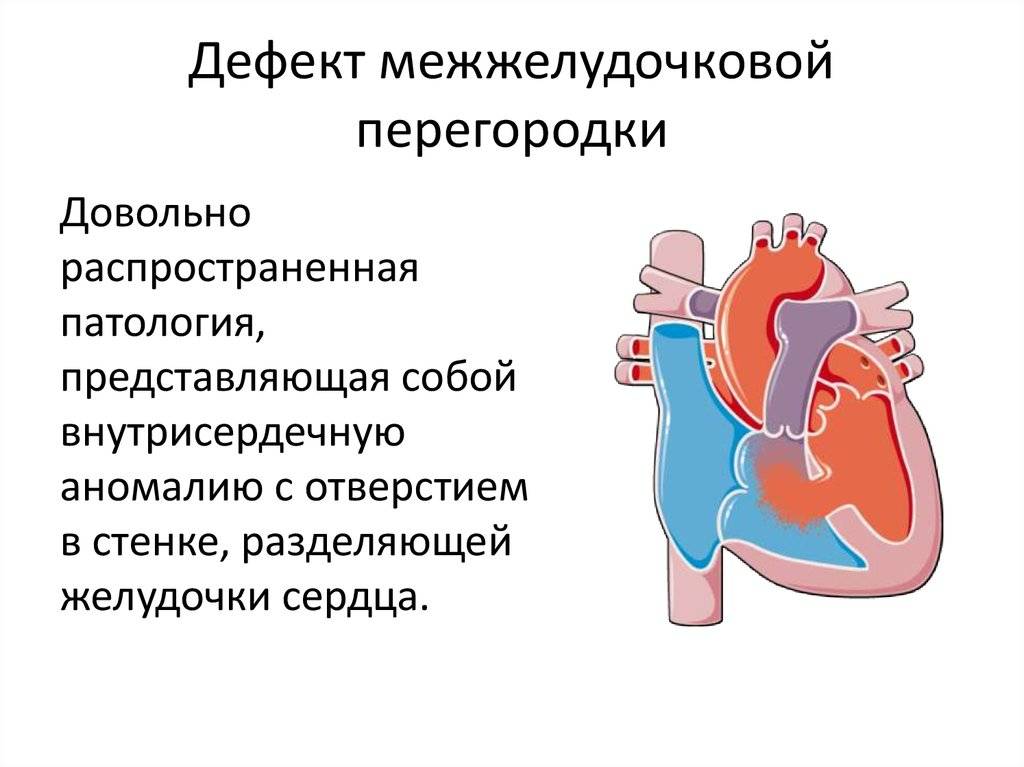
Лечение дефекта
Лечение не требуется в двух случаях: если дефект состоит из мышечной ткани (вне зависимости от размера и локализации от него можно ожидать самостоятельного закрытия), а также, если отверстие небольшое, а ребенку не более двух лет. Маленькие повреждения могут затягиваться в раннем детском возрасте – поэтому требуется только наблюдение.
Остальным пациентам необходима специфическая операция – закрытие дефекта межжелудочковой перегородки. Несмотря на то, что процедуру стараются провести как можно раньше, иногда требуется выждать некоторое время. В таком случае назначают поддерживающую медикаментозную терапию, призванную снизить нагрузку на сердечную мышцу и поддержать сосуды. Существует два принципиально разных подхода к хирургии: эндоваскулярное лечение и открытая операция. Последний вариант сложный технически – требуется специальное оборудование для поддержания искусственного кровообращения, а реабилитационный период может протекать с осложнениями.
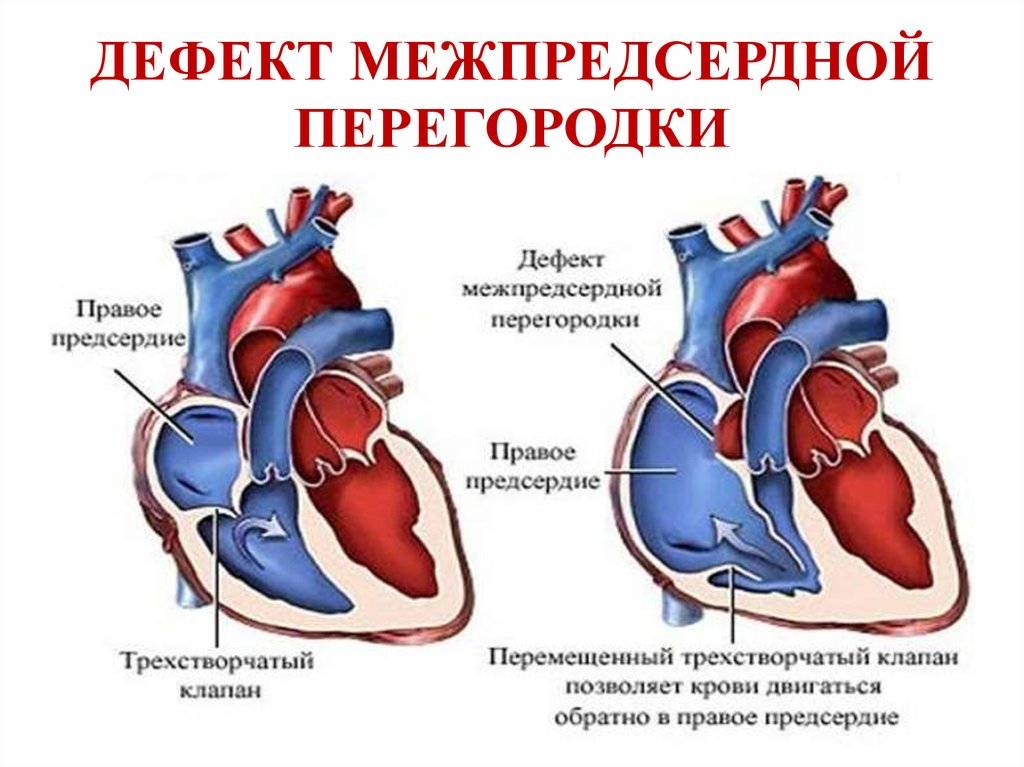
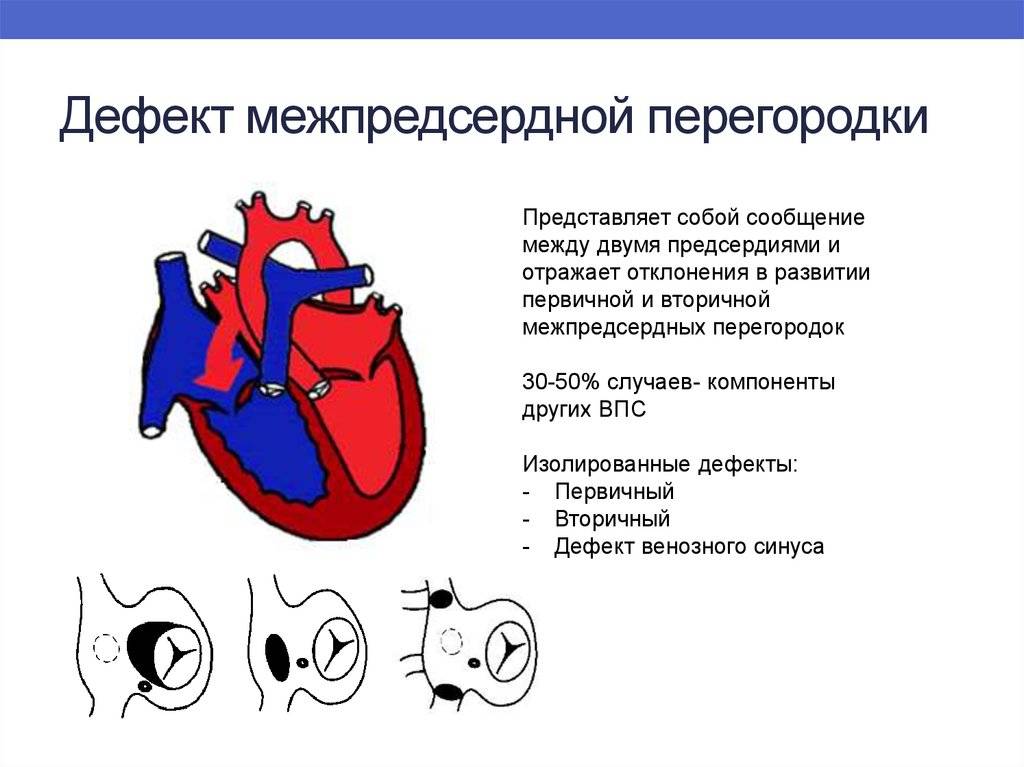
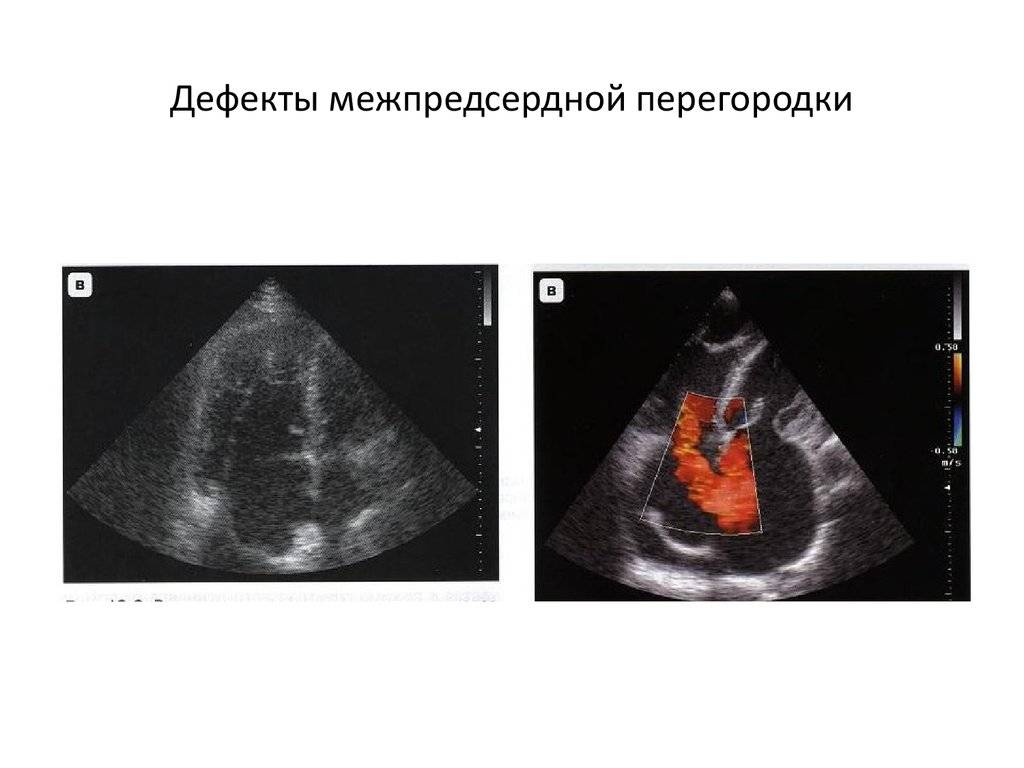
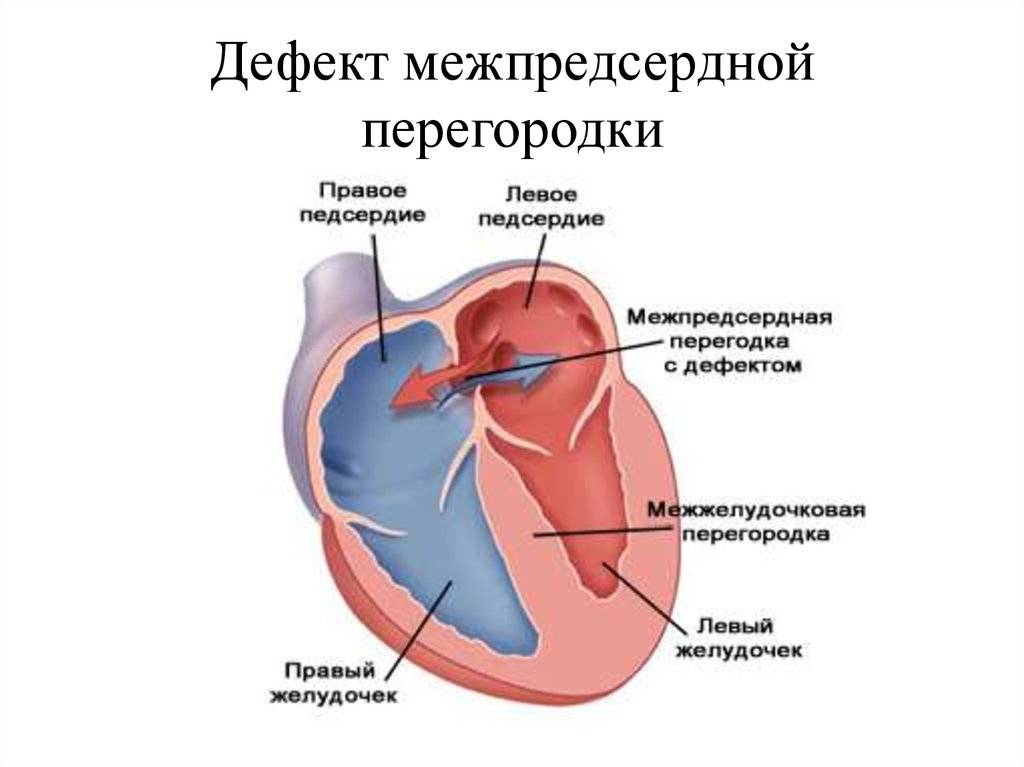
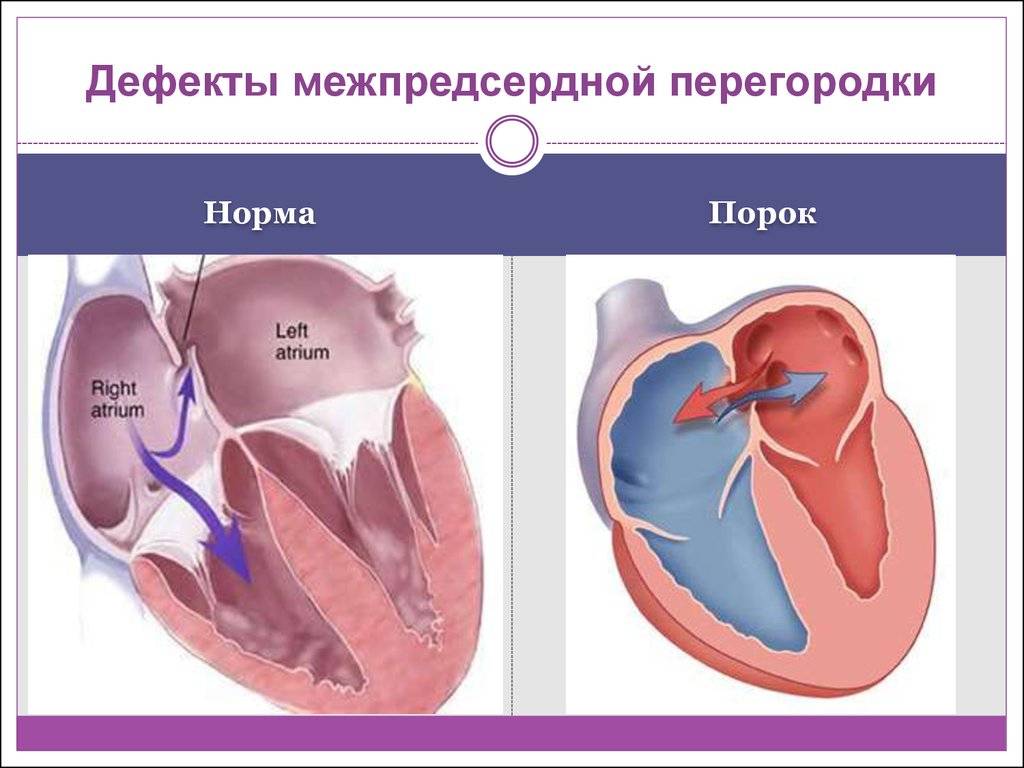
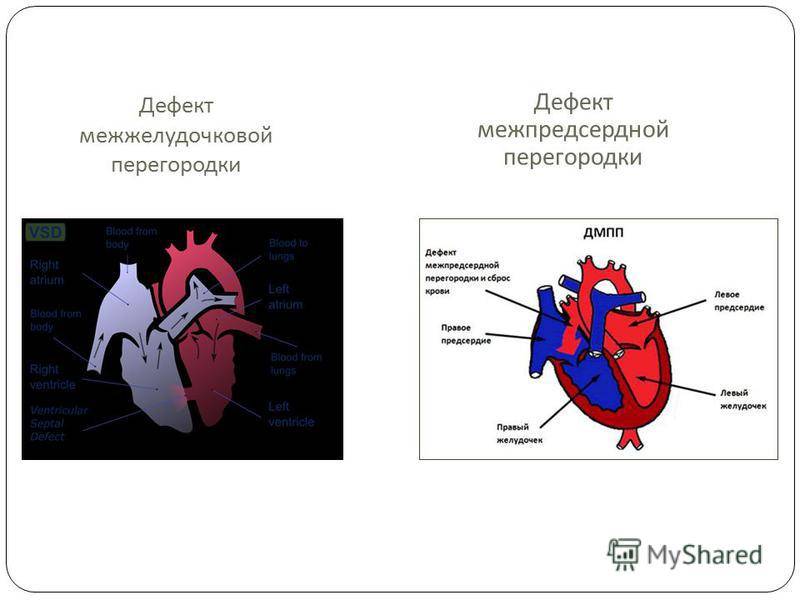
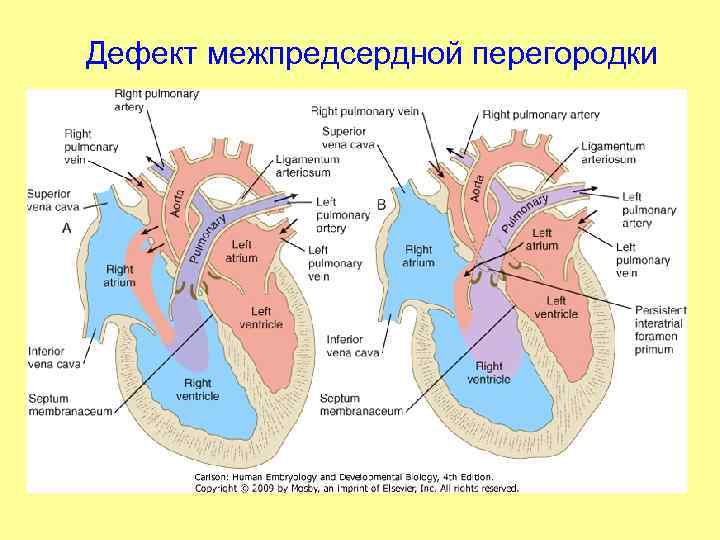
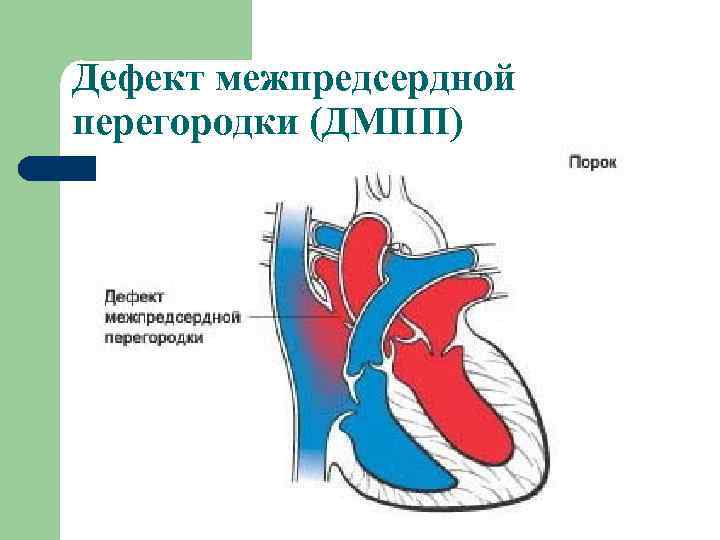
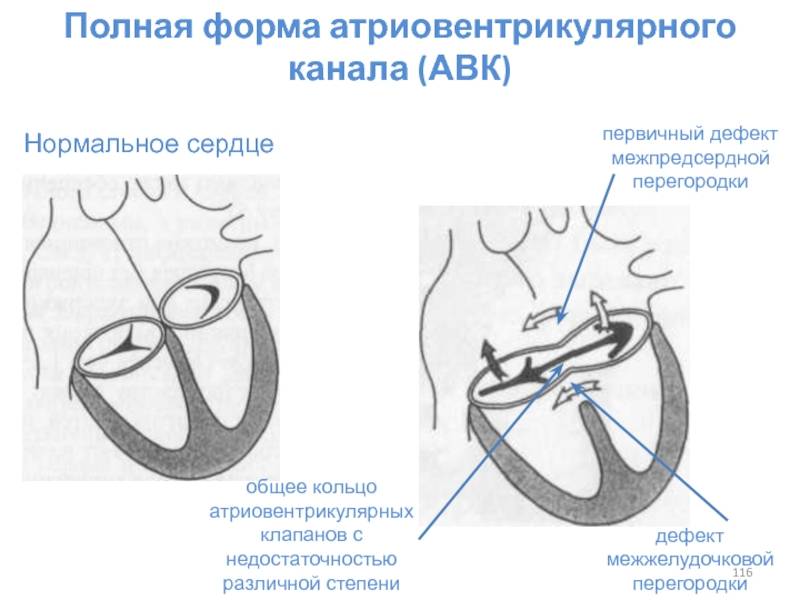
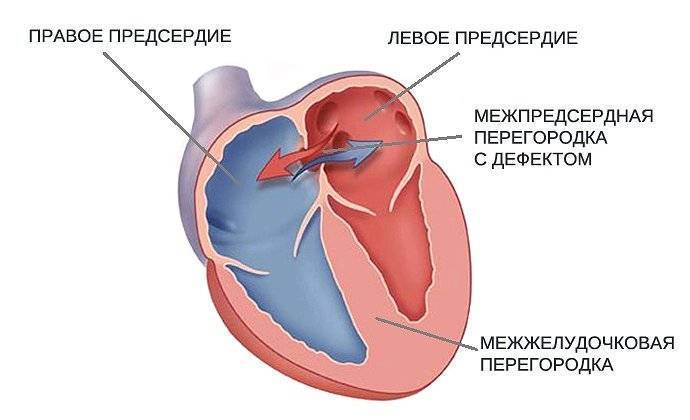
Дефекты межпредсердной перегородки (ДМПП)
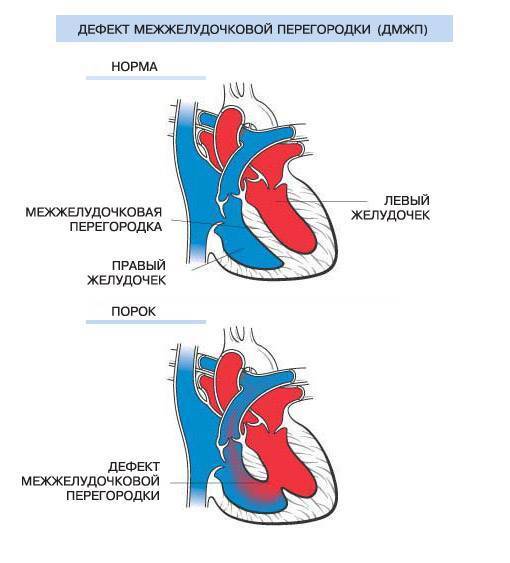
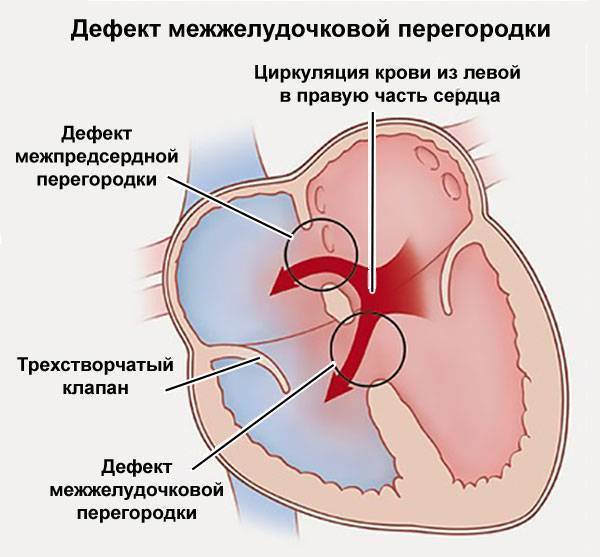
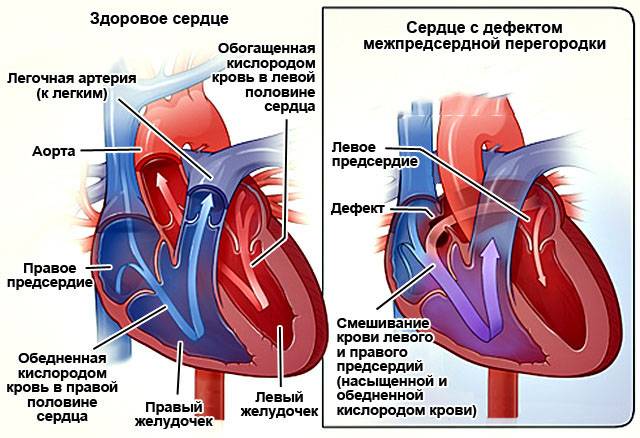
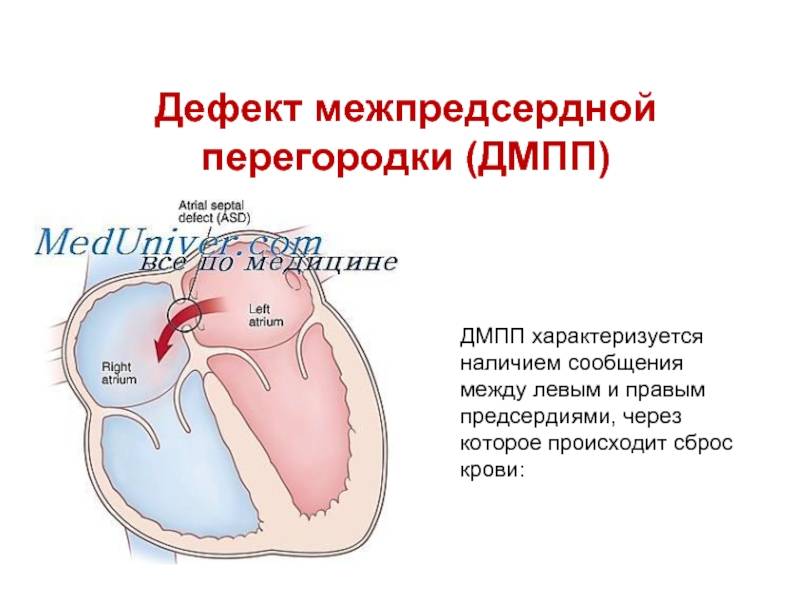
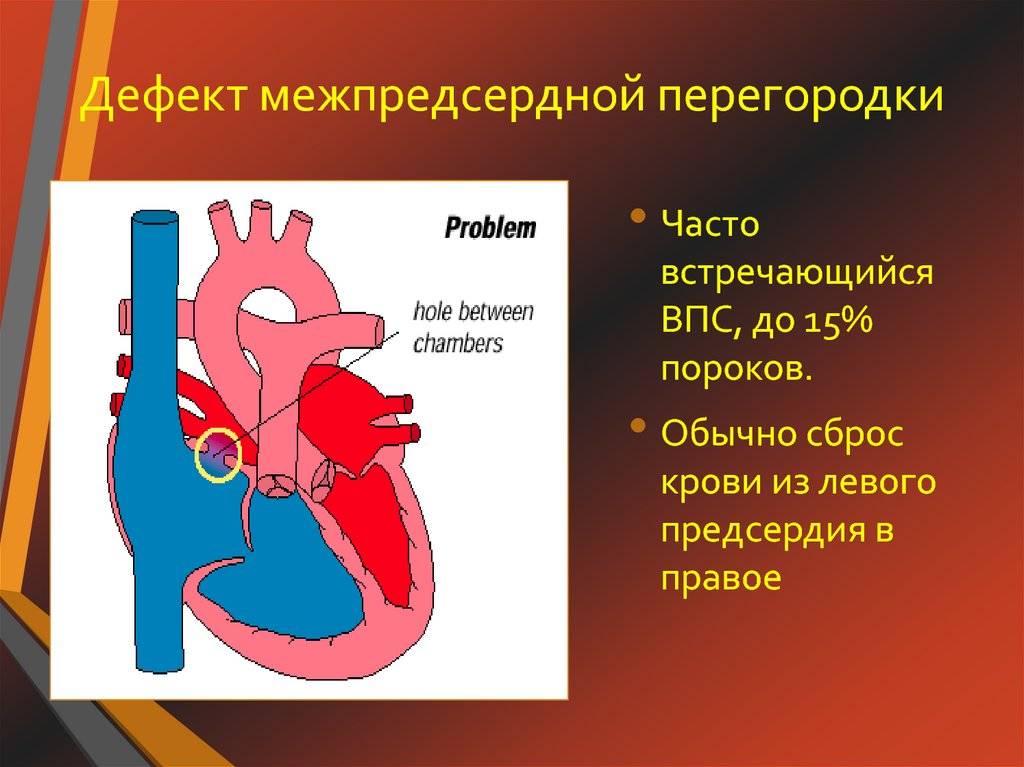
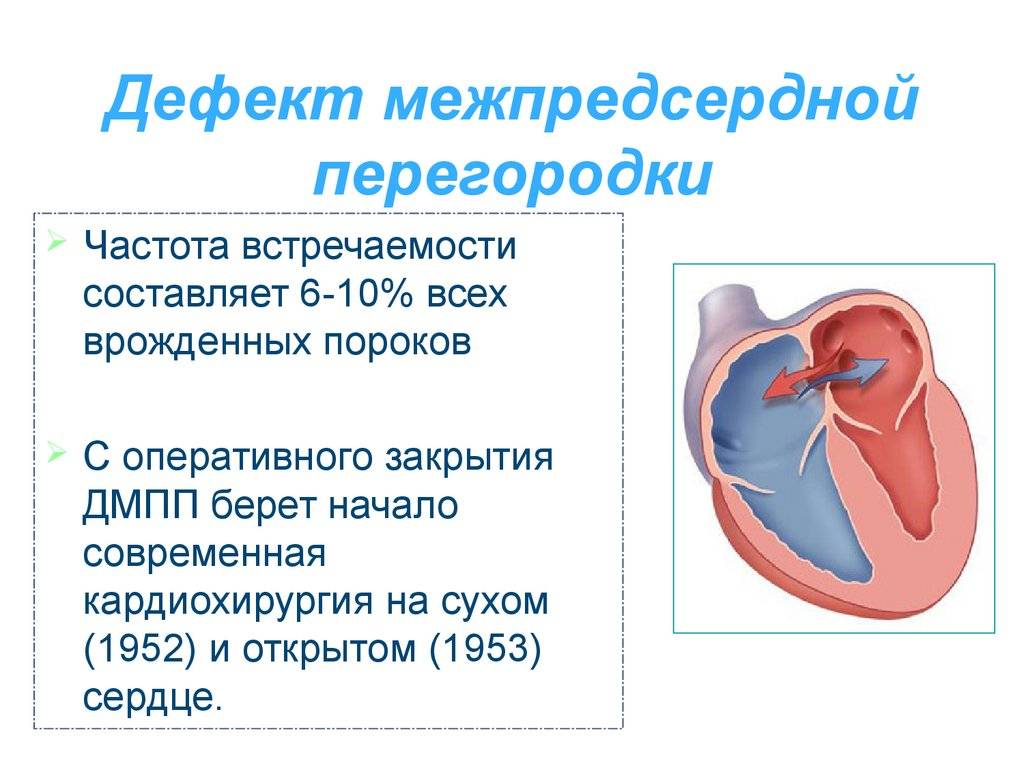
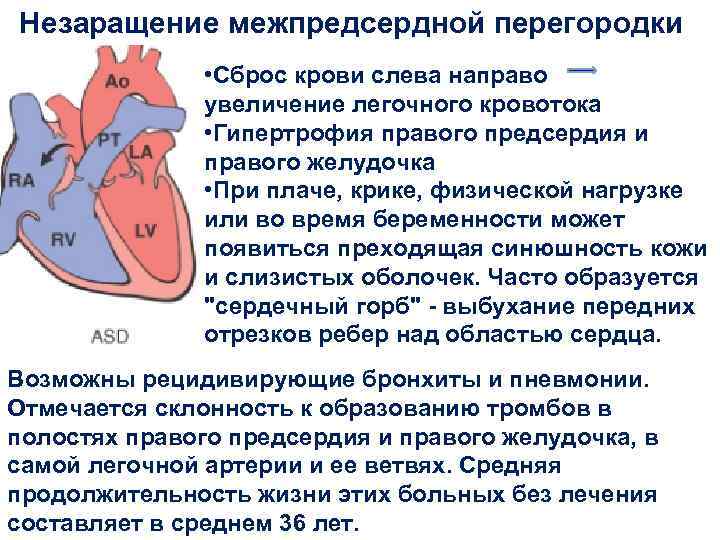
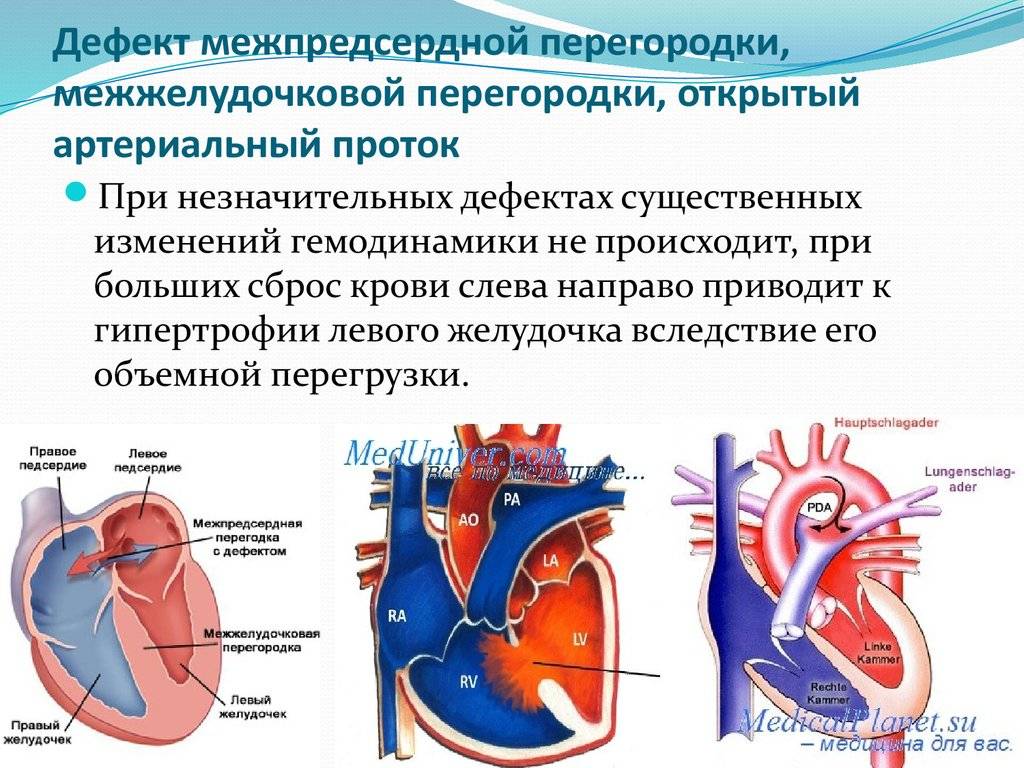
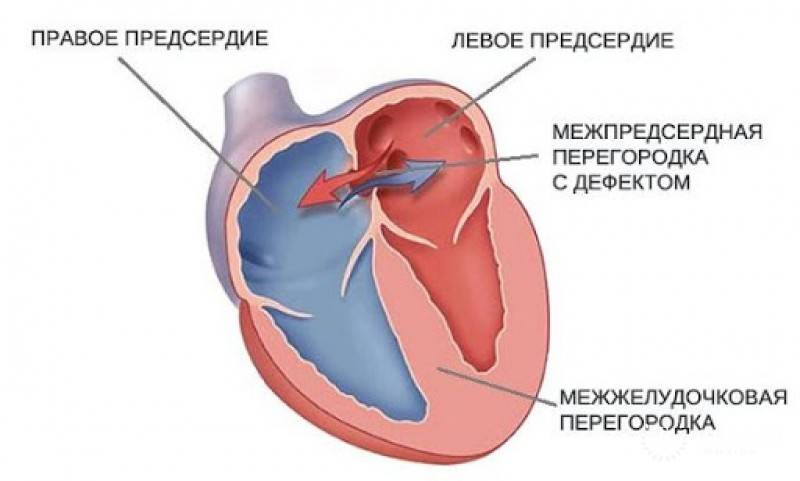
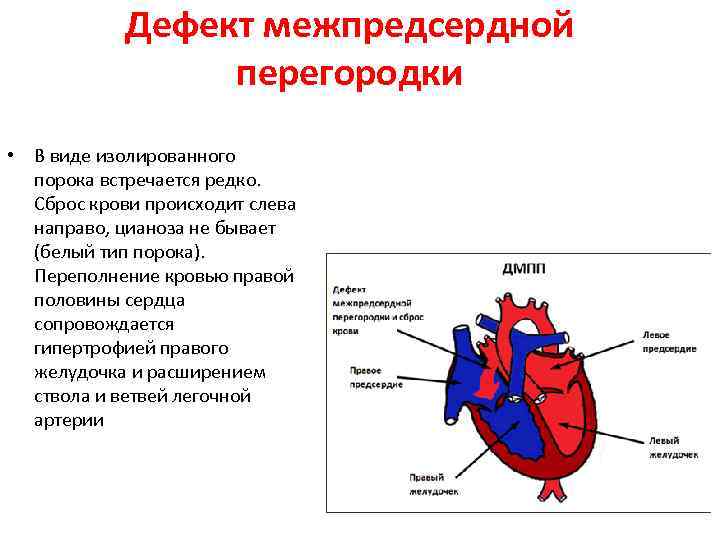
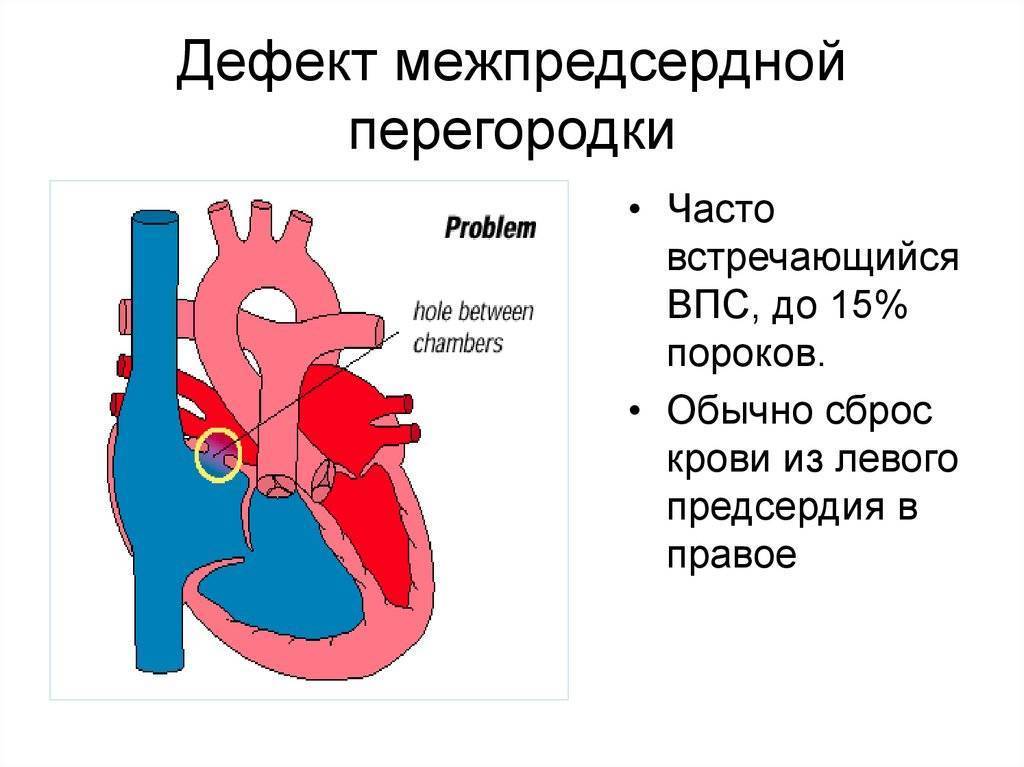
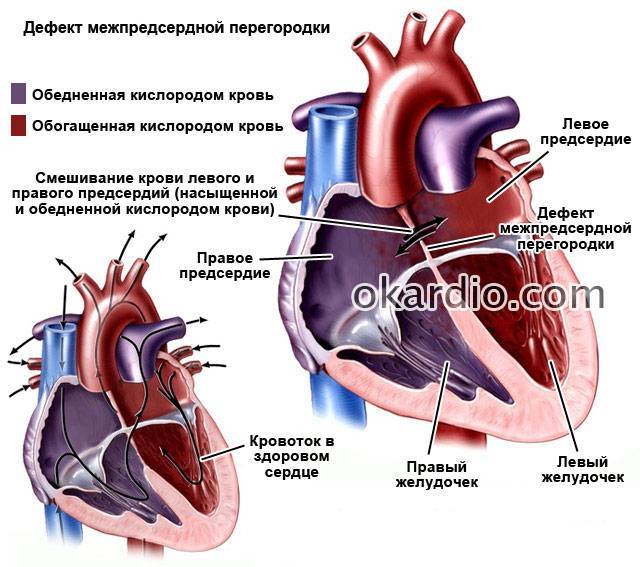
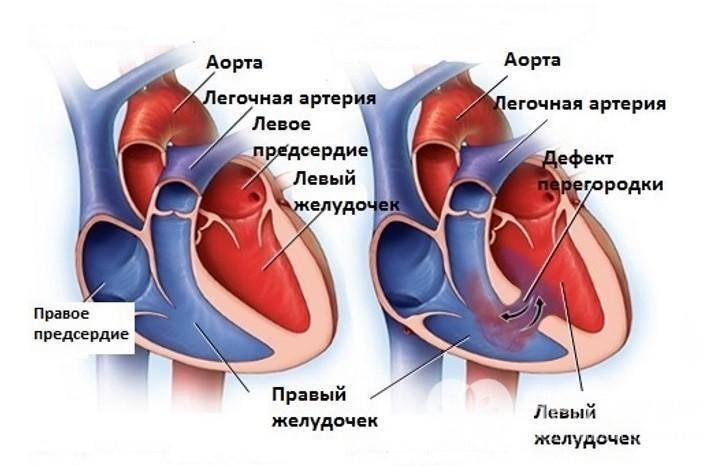
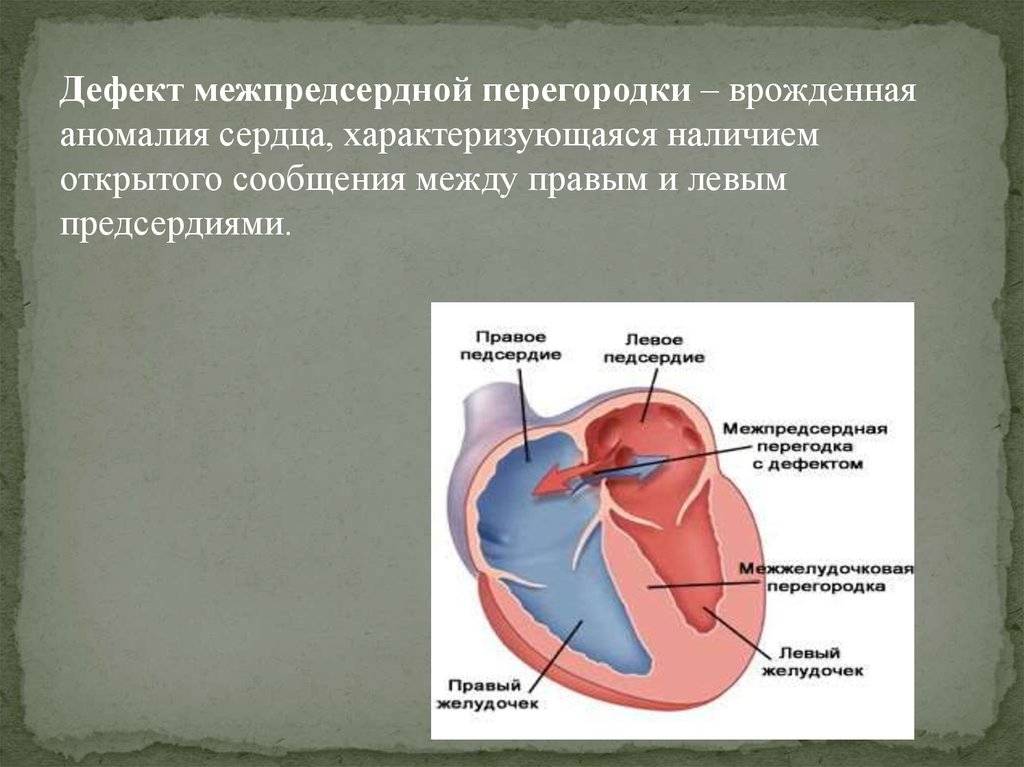
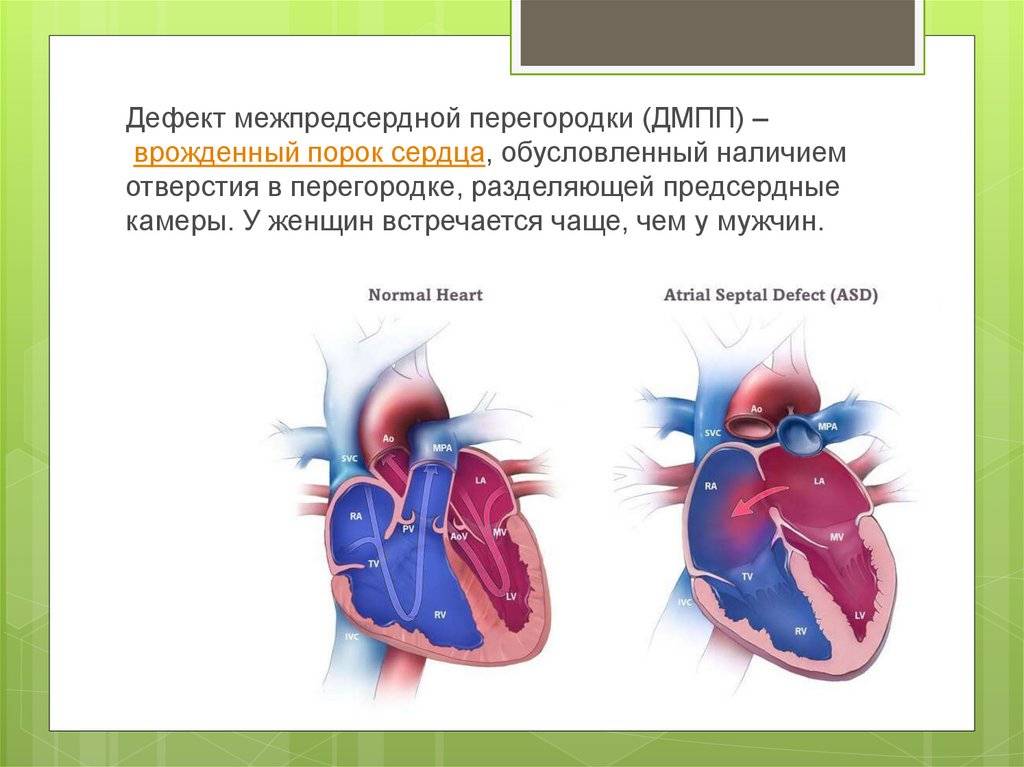
Недоразвитие межпредсердной перегородки может привести к образованию дефекта межпредсердной перегородки (ДМПП) — открытого отверстия между правым и левым предсердиями. В результате этого кровь из левого предсердия под более высоким давлением попадает в правое предсердие и далее в правый желудочек и легкие.
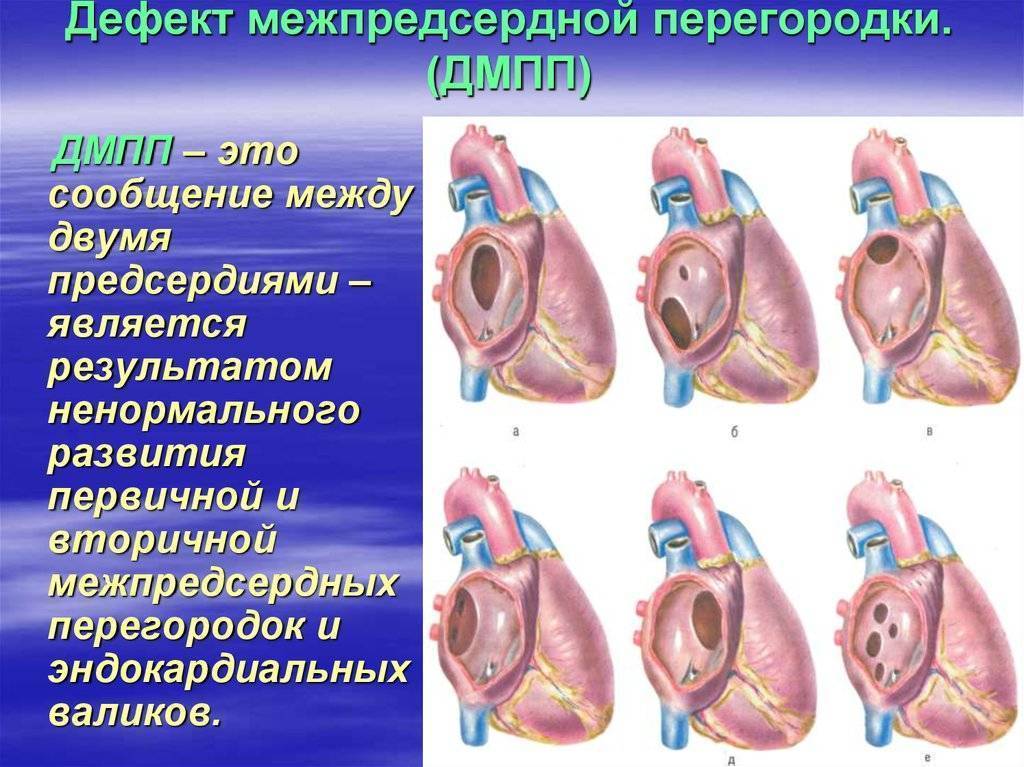
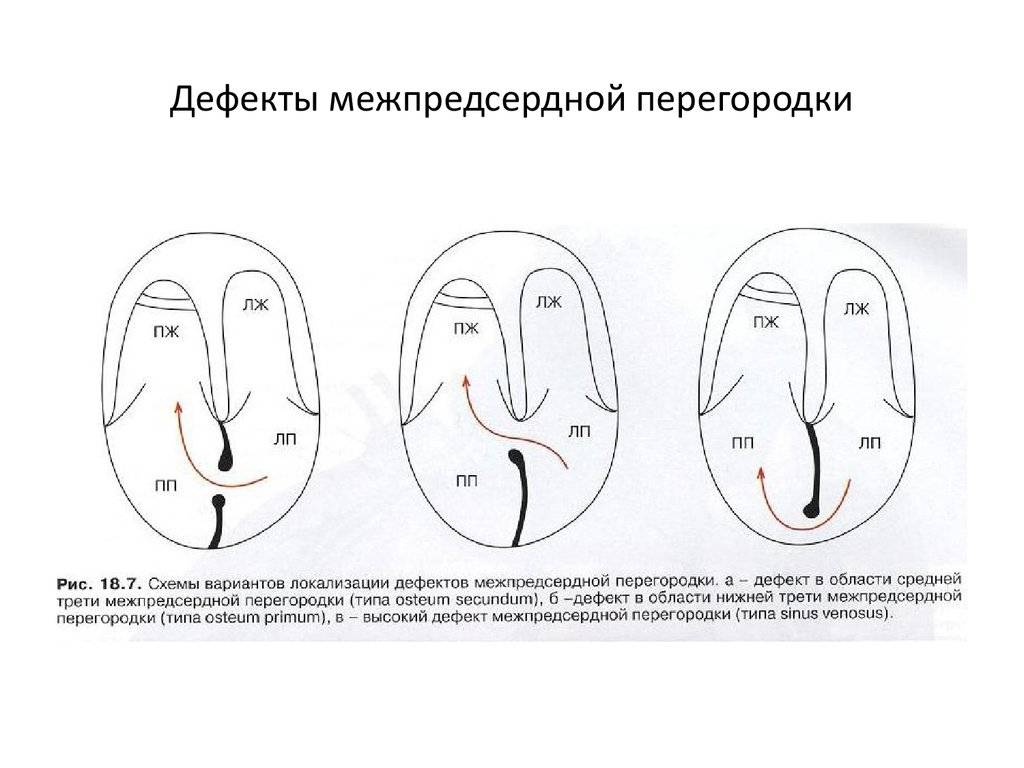
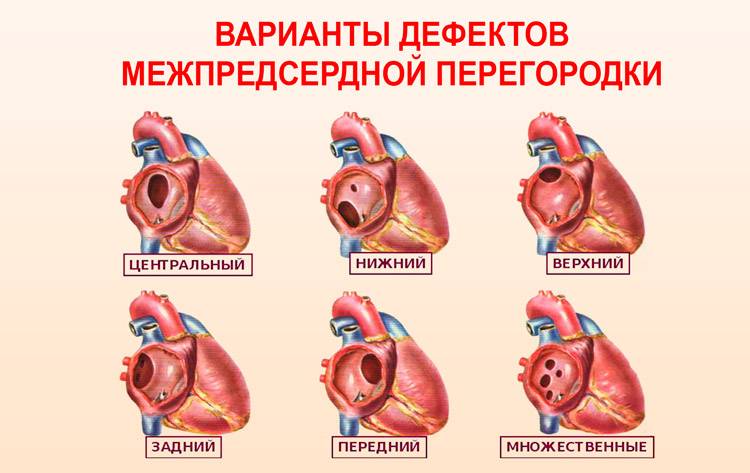
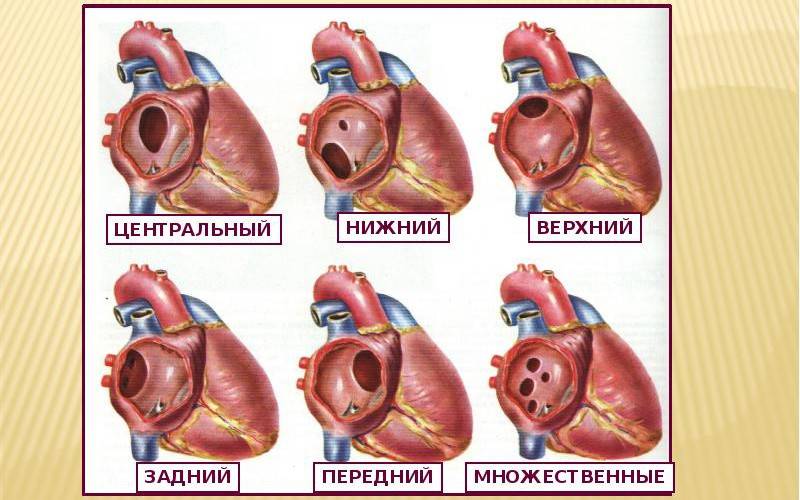
По расположению различают несколько видов дефектов межпредсердной перегородки:
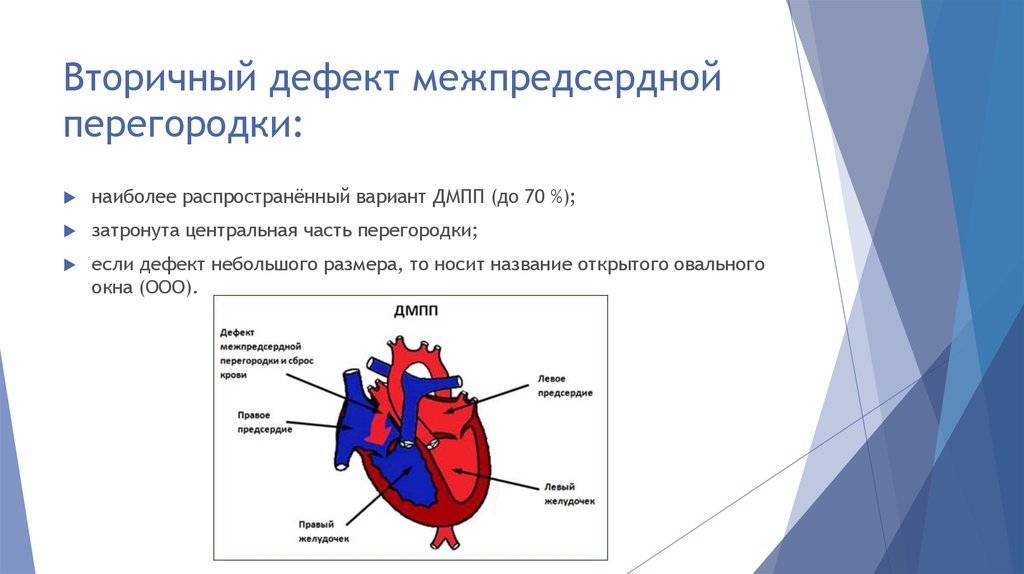
- «Вторичный (центральный) ДМПП» является самым частым и встречается в 80% случаев.
- «Первичный ДМПП» встречается в 15% случаев.
- На остальные формы ДМПП приходится менее 5%.
Диаметр ДМПП варьируется от 3 мм. до 3 см. и более.
Варианты дефектов межпредсердной перегородки
80% дефектов у новорожденных закрываются к возрасту 18 месяцев. В 20% случаев дефект сохраняется, при этом показанием к закрытию ДМПП у детей является отверстие более 8 мм., наличие сердечной недостаточности, незаращение дефекта к возрасту 4 лет.
Зачастую дефект межпредсердной пререгородки протекает бессимптомно и не ограничивает жизнь человека на протяжении многих лет, вследствие чего остаётся не диагностированным.
У 70% пациентов не выявленный в детстве ДМПП начинает проявляться в возрасте от 18 до 40 лет.
Проявлениями ДМПП со временем становятся:
- повышенная физическая утомляемость;
- появление одышки при повседневных нагрузках;
- пароксизмы учащенного неритмичного сердцебиения (суправентрикулярная тахикардия, трепетание и фибрилляция предсердий);
- повышенная частота инфекционных заболеваний дыхательной системы;
- отеки нижних конечностей.
Часто пациенты не подозревают о наличии у них ДМПП и диагноз устанавливается неожиданно при плановом выполнении ЭХО-КГ.
Целью закрытия дефекта межпредсердной пререгородки является снижение повышенной нагрузки на сердце и легкие, предотвращение сердечно-легочной недостаточности и последующих необратимых морфологических изменений тканей сердца и лёгких. Чем раньше ДМПП будет устранён, тем выше вероятность полного восстановления морфологии сердца и лёгких, и ниже вероятность развития осложнений из-за длительной их перегрузки.
Наилучшие результаты лечения проявляются при закрытии дефекта у пациентов до 25 лет. Операции проведённые у пациентов старше 40 лет улучшают качество жизни, увеличивают переносимость физических нагрузок, уменьшают проявления одышки. Однако, у данной возрастной группы в результате длительного наличия ДМПП часто развиваются нарушения ритма сердца в результате стойких изменений стенки предсердий: тахикардия, трепетание и фибрилляция предсердий. Таким пациентам после закрытия дефекта необходимо рассмотрение вопроса о выполнении радиочастотной аблации для восстановления нормального сердечного ритма.
3.Симптомы и диагностика
В раннем детском возрасте течение, как правило, бессимптомное. Однако поводом для тщательного обследования, – в т.ч. кардиологического, где обычно и выявляется аневризма, – должны стать отставание ребенка в психофизическом развитии, недостаточная масса тела, частые ОРВИ; на более поздних этапах – признаки инфантильности репродуктивной системы, постоянная бледность, утомляемость от малейших физических нагрузок, боли в области сердца, иногда заметное выпячивание грудной клетки в кардиальной зоне.
Выраженность указанного симптомокомплекса широко варьирует – от тяжелой до незначительной, существенно не влияющей на качество жизни и общее развитие. Наибольшую опасность представляет разрыв аневризмы с формированием межпредсердного дефекта (сообщения), вследствие чего нарушается нормальная, естественная для миокарда гемодинамика. Однако и такое развитие событий выше не случайно названо непредсказуемым: в одних случаях приобретенный порок позволяет в течение десятилетий вести вполне обычный образ жизни, в других создает угрозу инсульта или т.н. внезапной сердечной смерти. После 40 лет пациента с дефектом МПП, образовавшимся вследствие прорыва аневризмы, зачастую приходится инвалидизировать из-за нарастающих гемодинамических нарушений и рисков.
В диагностике, помимо анамнеза, результатов клинического осмотра и наблюдения, наибольшее значение приобретает ультразвуковая эхокардиография (ЭхоКГ), которая практически не имеет противопоказаний, допускает повторные исследования в динамике и позволяет наглядно визуализировать аневризму с точной оценкой ее характеристик. В качестве уточняющей диагностики, – обычно для выявления и исследования сопутствующих аномалий и пороков, – дополнительно могут быть назначены чреспищеводное УЗИ, КТ, катетеризация сердца.
Реабилитация после лечения дефекта межпредсердной перегородки у детей
После оперативного вмешательства пациент проведет несколько дней под присмотром медперсонала. В этот период медики тщательно следят за гемодинамическими показателями, водно-электролитным и кислотно-щелочным балансом, работой всех органов и систем. Объем терапии определяется индивидуально.
Лучшие реабилитологи «Хадассы» составят индивидуальный план восстановления. При необходимости больного переведут в специализированное отделение.
|
После возвращения домой реабилитацией будут заниматься родители — им дадут рекомендации и обучат правильному уходу за ребенком. |
После выписки ребенок наблюдается по месту жительства. В течение полугода нельзя посещать детский сад. Школьников переводят на индивидуальное обучение
Очень важно придерживаться принципов правильного питания, следить за интенсивностью физических нагрузок
Причины и разновидности
Патологическое отверстие формируется еще в ходе эмбрионального развития – поэтому заболевание и называется врожденный порок сердца.
Существует ряд факторов, которые могут спровоцировать рождение ребенка с пороком сердца:
- Инфекционные болезни. Особенно опасны для развития ребенка такие болезни, как краснуха, корь и ветрянка. К счастью, сейчас для женщин, которые не смогли переболеть до родов, существует вакцина.
- Курение, употребление алкоголя, прием наркотиков.
- Некоторые лекарственные препараты, например, литийсодержащие, могут спровоцировать развитие порока сердца.
- Наличие генетической предрасположенности: по статистике, один случай из двадцати объясняется наследственностью.
Если дефект небольшой, то симптомы выражены не так явно, как при крупном. Большие множественные отверстия считаются самой тяжелой формой заболевания. Если дефект состоит из мышц, то есть вероятность, что он самостоятельно затянется в течение первого года жизни – это происходит из-за общего развития мышечной стенки сердца. В остальных случаях ожидать самовыздоровления не стоит – поэтому операцию проводят как можно раньше, если это позволяет состояние ребенка.
Показания
- наличие отверстия в перегородке между желудочками сердца;
- патологический заброс крови в правый желудочек;
- повышенная нагрузка на правый желудочек;
- выраженная симптоматика.
Противопоказания
- особое расположение отверстия – близко к клапанам сердца;
- наличие некоторых других заболеваний сердца;
- непоправимые изменения в легких;
- нарушение свертываемости крови;
- острые инфекционные и воспалительные заболевания.