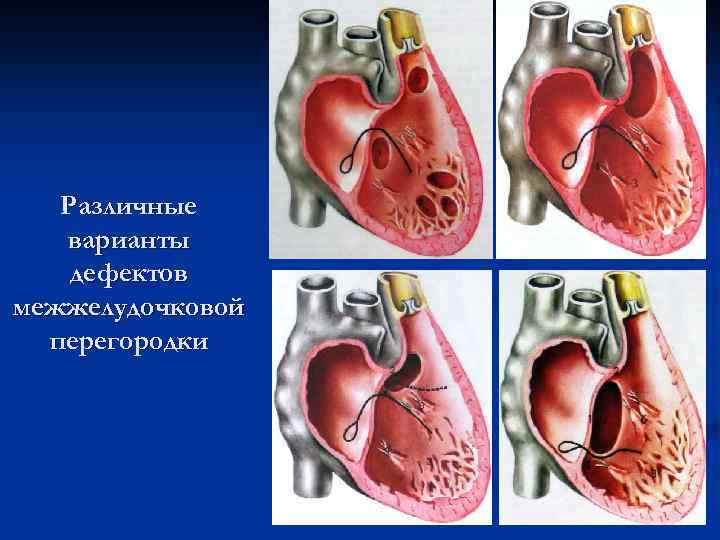
SQLITE NOT INSTALLED
Правое предсердие
Функциональная анатомия правого предсердия
Правое предсердие имеет цилиндрическую форму; у новорожденных объем
полости составляет 6,5-10 см3, к концу 1 года жизни — 11-18
см3, в 7-9 лет — 22-36 см3, в 18-25 лет — 100-150
см3.
Правое предсердие изучают в двухмерном режиме из проекции 4-х камер
с верхушки или субксифоидально. При субксифоидальном доступе можно
визуализировать место впадения нижней полой вены, а также ее заслонку
(складка эндокарда высотой 5-10 мм) и межвенозный бугорок (на границе
устьев верхней и нижней полой вены). На латеральной стенке правого
предсердия в ряде случаев удается визуализировать мышечный валик (пограничный
гребень ушка правого предсердия). При дилатации ушка могут визуализироваться
гребенчатые мышцы в виде трабекулярных образований, обычно соединяющихся
с устьем полых вен.
Размеры правого предсердия зависят от возраста: у новорожденных и
детей до года переднезадний размер колеблется от 1,1 до 2,1 см, у
детей 1-6 лет — 1,1-2,5 см, у детей 7-12 лет — 1,3-2,5 см, 13-17
лет — 1,4-2,5 см. Ширина предсердия у новорожденных и детей до 1
года от 1,2 до 1,9 см, у детей 1-6 лет — 1,2-2,3 см, у детей 7-12
лет — 1,3-2,3 см, у 13-17-летних — 1,4-2,3 см.
Двухмерная эхокардиография правого предсердия
Правое предсердие визуализируют в нескольких продольных и поперечных
сечениях. Из субкостального доступа определяют место впадения нижней
полой вены в полость камеры (situs solitus). В проекции 4-х камер
из апикального или субкостального доступа устанавливают форму камеры,
наличие в ней дополнительных образований, взаимосвязь с желудочковой
камерой.
Дилатация правого предсердия
- Идиопатическая аневризма правого предсердия.
- Аномальный дренаж легочных вен.
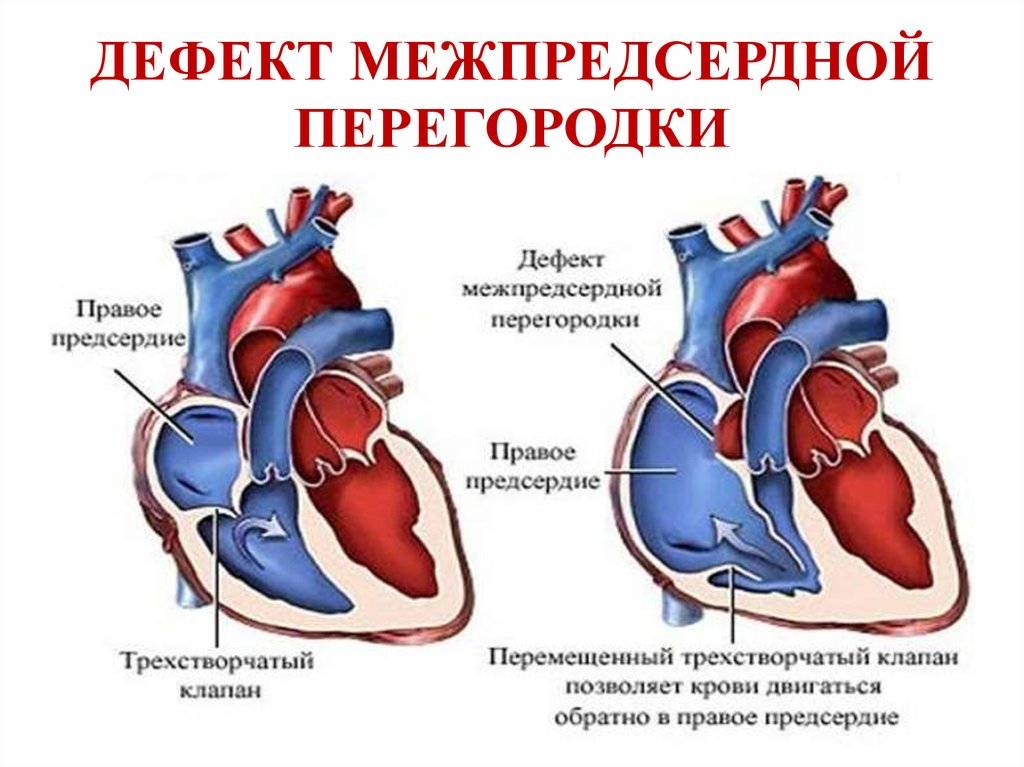
- Дефект межпредсердной перегородки.
- Открытый атриовентрикулярный канал.
- Аномалия Эбштейна.
- Стеноз трикуспидального клапана.
- Недостаточность трикуспидального клапана.
- Опухоль правого предсердия.
- Рестриктивная кардиомиопатия.
- Аритмогенная дисплазия правого желудочка.
- Частичное врожденное отсутствие перикарда.
- Легочное сердце.
- Застойная сердечная недостаточность.
- Констриктивный перикардит.
- Прорыв аневризмы синуса Вальсальвы в правое предсердие.
- Портальная гипертензия.
Уменьшение полости правого предсердия
- Сдавление при опухолях средостения.
- Синдром гипоплазии правого желудочка.
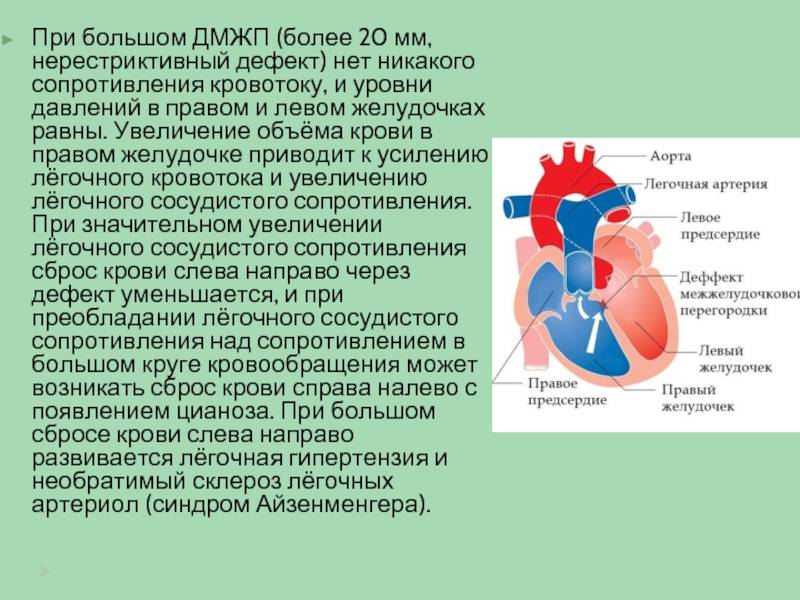
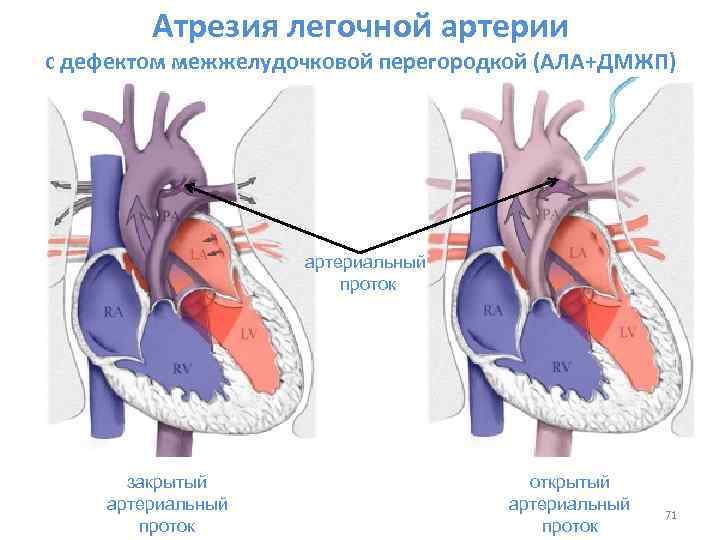
- Большой лево-правый шунт на уровне желудочков (ДМЖП)
или магистральных сосудов (ОАП).
Дополнительные эхосигналы в полости правого предсердия:
- Опухоли правого предсердия (чаще миксомы).
- Заслонка венечного синуса.
- Заслонка нижней полой вены (Евстахиев клапан).
- Заслонка овального отверстия.
- Гребенчатые мышцы ушка правого предсердия.
- Тромб в правом предсердии.
- Пролапс трикуспидального клапана.
- Пролапс клапана нижней полой вены.
- Аневризма межпредсердной перегородки.
ДМЖП у плода: что делать, и когда нужна операция?
На сегодняшний момент ни одно лекарство или процедура не способны вызвать произвольное закрытие отверстия перегородки сердца. Дефект возможно лишь ушить или закрыть трансплантатом.
В ряде случаев происходит самостоятельное исчезновение небольших дефектов, что избавляет от необходимости вмешательства. Крошечные отверстия перегородки без существенных нарушений кровотока позволяют применить выжидательную тактику до 6 — 36 месяцев.
Тем не менее, большие дефекты являются абсолютным показанием к хирургии. В зависимости от размеров дефекта и общего состояния новорожденного операция ДМЖП у ребенка может выполняться в первые месяцы жизни или откладываться до определенного срока.
Выбор метода вмешательства и времени его выполнения зависит от общего состояния ребенка, расположения и размера дефекта, давления в желудочках и предсердиях сердца, наличия противопоказаний.
При ДМЖП операция может проводиться по классической, «открытой» методике или с применением малотравматичного эндоваскулярного оборудования.
Крупные дефекты ушиваются после рассечения грудной клетки и камеры сердца. Операция проводится при помощи аппарата искусственного кровообращения большой бригадой опытных хирургов. Риск осложнений сводится до статистического минимума благодаря современному оборудованию и высочайшему мастерству оперирующих кардиохирургов.
В случае обнаружения небольших отверстий в перегородке предпочтение может отдаваться эндоваскулярной хирургии. Достоинствами методики являются отсутствие разрезов и меньший риск нежелательных последствий. Устранение дефекта при этом производится специальным устройством, которое вводится в сердечно-сосудистую систему через небольшой прокол бедренной артерии.
В нашем центре есть все необходимое для лечения детей с указанной патологией.
На первичной консультации доктор подробно расскажет о прогнозах и степени ДМЖП у плода, и что делать с имеющейся проблемой дальше.
При необходимости операции она будет выполнена в наилучших для этого условиях — современной оснащенной операционной коллективом из самых опытных кардиохирургов.
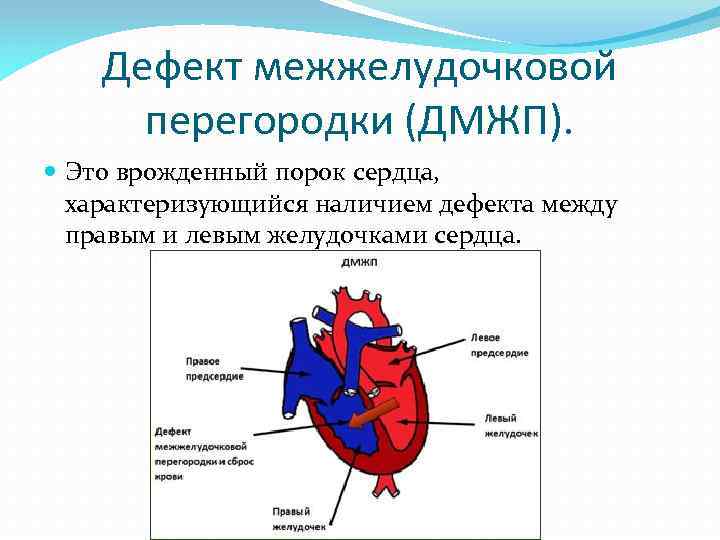
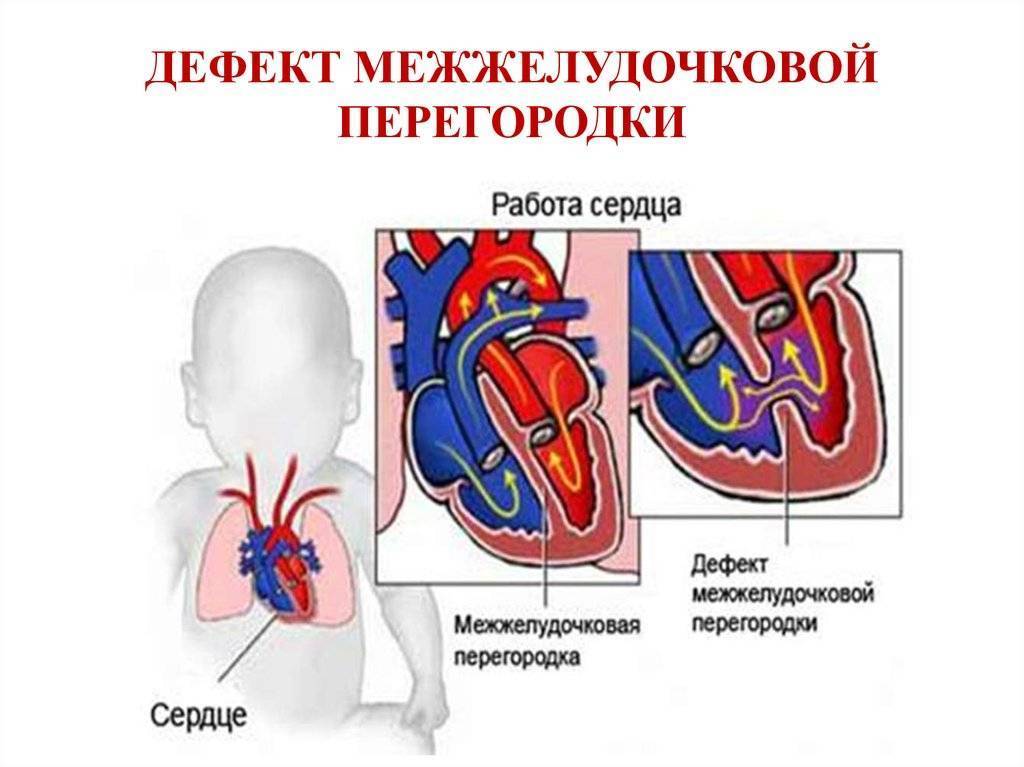
Что такое ДМЖП сердца у детей?
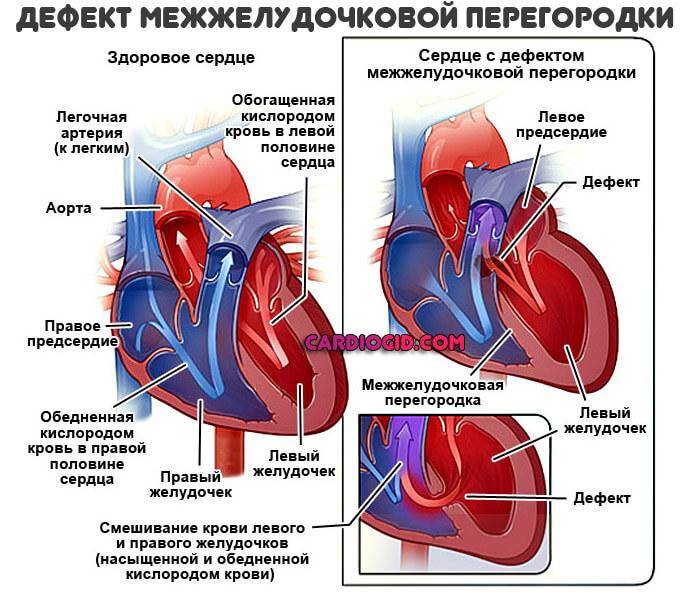
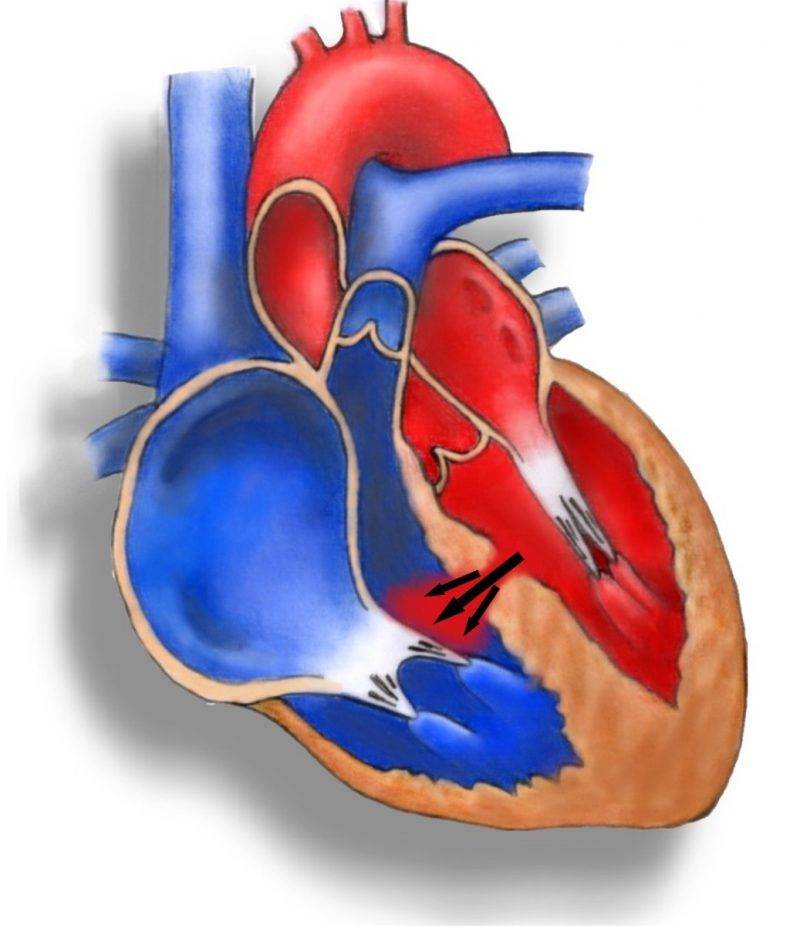
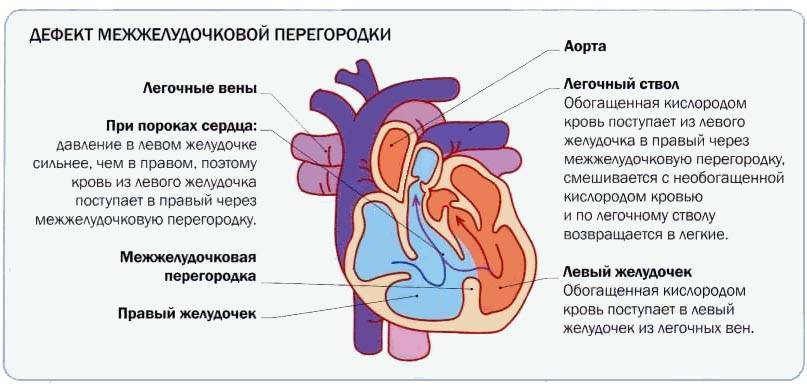
Нормальная работа сердца основывается на том, что венозная кровь от тела, попадающая в правое предсердие и желудочек, поступает сначала в легкие, где насыщается кислородом — только после этого, завершив малый круг кровообращения, она попадает в левую половину сердца, откуда через аорту распространяется по всему телу, совершая большой круг кровообращения. При этом венозная кровь из правых отделов сердца не смешивается с насыщенной кислородом кровью левых отделов.
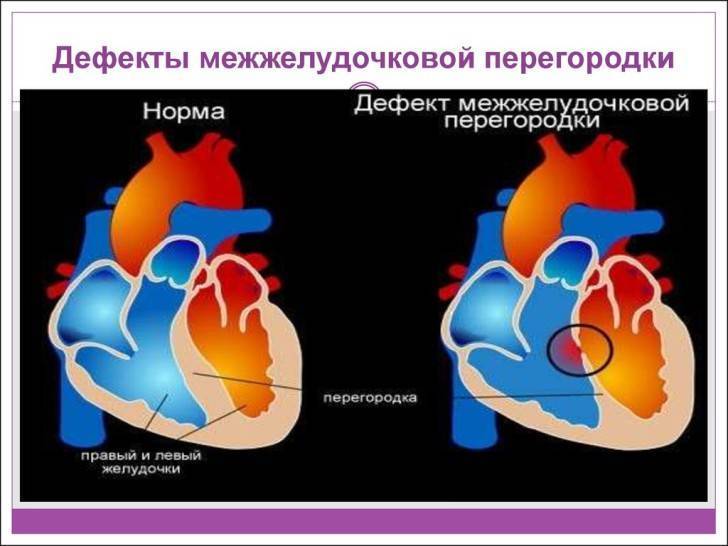
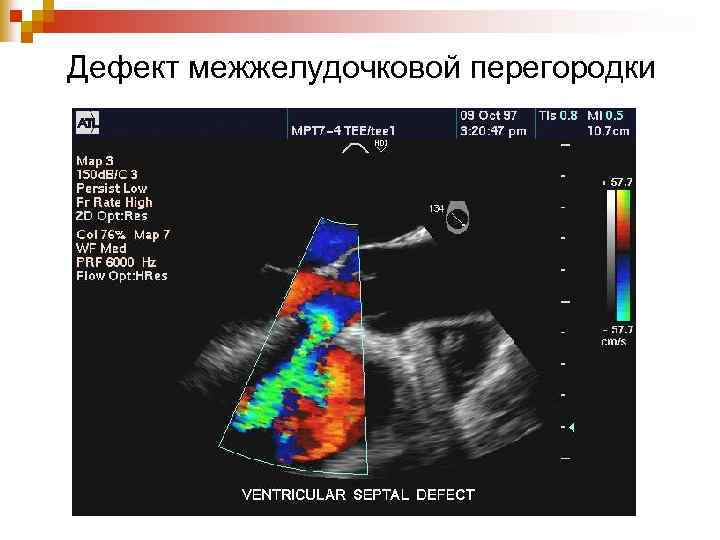
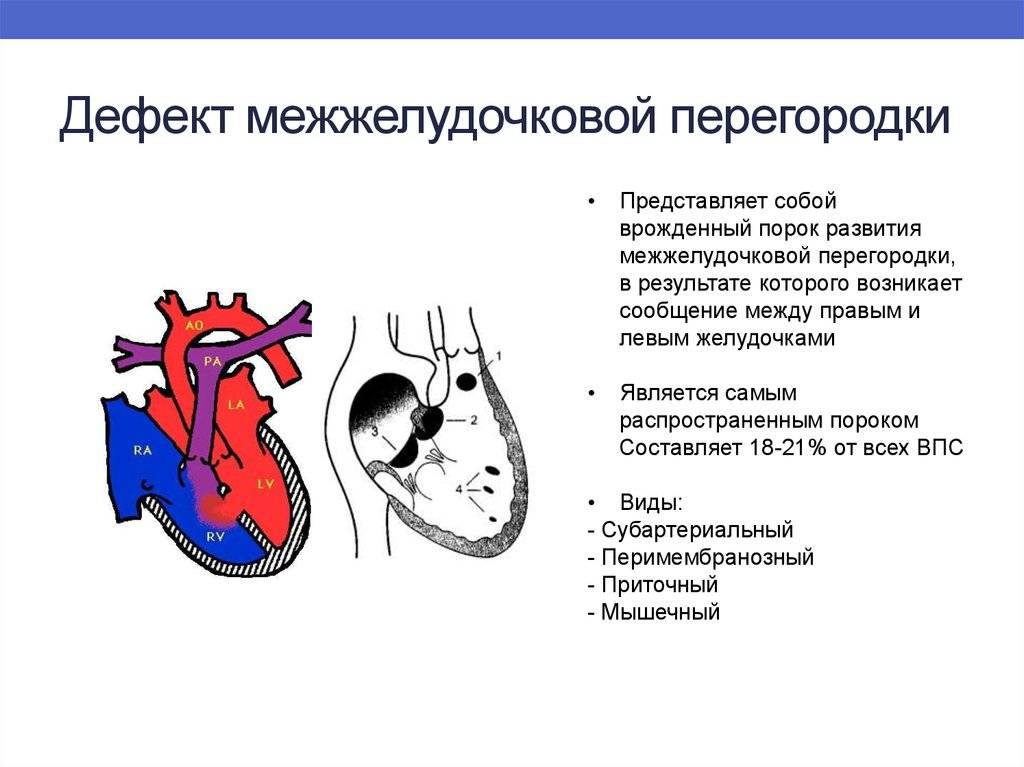
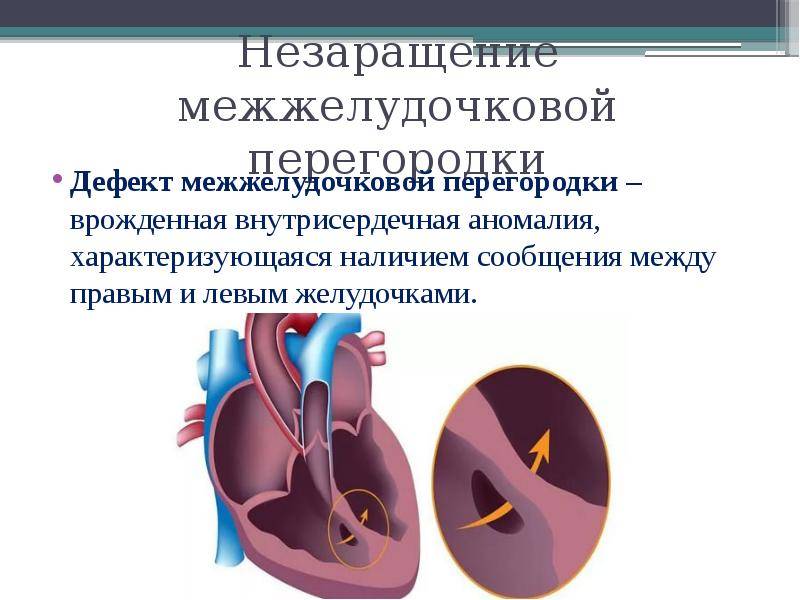
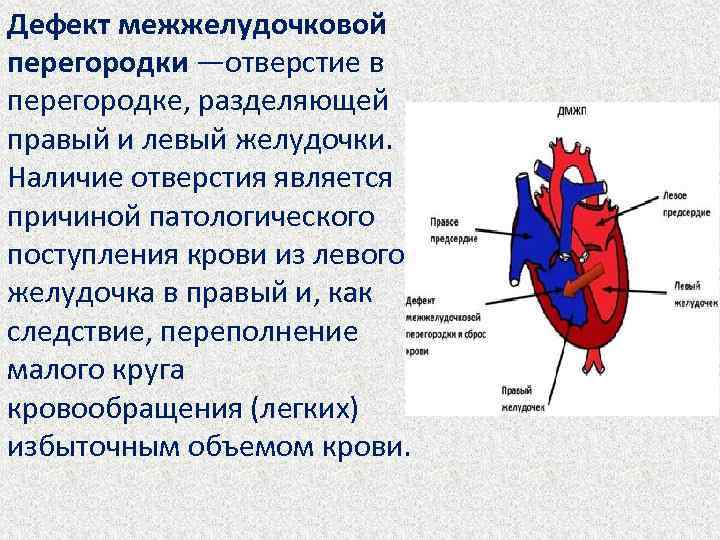
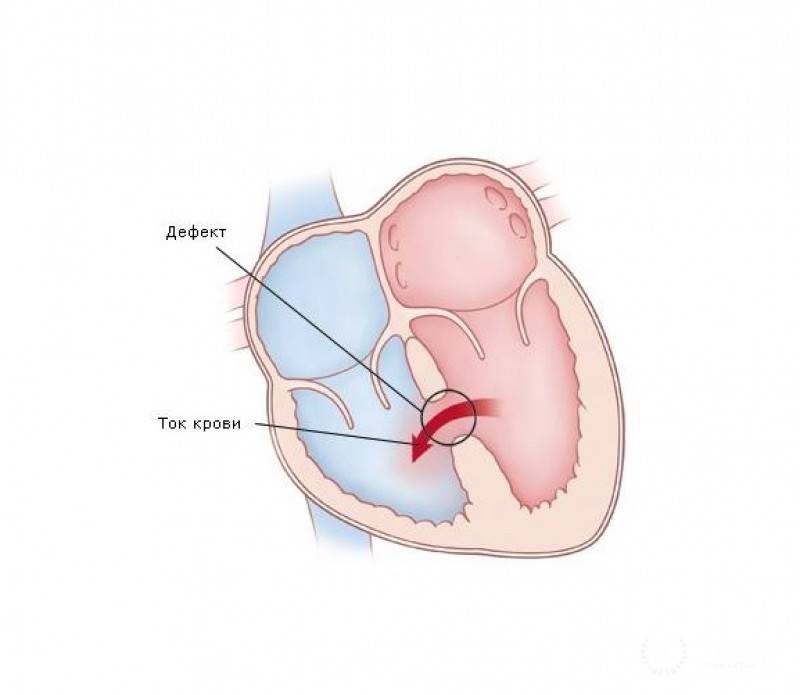
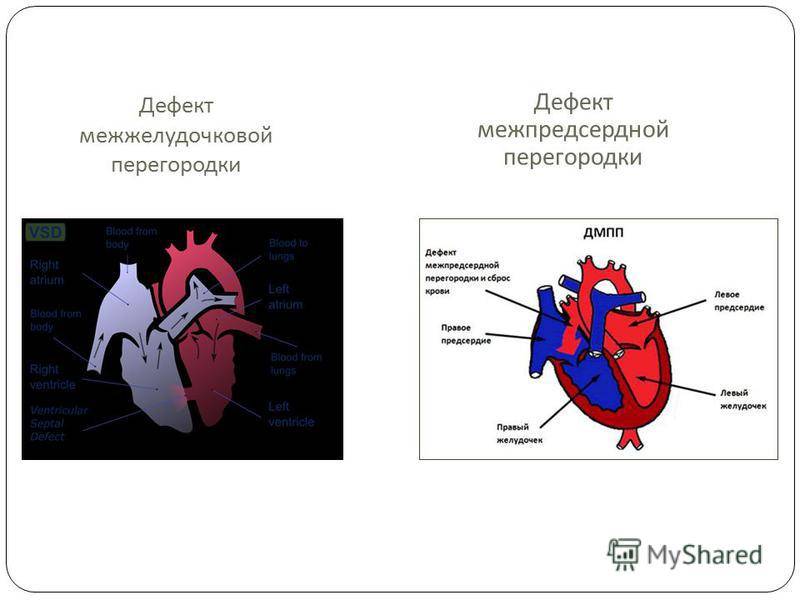
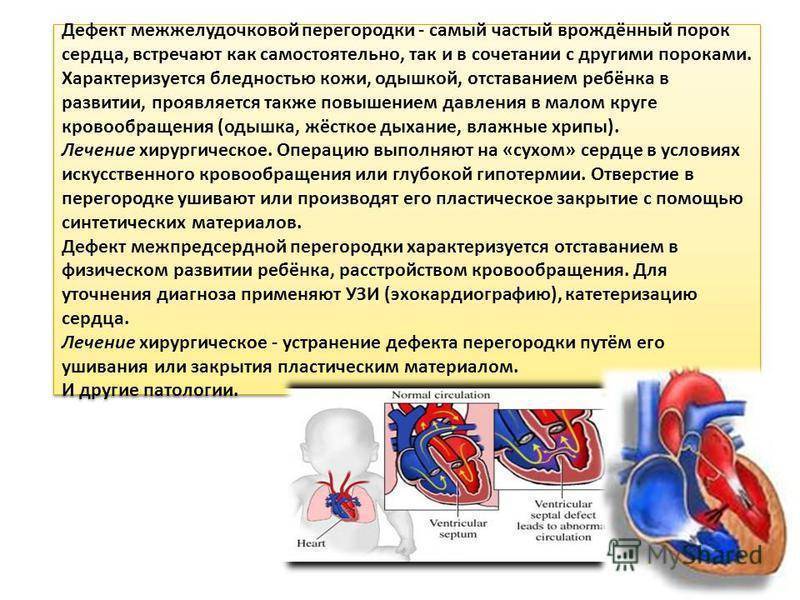
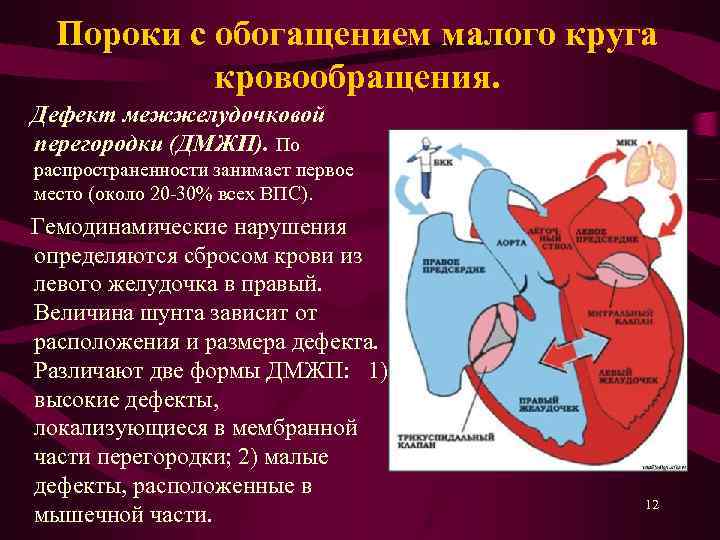
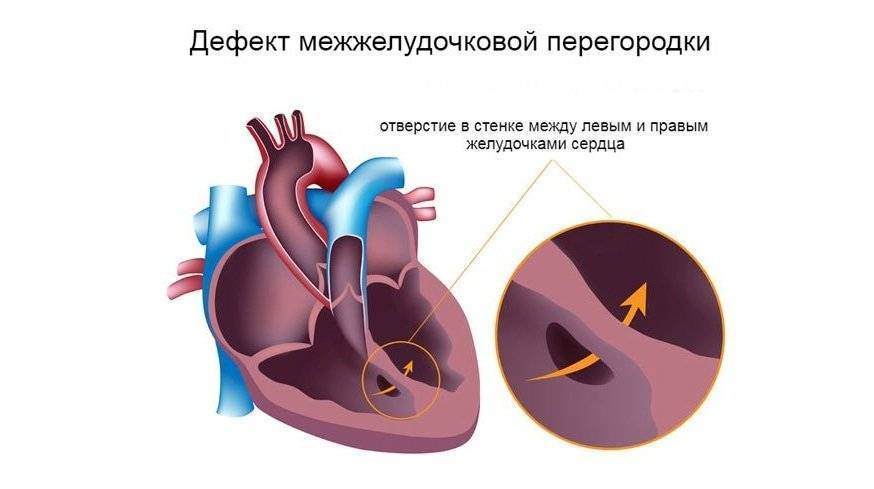
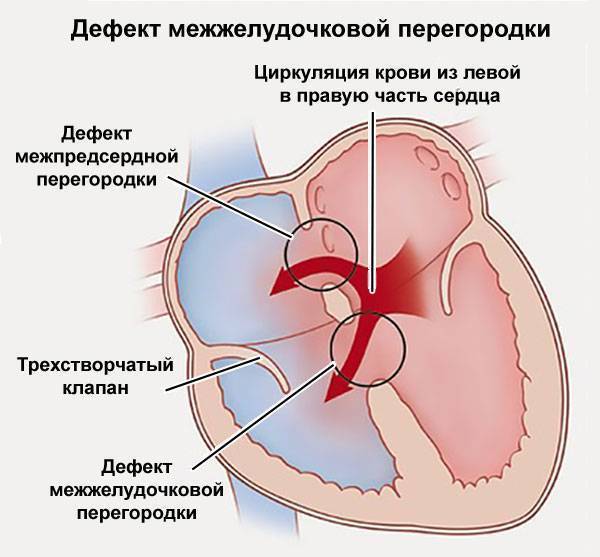
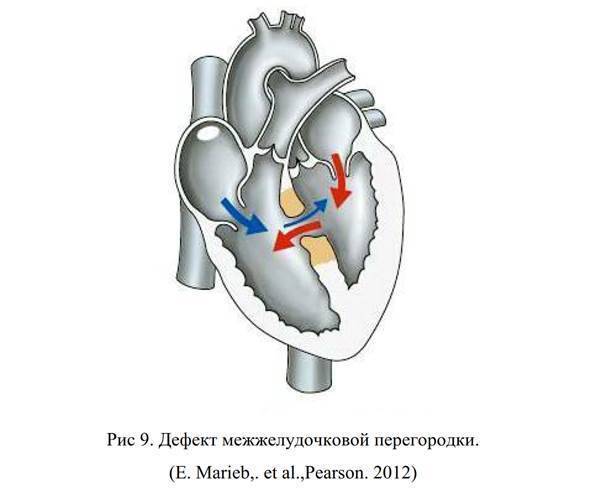
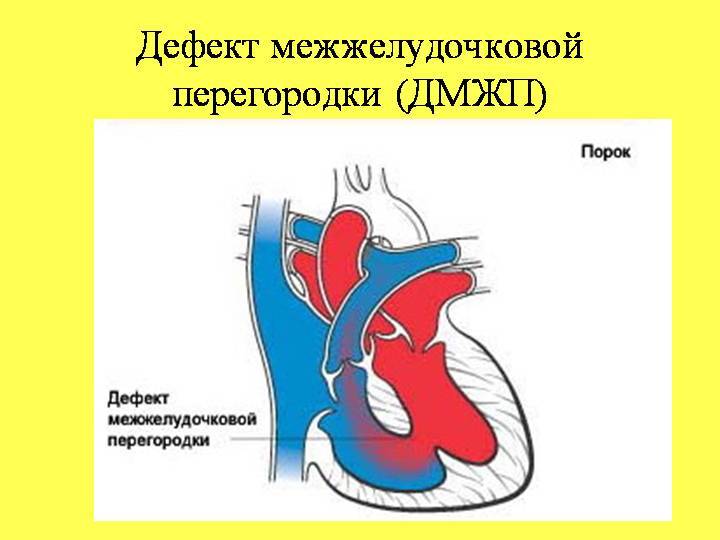
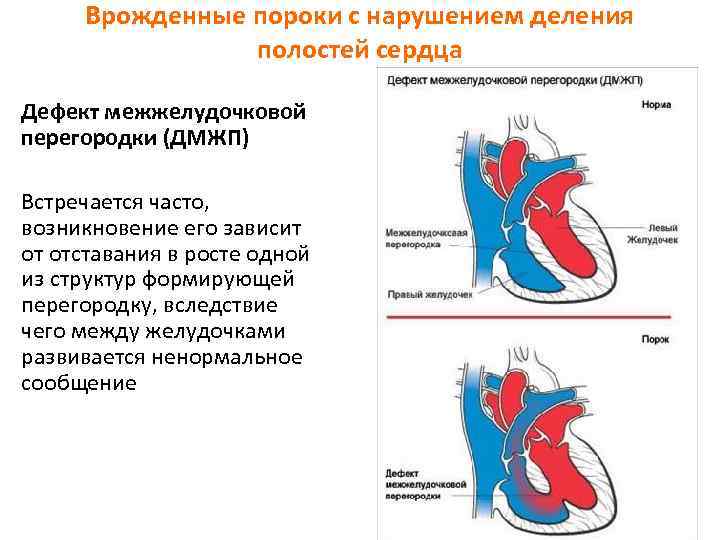
Существуют различные дефекты перегородки, которая обеспечивает это разделение венозной и артериальной крови в сердце. Такой врожденный порок может возникнуть как между предсердиями, так и между желудочками. Дефект межжелудочковой перегородки сердца (ДМЖП) составляет от 10 до 30 % всех видов врожденных пороков сердца у новорожденных и занимает второе место по частоте встречаемости у детей старше 3 лет. Для данного порока сердца характерно наличие отверстия в межжелудочковой перегородке (она разделяет желудочки, «перекачивающие» кровь в большом и малом кругу кровообращения). Вследствие такого дефекта дополнительный «несанкционированный» объем крови может поступать из левого в правый желудочек, что влечет за собой избыточное наполнение малого круга, который проходит через легкие. Как результат таких патологических изменений – заболевания органов дыхания, появление выраженной одышки, частое воспаление легких, простуды и даже отставание в умственном и физическом развитии. Особенно такие проблемы характерны для пациентов с диаметром дефекта от 10 до 15 мм – им показано неотложное оперативное вмешательство. При небольших размерах отверстия в перегородке (около 2-5 мм) отклонения в состоянии здоровья у детей могут не обнаруживаться.
Виды патологии
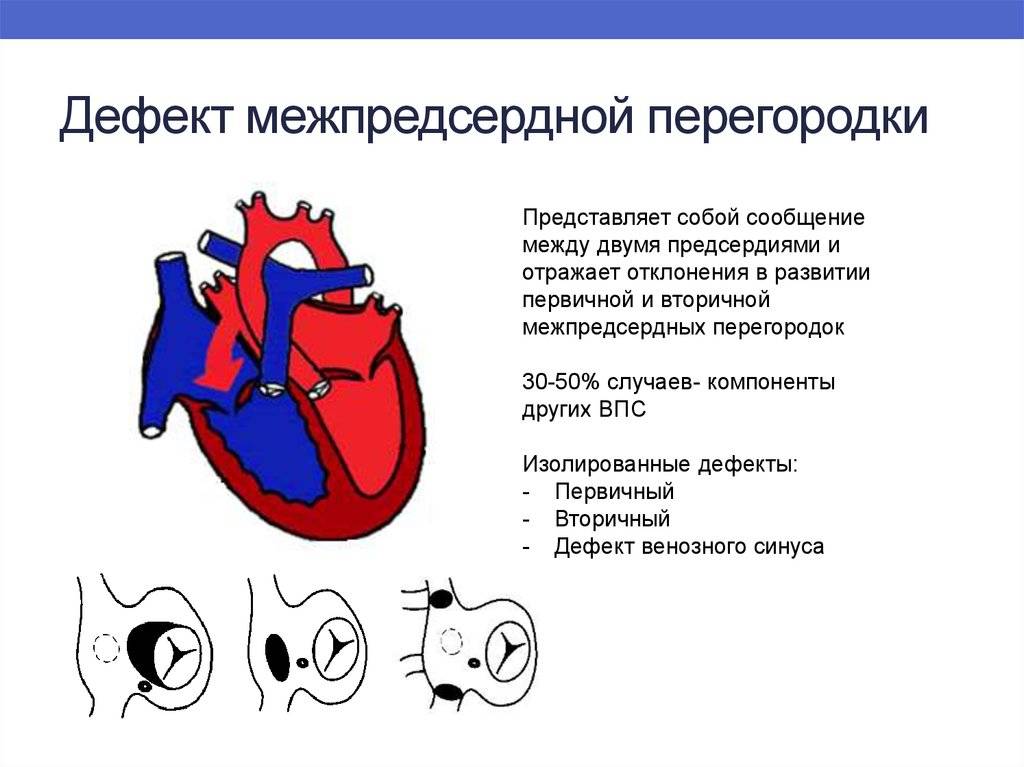
Существует разделение патологии по количественным и качественным показателям: числу, локализации и размерам перегородочных отверстий. Но самой распространенной классификацией ДМПП признано деление по характеру недоразвитости ткани:
- Первичная аномалия. Сообщение между предсердиями сохраняется на фоне недоразвития или расщепления створок, атриовентрикулярного канала. Располагается чаще в нижнем секторе, обладает большим диаметром до 5 см.
- Вторичная аномалия. Располагается чаще по центру или в венозных устьях, отличается маленькими размерами до 2 см.
- Комбинированное нарушение. Сочетаются между собой и с другими тяжелыми сердечными пороками.
- Трехкамерное сердце. Образуется, когда перегородочная пленка совсем отсутствует или максимально недоразвита. В этом случае предсердия образуют общую полость.
У новорожденных нередко диагностируют так называемое «открытое овальное окно», которое также считается патологическим сообщением между предсердиями. Связывается этот дефект с замедленным развитием сердечной ткани, но он не является истинным ДМПП, так как в большинстве случаев регрессирует самостоятельно. Ткани догоняют в развитии, просвет затягивается в течение первого месяца жизни ребенка. Если этого не происходит, требуется медицинское вмешательство.
Левое предсердие
Левое предсердие имеет цилиндрическую форму, его объем у новорожденных
составляет 4-5 см3, к концу года достигает 10-14 см3,
к 7-9 годам 24-32 см3, 18-25 годам — 90-135 см3.
Размеры левого предсердия зависят от возраста. У детей до 1 года жизни
переднезадний размер составляет 0,8-1,7 см, у детей до 6 лет — 0,8-2,2
см, до 12 лет — 1,0-2,2 см, до 17 лет — 1,1-2,2 см. Ширина левого
предсердия у детей до 1 года жизни составляет 1-1,17 см, у детей до
6 лет — 1,1-2,1 см, 7-12 лет — 1,3-2,1 см, 13-17 лет — 1,5-2,3
см.
Одномерная эхокардиография левого предсердия
В одномерном режиме проводится визуализация передне-заднего размера
левого предсердия в IV стандартной позиции. В этой позиции ультразвуковой
луч пересекает область левого предсердия, прилежащую к атриовентрикулярному
отверстию.
Семиотика левого предсердия
Увеличение диаметра левого предсердия
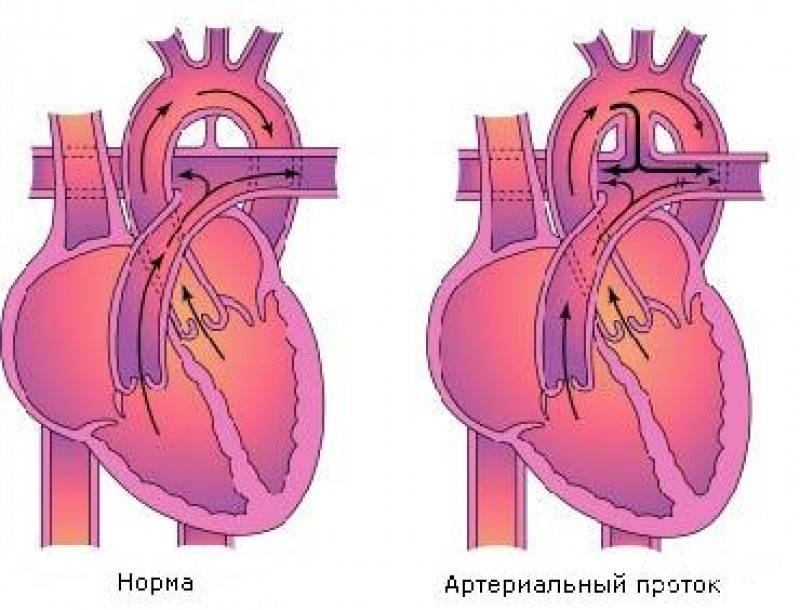
- Открытый артериальный проток.
- Дефект межжелудочковой перегородки.
- Недостаточность митрального клапана.
- Стеноз митрального клапана.
- Надклапанное митральное кольцо.
- Рестриктивная кардиомиопатия.
- Гипертрофическая кардиомиопатия.
Уменьшение диаметра левого предсердия
- Синдром гипоплазии левого желудочка.
- Тотальный аномальный дренаж легочных вен.
- Компрессия левого предсердия экстракардиальной опухолью
средостения. - Большой дефект межпредсердной перегородки.
- Миксома левого предсердия.
- Тетрада Фалло.
- Аномалия Эбштейна.
- Двойное отхождение магистральных сосудов от правого
желудочка.
Увеличение экскурсии задней стенки левого предсердия
Связано с увеличением трансмитрального кровотока при различных физиологических
и патологических состояниях.
- Недостаточность митрального клапана.
- Начальные стадии гипертонической болезни.
- Гиперкинетический кардиальный синдром.
- Спортивное сердце.
Дополнительные эхосигналы в полости левого предсердия
- Надклапанное митральное кольцо.
- Тромб левого предсердия.
- Отрыв сухожильных нитей от передней митральной створки.
- Отрыв сухожильных нитей от задней митральной створки.
- Миксома левого предсердия.
- «Болтающийся» митральный клапан (floppy
mitral valve). - Подвижные бактериальные вегетации митрального клапана.
Левое предсердие изучают в нескольких сечениях: парастернальное сечение
длинной оси левого желудочка, в прекции 4-х камер с верхушки и из
эпигастрального доступа
Обращают внимание на форму камеры (в норме
она должна быть овальной), наличие внутриполостных образований, взаимосвязь
с левым желудочком
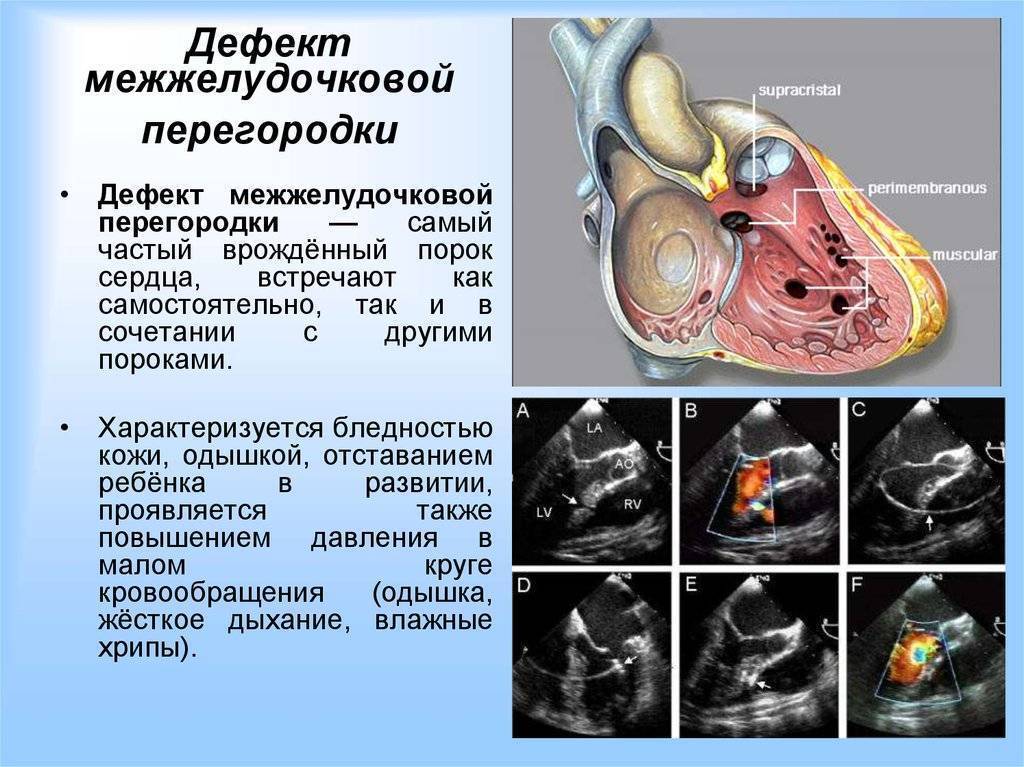
Что необходимо знать о дефекте межжелудочковой перегородки
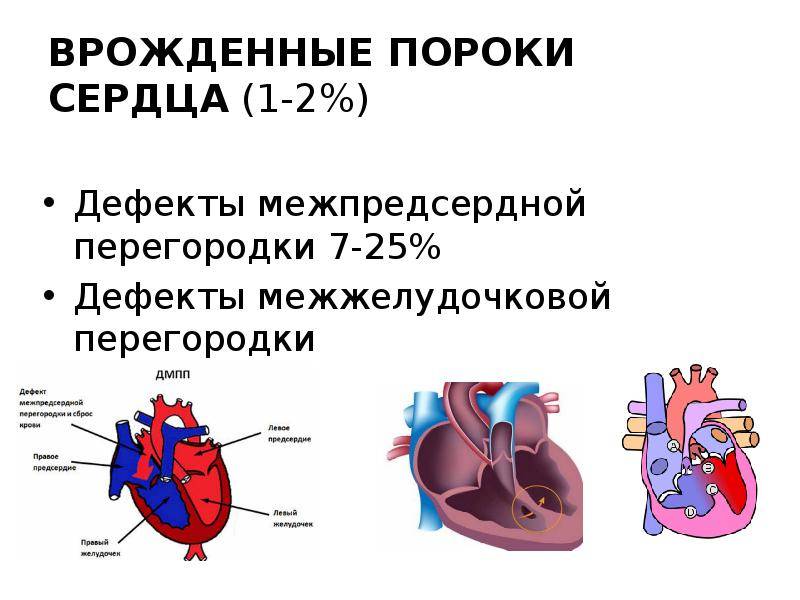
- Наиболее распространенный врожденный порок сердца — дефект межжелудочковой перегородки (25-30%).
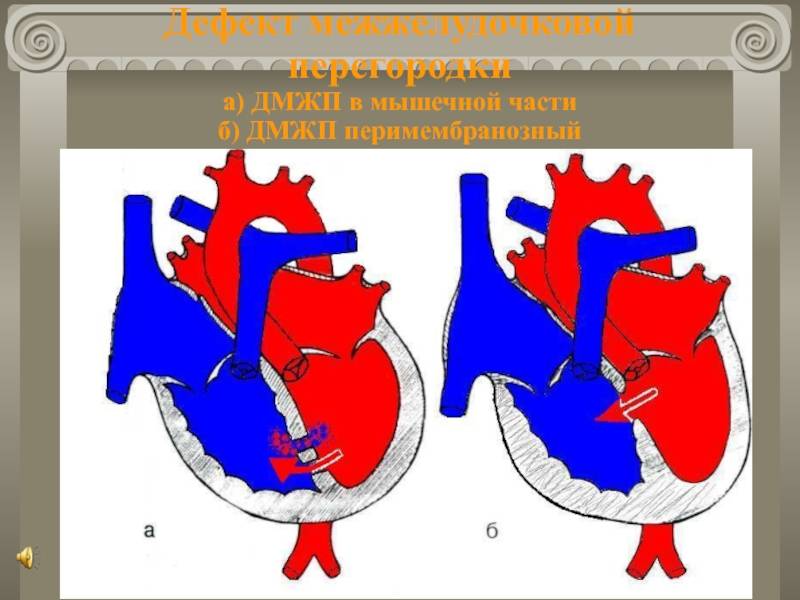
- Перимембранозный дефект межжелудочковой перегородки у плода (70-80% случаев): дефект в мембранной части перегородки
- Дефект границы перегородочной створки трикуспидального клапана и/или клапана аорты.
- Мышечный дефект: одиночный или множественный (дефект по типу «швейцарского сыра»)
- Ограничена только мышечной частью перегородки (расположение в центральной или верхушечной части перегородки).
- «Двойной» дефект межжелудочковой перегородки, возникающий в перегородке канала между аортой и легочным стволом.
- Атриовентрикулярный канал или частично открытый, возникающий в перегородке на входе в правый желудочек.
- Перегрузка объемом правого желудочка и левого предсердия
- У 50% пациентов дефект межжелудочковой перегородки возникает в сочетании с другими пороками сердца.
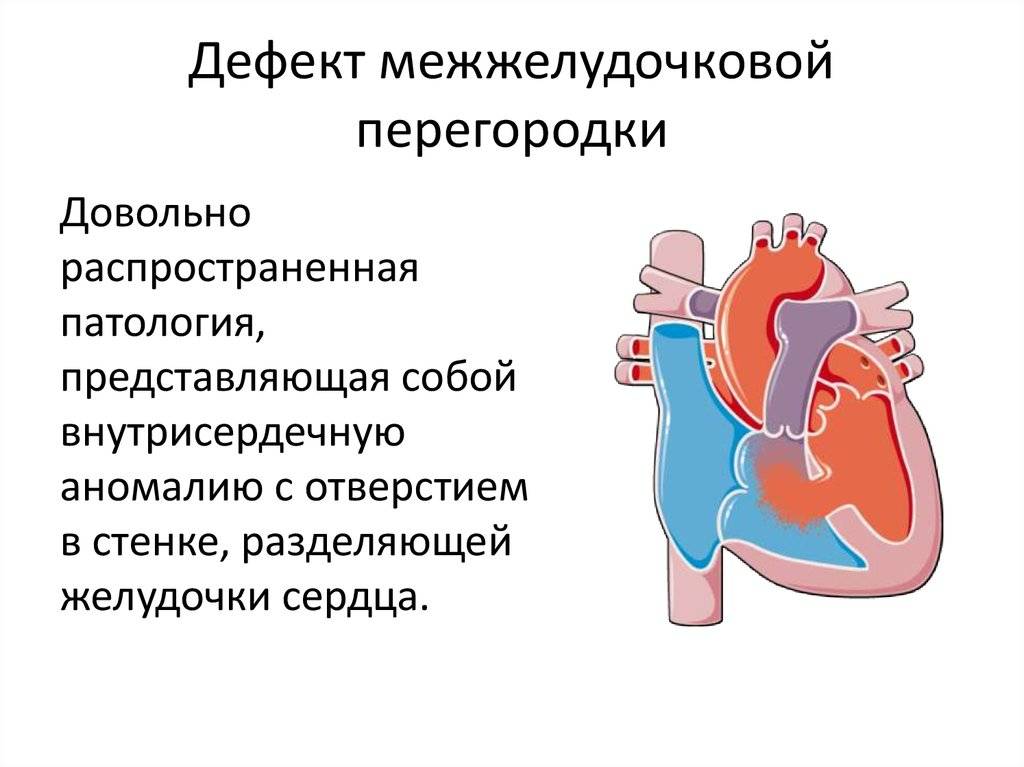
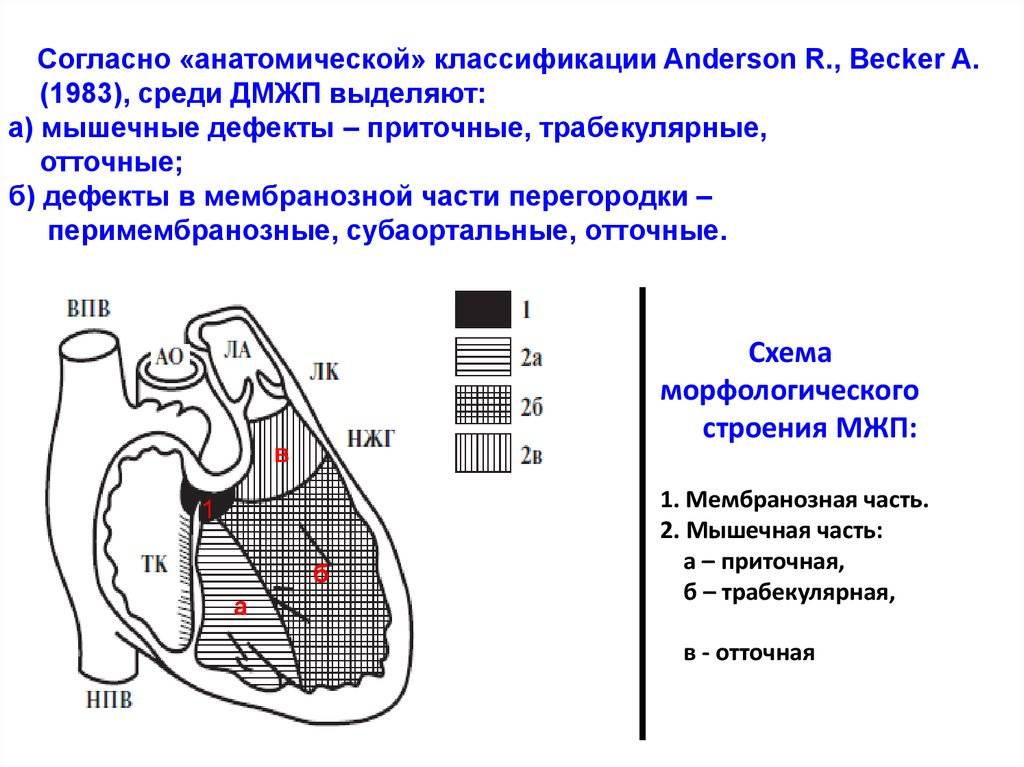
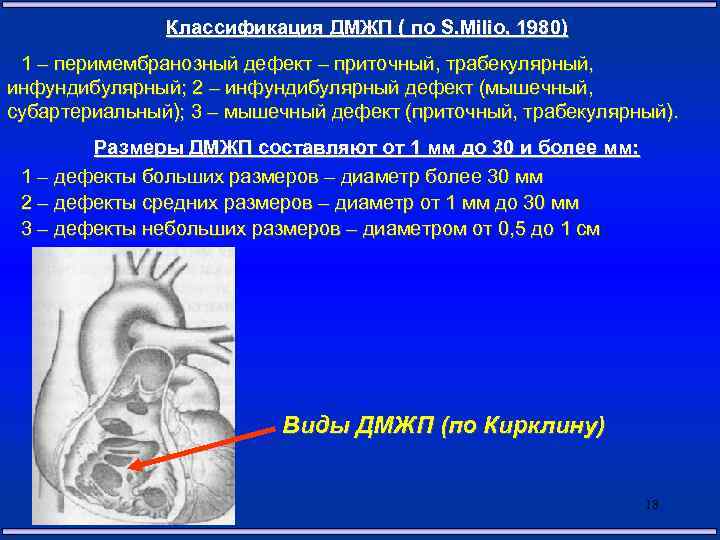
Классификация
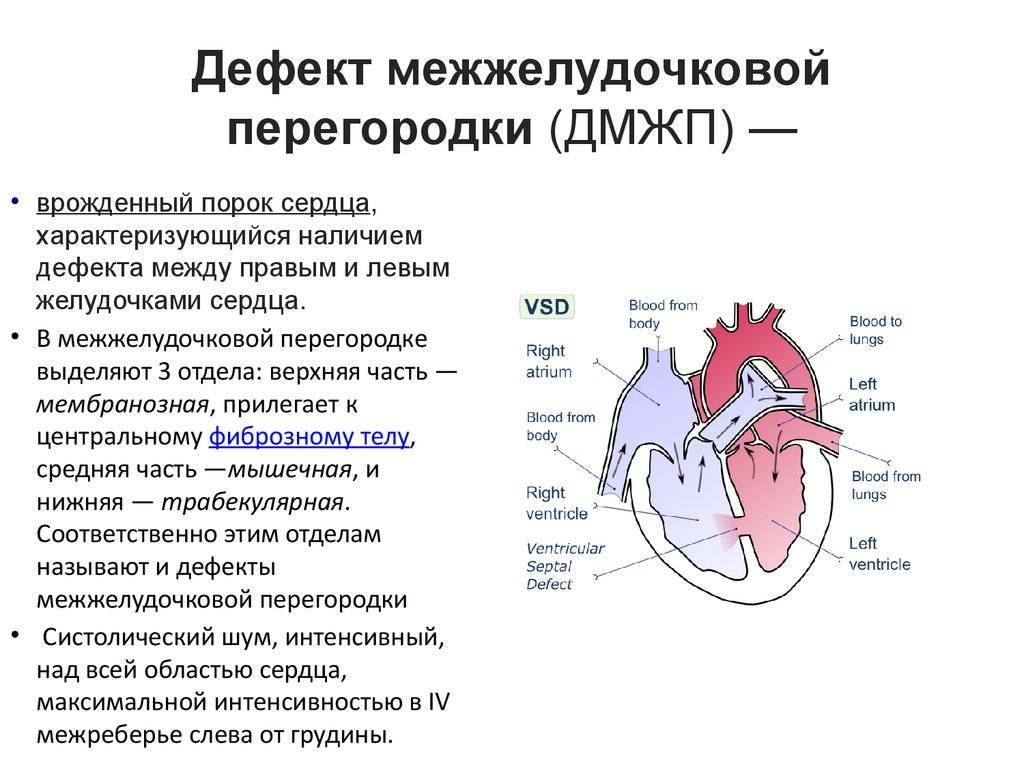
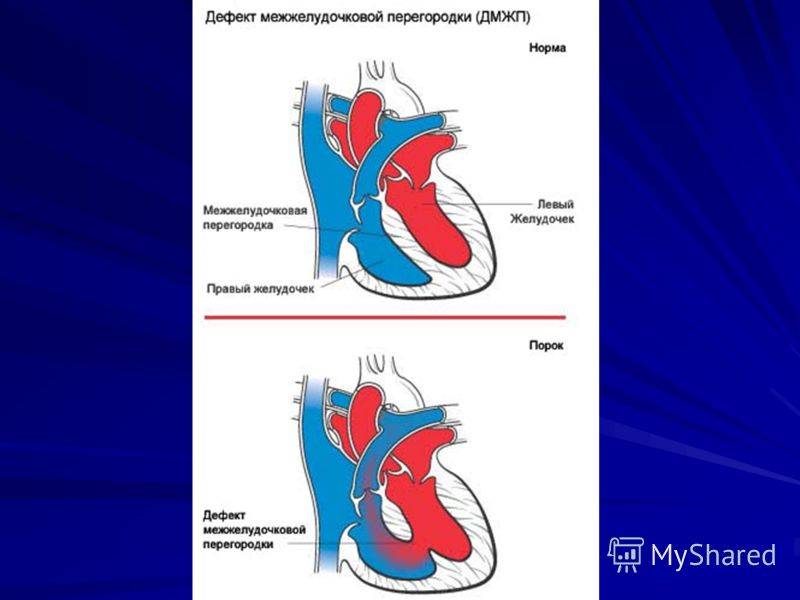
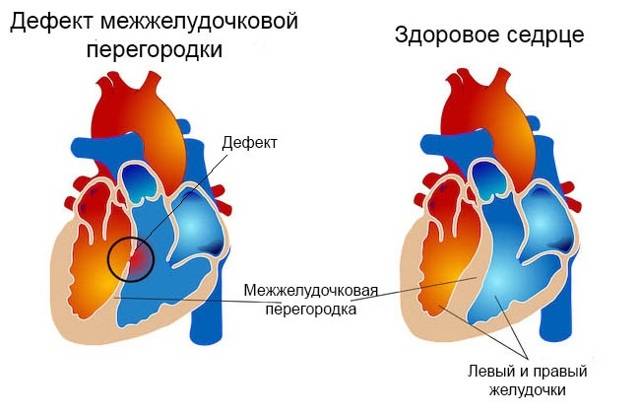
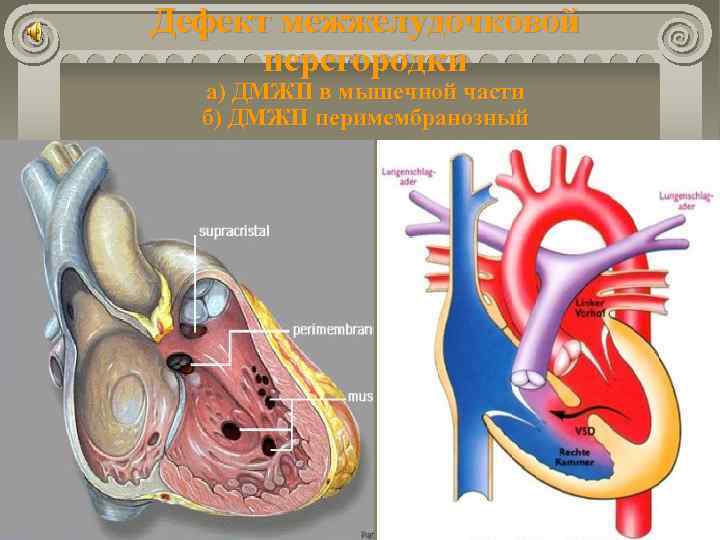
В межжелудочковой перегородке выделяют 3 отдела: верхняя часть — мембранозная, прилегает к центральному фиброзному телу, средняя часть — мышечная, и нижняя — трабекулярная. Соответственно этим отделам называют и дефекты межжелудочковой перегородки, однако большинство из них имеют перимембранозную локализацию (до 80 %). На долю мышечных ДМЖП приходится 20 %.
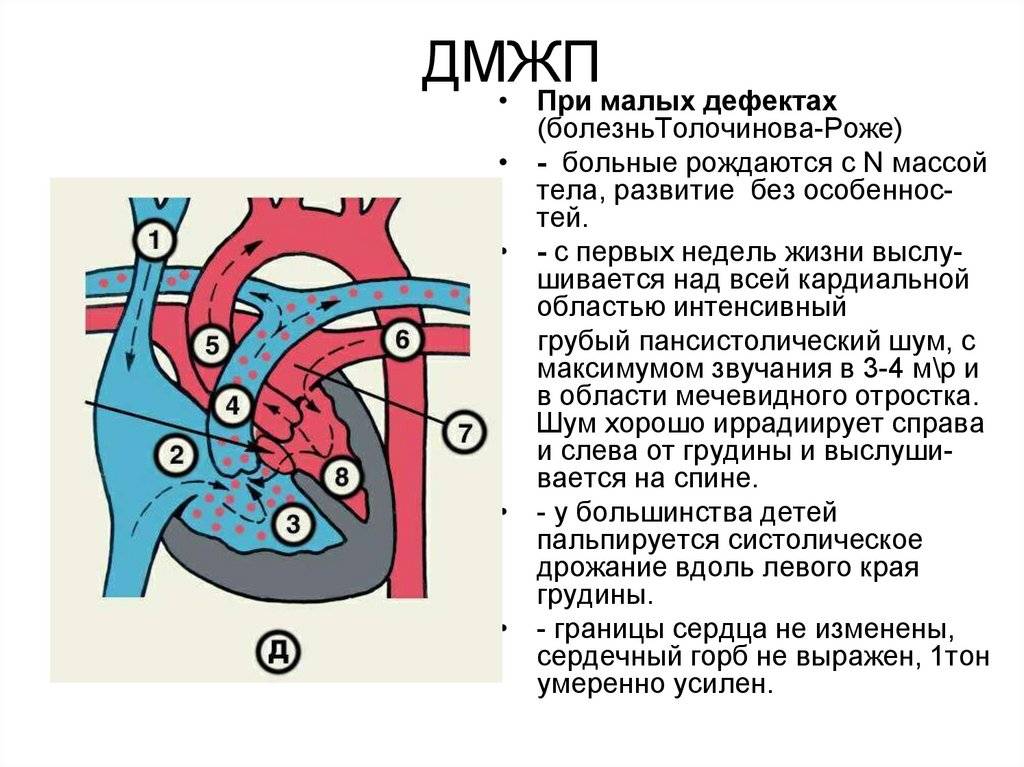
По размерам дефекты подразделяют на большие, средние и малые. Для правильной оценки величины дефекта его размер надо сравнивать с диаметром аорты. Мелкие дефекты размером 1-2 мм, расположенные в мышечной части межжелудочковой перегородки, называются болезнью Толочинова-Роже. Вследствие хорошей аускультативной картины и отсутствия гемодинамических нарушений для их характеристики уместно выражение: «много шума из ничего». Отдельно выделяют множественные большие дефекты межжелудочковой перегородки, по типу «швейцарского сыра», имеющие неблагоприятное прогностическое значение.
Лечение дефекта межжелудочковой перегородки у детей: в Израиле достигают максимального успеха
- Терапевтическая катетеризация сердца. Это малоинвазивная процедура, суть которой заключается во введении через бедренную артерию зонда вплоть до места дефекта. Через этот зонд подается сетка-заплатка, которая закрывает просвет в межжелудочковой перегородке. Со временем заплатка обрастает волокнами соединительной ткани, закрывая таким образом дефект полностью. Катетеризация проводится под контролем рентгена. Наиболее современная разновидность данной операции — установление упоминавшегося выше самораскрывающегося окклюдера AMPLATZER.
- Радикальная операция. Классическая операция по «ушиванию» дефекта, либо постановка специальной заплаты (она со временем полностью врастает в нормальные ткани сердца) проводится при помощи аппарата искусственного кровообращения. Для пластики отверстия используются либо синтетические материалы, либо ткань собственного перикарда, из которой иссекается небольшой лоскут. После того, как дефект закрыт, кровообращение нормализуется, однако регулярное наблюдение у кардиолога по-прежнему необходимо.
- Паллиативная операция. Для детей, которым по каким-то причинам не показана немедленная хирургическая коррекция дефекта, существует возможность промежуточной операции, которая снимает самые тяжелые симптомы и позволяет дать ребенку шанс на нормальное развитие. Это частичная мера лечения ДМЖП, которая позволяет значительно сузить просвет легочной артерии. Во время такой операции просвет легочной артерии искусственно суживается, что позволяет снизить кровоток в легких и понизить давление в них до нормального.
Важно учитывать, что помимо появления респираторных симптомов дефект межжелудочковой перегородки «агрессивен» с точки зрения развития так называемой легочной гипертензии. Это проявляется значительным повышением давления в легочных кровеносных сосудах
Такое грозное осложнение является противопоказанием к проведению операции, крайне необходимой для больных с большими дефектами. Поэтому немаловажным является своевременное выявление патологии и направление пациента на операцию.
Лечение дефектов межжелудочковой перегородки в Израиле
Лечение дефектов межжелудочковой перегородки хирургическое. Если у ребенка имеются признаки сердечной недостаточности, то операцию производят как можно раньше, в первый три месяца его жизни. В случае если состояние ребенка позволяет подождать, то показания к операции рассматривают, исходя из показателей давления в малом круге кровообращения. В случаях, когда давление в легочных артериях не высокое, операцию стараются отложить до 1 года, поскольку есть шансы на самостоятельное заращение дефекта межжелудочковой перегородки. Иногда существует возможность отложить операцию до возраста 5 лет.
Радикальная операция проводится с применением аппарата искусственного кровообращения. Наиболее щадящий подход к межжелудочковой перегородке осуществляется через правое предсердие. В тех случаях, когда это неосуществимо, хирурги используют возможность доступа через левое предсердие, аорту или легочную артерию. В зависимости от размеров дефекта производится сшивание отверстия. В качестве “заплаты” применяют синтетический материал или лоскут, взятый из ткани собственного перикарда пациента. Закрепление заплаты производится с помощью П-образных швов. Обшиваются все края дефекта. С помощью специальной аппаратуры проверяется герметичность заплаты.
В некоторых случаях операция осуществляется в частичном объеме. Такой подход называется паллиативным. Целью данного метода является сужение просвета легочной артерии. Вскрыв грудную клетку, через перикард открывают доступ к легочному столбу, накладывают на него лигатуру (толстую шелковую нить) и перевязывают ее, сужая диаметр легочного ствола. Процедура напоминает наложение манжеты. Степень сужения легочного ствола определяется показателями давления крови в нем, общего кровяного давления, а также путем наблюдений за установившимся в результате манипуляции режимом кровообращения.
Операции по устранению дефектов межжелудочковой перегородки проводятся только в крупных кардиоцентрах, обладающих богатым опытом, накопленным высококвалифицированными хирургами. Кардиологический центр медицинского центра «Шиба» подобные операции выполняет в большом количестве, что позволило наработать большой и успешный практический опыт.
Результаты оперативного лечения благоприятные как в ближайшем, так и в отдаленном периоде.
Пороки сердца I
- Стеноз аорты
- Стеноз лёгочной артерии
- Дефект межпредсердной перегородки первичного типа
- Дефект межпредсердной перегородки вторичного типа
- Полный дефект ПЖП
- Частичный дефект ПЖП
- Тетрада Фалло
- Дефект межжелудочковой перегородки
- Дефект МЖП и открытый артериальный проток
Пороки сердца II
- Общий артериальный ствол
- Коарктация аорты
- Открытый артериальный проток
- Аномалия Эбштейна
- Болезнь Лаутембахера
- Тотальная аномалия соединения лёгочных вен
- Транспозиция магистральных сосудов
- Комплекс Эйзенменгера
Левое предсердие
Левое предсердие имеет цилиндрическую форму, его объем у новорожденных
составляет 4-5 см3, к концу года достигает 10-14 см3,
к 7-9 годам 24-32 см3, 18-25 годам — 90-135 см3.
Размеры левого предсердия зависят от возраста. У детей до 1 года жизни
переднезадний размер составляет 0,8-1,7 см, у детей до 6 лет — 0,8-2,2
см, до 12 лет — 1,0-2,2 см, до 17 лет — 1,1-2,2 см. Ширина левого
предсердия у детей до 1 года жизни составляет 1-1,17 см, у детей до
6 лет — 1,1-2,1 см, 7-12 лет — 1,3-2,1 см, 13-17 лет — 1,5-2,3
см.
Одномерная эхокардиография левого предсердия
В одномерном режиме проводится визуализация передне-заднего размера
левого предсердия в IV стандартной позиции. В этой позиции ультразвуковой
луч пересекает область левого предсердия, прилежащую к атриовентрикулярному
отверстию.
Семиотика левого предсердия
Увеличение диаметра левого предсердия
- Открытый артериальный проток.
- Дефект межжелудочковой перегородки.
- Недостаточность митрального клапана.
- Стеноз митрального клапана.
- Надклапанное митральное кольцо.
- Рестриктивная кардиомиопатия.
- Гипертрофическая кардиомиопатия.
Уменьшение диаметра левого предсердия
- Синдром гипоплазии левого желудочка.
- Тотальный аномальный дренаж легочных вен.
- Компрессия левого предсердия экстракардиальной опухолью
средостения. - Большой дефект межпредсердной перегородки.
- Миксома левого предсердия.
- Тетрада Фалло.
- Аномалия Эбштейна.
- Двойное отхождение магистральных сосудов от правого
желудочка.
Увеличение экскурсии задней стенки левого предсердия
Связано с увеличением трансмитрального кровотока при различных физиологических
и патологических состояниях.
- Недостаточность митрального клапана.
- Начальные стадии гипертонической болезни.
- Гиперкинетический кардиальный синдром.
- Спортивное сердце.
Дополнительные эхосигналы в полости левого предсердия
- Надклапанное митральное кольцо.
- Тромб левого предсердия.
- Отрыв сухожильных нитей от передней митральной створки.
- Отрыв сухожильных нитей от задней митральной створки.
- Миксома левого предсердия.
- «Болтающийся» митральный клапан (floppy
mitral valve). - Подвижные бактериальные вегетации митрального клапана.
Левое предсердие изучают в нескольких сечениях: парастернальное сечение
длинной оси левого желудочка, в прекции 4-х камер с верхушки и из
эпигастрального доступа
Обращают внимание на форму камеры (в норме
она должна быть овальной), наличие внутриполостных образований, взаимосвязь
с левым желудочком
Литература
- 1.Банкл Г. Врожденные пороки сердца и крупных сосудов. — 1980. — 312 с.
- 2. Белозеров Ю.М. Детская кардиология. — МЕДпресс-информ, 2004. — 600 с.
- 3. Белоконь Н.А., Подзолков В.П. Врожденные пороки сердца. — 1991. — 352 с.
- 4. Василенко В.Х.,Фельдман С.Б., Могилевский Э.Б. Пороки сердца. — 1983. — 366 с.
- 5. Вишневский А.А., Галанкин Н.К. Врожденные пороки сердца и крупных сосудов. — 1962. — 210 с.
- 6. Имре Литтманн, Рене Фоно. Врожденные пороки сердца и крупных сосудов. — 1954. — 232 с.
- 7. Прахов А.В. Неонатальная кардиология. — НГМА, 2008. — 388 с.
- 8. Шарыкин. Врожденные пороки сердца. — Теремок, 2005. — 384 с.
Что выявляет УЗИ
В нашей клинике используется современное 4D оборудование, имеющее допплеровский режим. С его помощью можно получить изображение 3-х главных сосудов — верхней полой вены, лёгочного ствола и восходящей аорты. Во время обследования выявляется не только расположение сосудов, но и их диаметр и другие параметры.
На экране монитора будут видны следующие патологии плода:
- Уменьшение диаметра аорты при расширении лёгочного ствола можно говорить об гипоплазии (недоразвитости) левых отделов сердца малыша, отвечающих за начало кровообращения;
- Уменьшение ствола лёгочной артерии в размерах при сохранении в норме диаметров аорты и верхней полой вены указывает на стеноз (сужение) лёгочной артерии. У плода выявляются только выраженные формы;
- Маленький диаметр аорты при нормальном 4-камерном строении сердца является следствием коарктации аорты (сужение аорты сердца в определённом сегменте);
- Визуализация 2 сосудов вместо 3 может быть следствием соединения сосудов в общий артериальный ствол;
- Смещение аорты вперёд или правее лёгочной артерии наблюдается при транспозиции магистральных сосудов;
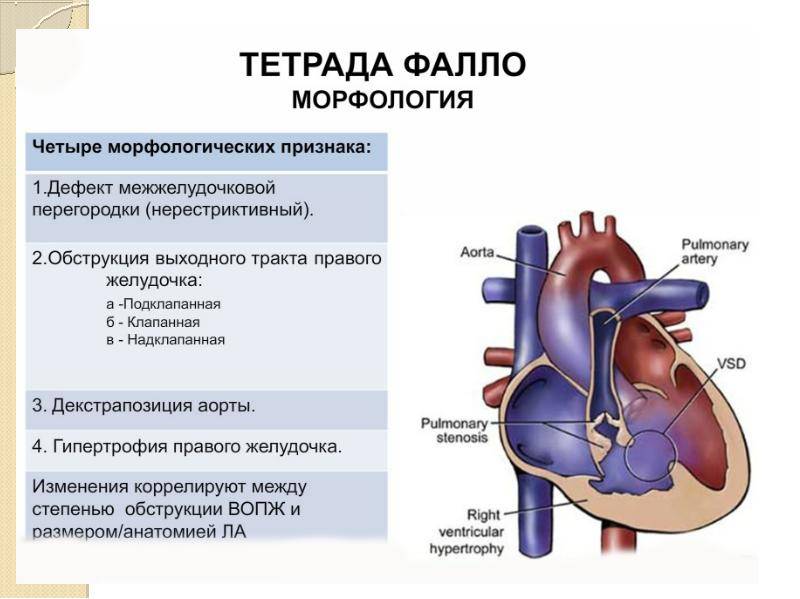
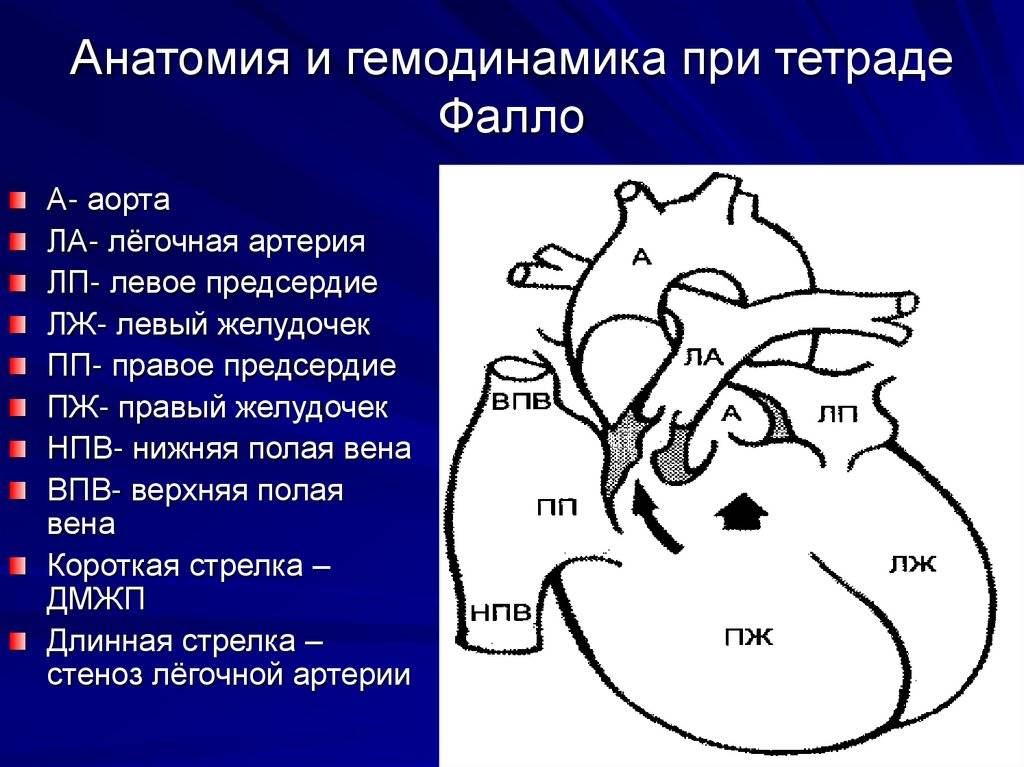
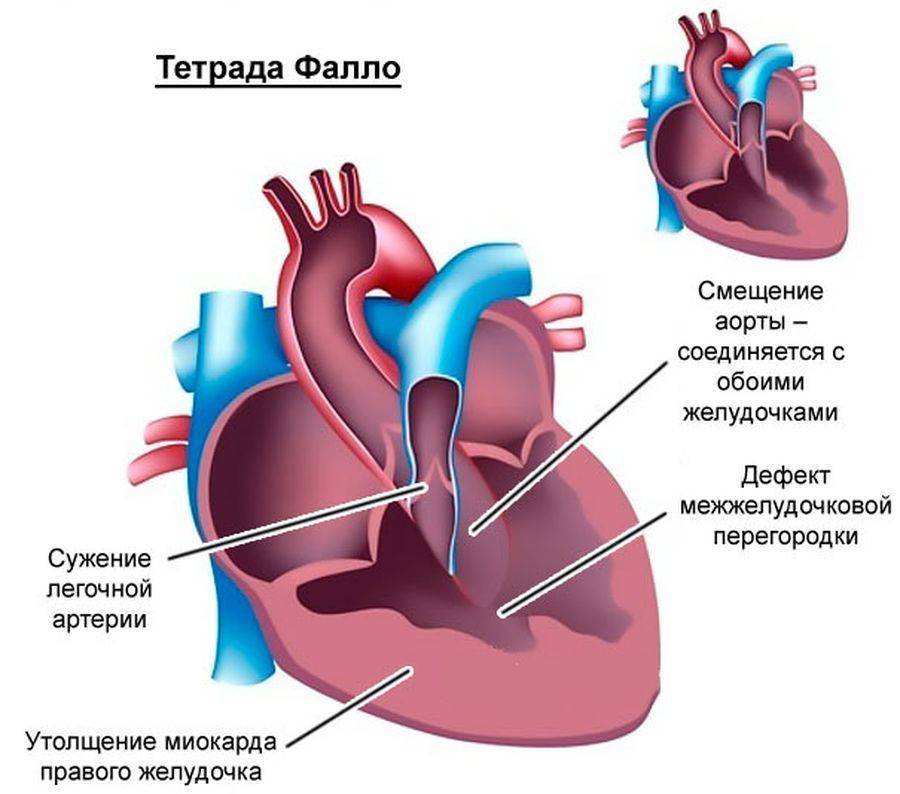
- Диаметр аорты расширен, но при этом сужен диаметр лёгочной артерии, а аорта смещена вперёд. Это может является тетрадой Фалло (очень тяжёлая сочетанная аномалия сердца). Проблема включает в себя стеноз или гипертрофию выходного отдела правого желудочка, дефект межжелудочковой перегородки, декстропозицию аорты (отхождение в правую сторону). Диагностика плода крайне затруднительна, поэтому на помощь приходит допплеровский режим, помогающий визуализировать поток крови в аорту из обоих желудочков;
- Гипоплазия (недоразвитость) правых камер сердца определяется по уменьшению их размеров относительно левых камер. Эта патология сопровождается обычно дисплазией (провисанием или выбуханием) митрального клапана;
- Общий предсердно-желудочковый канал виден как дефект перегородки сердца с расщеплением атриовентрикулярного клапана;
- Гипопластический синдром левых отделов сердца проявляется в виде недоразвития желудочка и митрального и аортального клапанов;
- Единственный желудочек также не является нормой, потому что их должно быть два и они хорошо просматриваются в четырёхкамерном срезе;
- При недоразвитости трёхстворчатого клапана кровь из правого предсердия не попадает в левое, что хорошо видно при допплеровском исследовании;
- Со 2 триместра фиброэластоз эндокарда визуализируется как утолщение миокарда и ухудшении его сокращения;
- Недоразвитие миокарда одного из желудочков (аномалия Уля) заметна на 2 триместре.
Преимущества эндоваскулярной методики
Эндоваскулярный способ закрытия дефекта выгодно отличается от операции по ушиванию ДМПП. Последняя требует искусственного поддержания кровообращения во время операции, имеет больше противопоказаний и значительный период реабилитации. Несмотря на то, что хирургическое лечение прочно вошло в практику и применялось долгое время, сейчас оно уступает место эндоваскулярному методу.
Главное преимущество в том, что эндоваскулярная операция – это малоинвазивная хирургия. После нее не остается шрамов, процедура не требует разрезов или открытого доступа. У эндоваскулярного метода чрезвычайно низкий процент послеоперационных осложнений. Пациентам не требуется длительная госпитализация и реабилитация.
На данный момент эндоваскулярная операция – это общепризнанный мировой стандарт, отвечающий всем требованиями безопасности и эффективности.
Принцип работы окклюдера
Впервые операция с помощью окклюдера была произведена в конце 80-х годов прошлого века – это был эксперимент на животных. Окклюдер – это специальное устройство, которое устанавливают через сосудистый доступ, а после установки оно выполняет функцию заплатки. Со временем техника выполнения таких операций совершенствовалась, и сейчас успешно применяется для лечения тысяч пациентов. Уже в 21 веке появилось множество модификаций и разновидностей окклюдеров для разных случаев.
Принцип работы устройства следующий: конструкция, раскрывающаяся подобно зонтику, заводится в нужное место через сосуд. После установки заплатки никаких других манипуляций не требуется. Окклюдер производят из сплавов металлов, давно применяемых в медицине – из никеля и титана, покрытых сверху специальным биосовместимым волокном. Материалы протестированы множество раз, они не вызывают аллергии. Устройство сконструировано таким образом, что центровка в отверстии перегородки происходит самостоятельно – задача врача довести окклюдер по сосудам до нужного места. Модель устройства подбирается в зависимости от конкретного дефекта – существуют разные модификации для лечения разных пороков сердца.
Доставка к сердцу производится с помощью катетера, который заводят в крупный сосуд – артерию или вену бедра. Размер окклюдера не больше 2,5 мм в диаметре, поэтому он спокойно проходит по сосудистому руслу. Устройство раскрывается только после установки в соответствующее положение рядом с дефектом перегородки.
Операция выполняется квалифицированными врачами, прошедшими специальное обучение. Процедура проводится в операционной. Пациент во время операции лежит. Врач может контролировать все свои действия с помощью специального оборудования, передающего изображение на мониторы. В ходе операции проводится мониторинг жизненных показателей.
Читать полностью
Врачи, выполняющие эндоваскулярное закрытие дефекта межпредсердной перегородки
Бабунашвили Автандил Михайлович
Врач сердечно-сосудистый хирург, заведующий отделением сердечно-сосудистой хирургии, доктор медицинских наук, профессор, заслуженный врач РФ
Стаж 34 года
Записаться на прием
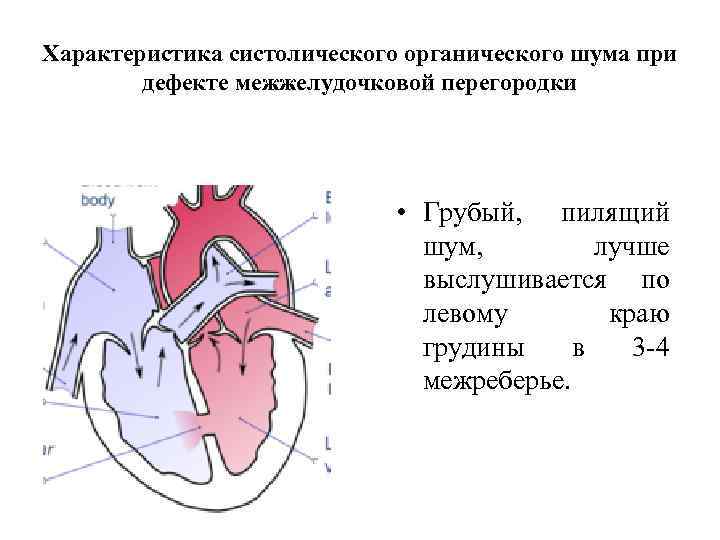
Симптомы малых и больших дефектов межжелудочковой перегородки (ДМЖП) у детей:
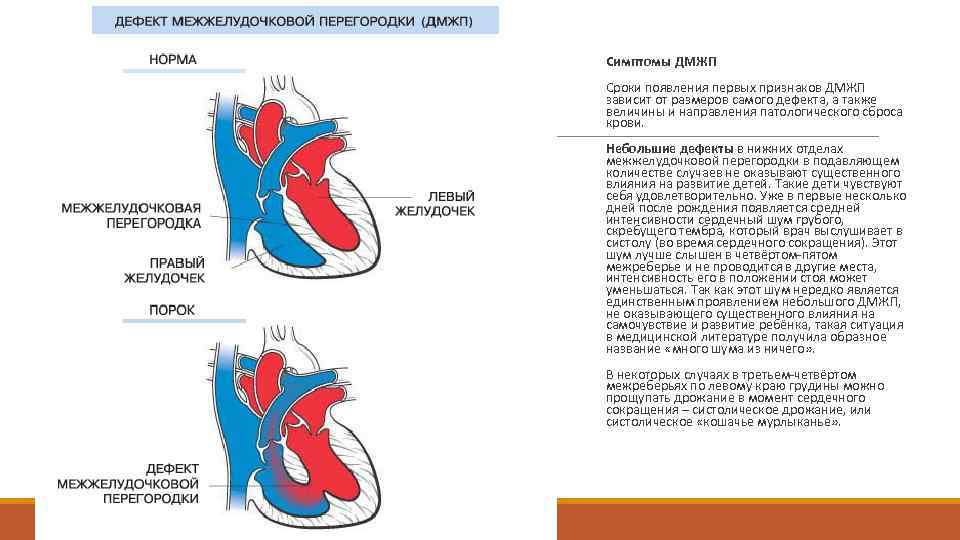
- Малые дефекты — болезнь Толочинова—Роже. Главным клиническим проявлением такого вида ДМЖП сердца у детей является грубый систолический шум над областью сердца, определяемый уже в первые дни жизни малыша. В более старшем возрасте у детей может появляться утомляемость и одышка во время физической нагрузки.При таком ДМЖП болезнь протекает достаточно благоприятно и ребенок по физической активности ничем не отличается от здоровых детей. Необходимости в проведении оперативного лечения нет. Бывают случаи, когда такие дефекты самостоятельно закрываются к 4-5 годам – они составляют 25-40%. Тем не менее такие дети должны находиться под постоянным контролем врача-кардиолога.
- Большие дефекты межжелудочковой перегородки (ДМЖП) При таком виде ДМЖП у 25-30% младенцев может развиться сердечная недостаточность. Симптомы порока выявляются в первые месяцы после рождения. Это затруднение процесса кормления, в т.ч. сосательного рефлекса, одышка, отставание в развитии, заболевания верхних дыхательных путей и воспаления легких. Впоследствии возможно появление одышки в состоянии покоя, в нижних отделах легких регистрируются застойные влажные хрипы, страдает печень.
Большие дефекты в межжелудочковой перегородке несут максимальный вред здоровью маленького пациента: они усугубляют течение и прогноз заболевания. Симптомы ДМЖП у новорожденного бывают заметны уже на первых неделях жизни: физическое развитие и набор веса замедляются в сравнении с их сверстниками; в сосудах легких повышается давление, благодаря повышенному объему крови, что в свою очередь может привести к повреждению стенок сосудов. В случае большого дефекта бывает показана операция для хирургического закрытия отверстия. Такая операция проводится на открытом сердце.
В случае малых размеров отверстия явные негативные симптомы развиваются не сразу, так как дополнительная нагрузка на сердце достаточно мала. Небольшие отверстия часто с возрастом закрываются сами.
Лечение
Лечение данного порока подразумевает консервативную терапию сердечной недостаточности и хирургическую коррекцию порока сердца. Консервативное лечение складывается из препаратов инотропной поддержки (симпатомиметики, сердечные гликозиды), мочегонных препаратов, кардиотрофиков.
В случаях высокой легочной гипертензии назначаются ингибиторы ангиотензинпревращающего фермента — капотен или каптоприл.
Оперативные вмешательства подразделяются на паллиативные операции (в случае ДМЖП — операция суживания лёгочной артерии по Мюллеру) и радикальную коррекцию порока — пластика дефекта межжелудочковой перегородки заплатой из листков перикарда в условиях искусственного кровообращения, кардиоплегии и гипотермии.
Уход за ребенком после операции на сердце
Берегите ребенка от инфекцийУход за рубцомГрудинаПрием препаратов, которые выписал врачмерить температуруСообщайте врачу о таких симптомах:
- повышение температуры выше 38°С;
- шов припух и из него начнет вытекать жидкость;
- боль в груди;
- бледность или синеватый оттенок кожи;
- припухлость лица, вокруг глаз или другие отеки;
- одышка, усталость, отказ от игр;
- тошнота, рвота;
- головокружение, потеря сознания.
Общение с врачами
- Анализ мочи первый месяц придется сдавать каждые десять дней. А следующие полгода 2 раза в месяц.
- Электрокардиограмму, фонокрадиограмму, эхокардиографию необходимо будет делать 1 раз в три месяца первые полгода. В дальнейшем два раза в год.
- Через некоторое время желательно съездить с ребенком в специальный санаторий на 1-3 месяца.
- Прививки придется отложить на полгода.
- В общей сложности ребенок будет оставаться на учете у кардиологов на протяжении 5 лет.
Питание
- Свежие фрукты и соки.
- Свежие и приготовленные овощи.
- Блюда из мяса, вареного, запеченного или тушеного.
- Молочные продукты: молоко, творог, йогурты, сметана. Особенно полезна будет творожная запеканка с сухофруктами.
- Яйца вареные или в виде омлета.
- Различные супы и блюда из круп.
Методы исследования
Заболевание может быть выявлено на плановом обследовании у кардиолога в первый год жизни ребенка. Если этого не произошло и появились явные симптомы, производится сбор анамнеза, пациент осматривается на предмет оценки цвета кожных покровов, характера дыхания, внутригрудных шумов. Далее требуется аппаратная диагностика, которая проводится следующими способами:
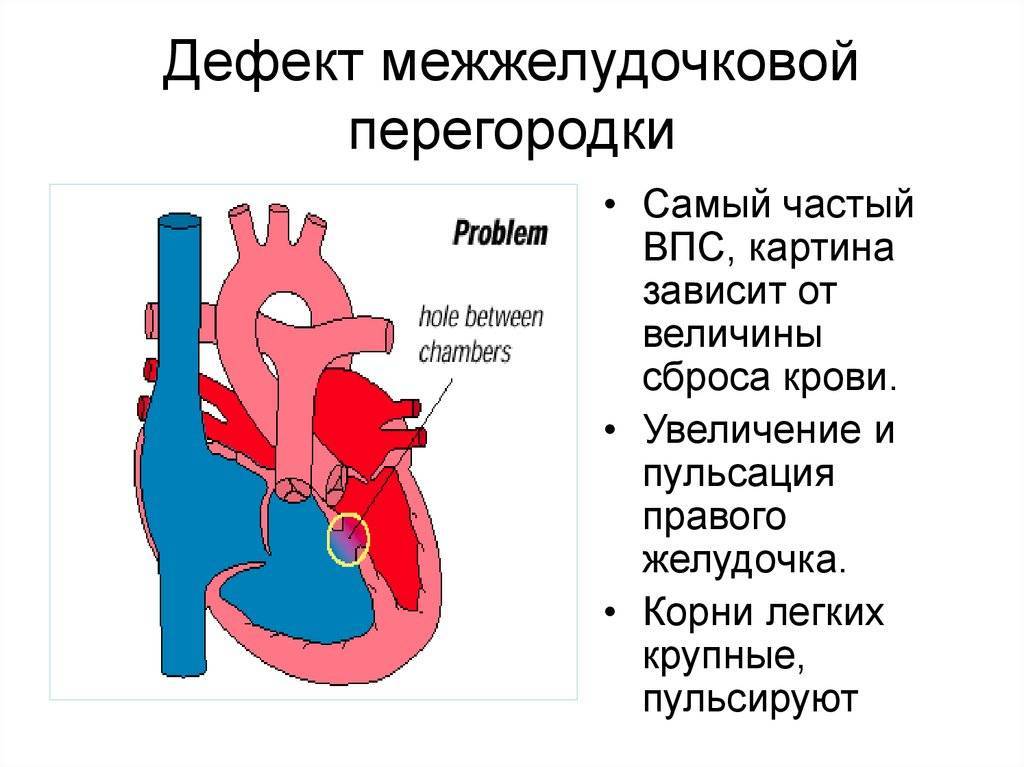
- ЭКГ. Показывает перегрузку в работе правосторонней части органа.
- Рентгенография. Проявляет усиленный легочный рисунок, увеличение легочной артерии и сердечной тени на снимках.
- Рентгеноскопия. Фиксирует усиление пульсации легочных корней, что является специфическим симптомом ДМПП.
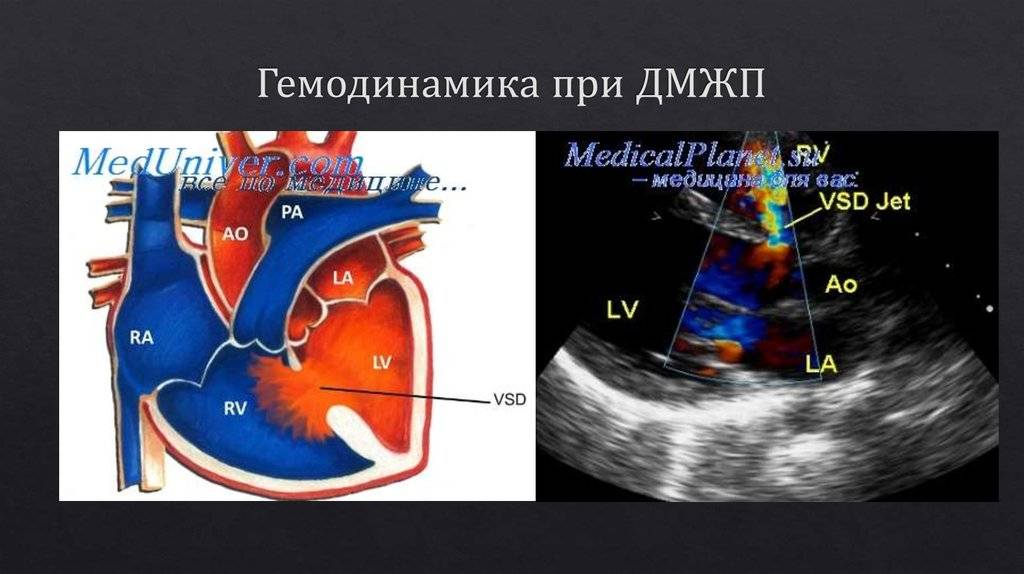
- ЭхоКГ. Визуально показывает локализацию просвета, определяет его размеры, а также левосторонний сброс кровяной массы.
- Зондирование сердечных полостей. Фиксирует повышение внутрисердечного давления в правосторонних сегментах.
- МРТ сердца. Наиболее информативная методика, способная предоставить полный объем информации о состоянии сердечно-легочной системы, если остальные диагностические методики не показали эффективности.
Лучшим вариантом исследования при врожденных дефектах строения внутренних органов служит МРТ. Без травмирования и болезненности, которые присущи стандартным эндоскопическим и зондирующим методикам, без повышенного радиационного излучения в противовес рентгену, можно сделать полноценное сканирование в любом возрасте, начиная с первых дней жизни. За один короткий сеанс врачи получат исчерпывающие данные об имеющихся нарушениях, что поможет вовремя приступить к лечению, избежать тяжелых последствия в будущем.