SQLITE NOT INSTALLED
Содержание статьи:
Лимфома (lymphoma) – злокачественная опухоль клеток иммунитета.При ней лимфоциты увеличиваются до гигантских размеров, бесконтрольно делятся и поражают лимфатическую систему: лимфоузлы, костный мозг, вилочковую железу.
От других онкологических заболеваний лимфома отличается диссеминацией по всему организму: с током лимфы переродившиесязлокачественныеклетки попадают во внутренние органы и критически нарушают их работу. Болезнь долго течет бессимптомно, а когда начинает проявляться, то часто весь организм уже поражен.
Большинстволимфомхарактеризуетсяпрогрессирующим течением и высокой злокачественностью с метастазированием. Тем не менее при раннем их выявлении благоприятный прогноз достигает ~90%.
Статистические данные о лимфомах:
- Ежегодно в России выявляют около 25 000 пациентов с раком данного типа – это 4% от всех онкобольных.
- Мужчины болеют чаще, чем женщины.
- Возрастной пик заболеваемости – 30-34 года и после 60 лет.
- В группе риска – больные с артритом двух и более суставов.
- Провоцирующий фактор – дефицит селена в организме.
- Есть предположение, что окрашивание волос чаще 1 раза в месяц темной краской увеличивают риск развития лимфомы на 26%.
- Считается что витамин Д обладает защитными свойствами против лимфомы.
- Благодаря современным методикам и препаратам за последние 10 лет смертность от лимфом в России снизилась на 27%.
Лечение Лейкоза у детей:
При обнаружении лейкоза ребенка нужно госпитализировать в специализированное учреждение онкогематологического профиля. Чтобы не возникли инфекционные осложнения, ребенка помещают в отдельный бокс, условия в котором максимально приближенны к стерильным. Рацион больного обязательно должен быть сбалансированным и полноценным.
Для лечения лейкозов необходима полихимиотерапия, направленная на полную эрадикацию лейкозного клона. При острых лимфобластных и миелобластных лейкозах необходима различная комбинация химиопрепаратов, дозы и способы введения.
Этапы лечения:
- достижение ремиссии болезни
- закрепление ремиссии
- поддерживающая терапия
- профилактика / лечение осложнений
Химиотерапию в части случаев дополняют активной и пассивной иммунотерапией: вакцинами БЦЖ, введением лейкозных клеток, интерферонами, противооспенной вакциной и т.д. Сегодня исследуется эффективность методов трансплантации пуповинной крови, костного мозга, стволовых клеток.
Также необходимо симптоматическое лечении при лейкемии у детей:
- проведение гемостатической терапии
- переливание эритроцитарной и тромбоцитарной массы
- дезинтоксикационные мероприятия (гемосорбция, внутривенные инфузии, плазмаферез, плазмосорбция)
- антибиотикотерапия инфекционных осложнений
Прогноз лейкоза у детей
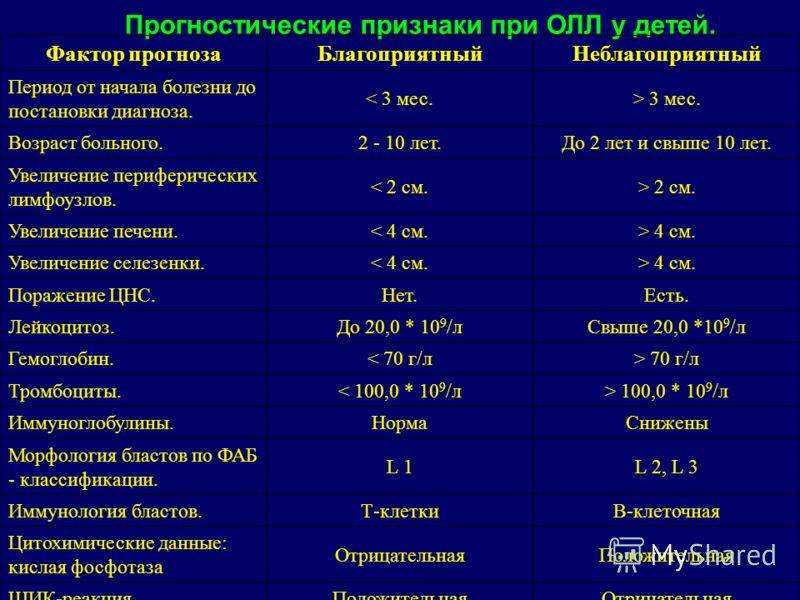
Прогноз зависит от возраста ребенка, когда у него возник лейкоз, от стадии диагностирования и прочих факторов. Худший прогноз дают детям, у которых лейкоз возник в возрасте до 2-х лет и старше 10-ти лет; у детей с диагнозом гепатоспленомегалии и лимфаденопатии; с нейролейкозом на момент диагностирования лейкемии. Также плохой прогноз у детей с Т- и В-клеточными вариантами лейкоза, при бластном гиперлейкоцитозе.
Благоприятный прогноз при остром лимфобластном лейкозе L1 типа; в случаях раннего начала лечения, при быстром достижении ремиссии; у детей в возрасте 2-10 лет. У девочек с острым лимфобластным лейкозом вероятность излечение несколько выше, чем у мальчиков.
При непроведении специфического лечения лейкоза у детей, гарантирован смертельный исход. Современная химиотерапия позволяет обеспечить отсутствие рецидивов на протяжении 5 лет у большинства детей. О вероятном выздоровлении можно говорить, если рецидива лейкоза не было 6-7 лет.
Лечение острого лимфобластного лейкоза
Протокол лечения острого лимфобластного лейкоза включает 4 фазы: индукция ремиссии, профилактика поражения центральной нервной системы, консолидация или интенсификация (после ремиссии) и поддержание ремиссии.
Ряд режимов придают особое значение раннему применению интенсивной многокомпонентной терапии. Режимы индукции ремиссии предусматривают ежедневный прием преднизолона, еженедельное введение винкристина с добавлением антрациклина или аспараги-назы. Другие препараты и комбинации, применяемые на ранних этапах лечения, включают цитарабин и этопозид, а также циклофосфамид. Некоторые режимы содержат средние или высокие дозы метотрексата внутривенно с лейковорином, применяемым с целью снижения токсичности. Комбинации и дозы препаратов могут модифицироваться в зависимости от наличия факторов риска. Аллогенная трансплантация стволовых клеток рекомендуется в качестве консолидации при Ph-позитивном остром лимфобластном лейкозе или при втором или последующем рецидиве или ремиссии.
Мозговые оболочки являются важной локализацией поражения при остром лимфобластном лейкозе; при этом профилактика и лечение могут включать интратекальное введение высоких доз метотрексата, цита-рабина и глюкокортикоидов. Может потребоваться облучение черепных нервов или всего головного мозга, эти методы часто используются у больных с высоким риском поражения центральной нервной системы (например, высокое количество лейкоцитов, высокий уровень лактатде-гидрогеназы в сыворотке, В-клеточный фенотип), но в последние годы их распространенность снизилась
4.Лечение заболевания
Лечение острого лимфобластного лейкоза зависит от множества факторов: вашего возраста, течения заболевания и других нюансов. В большинстве случаев врач использует несколько разнообразных методик лечения, наблюдая за состоянием пациента. К ним относятся:
Химиотерапия. Она представляет собой медикаментозный способ лечения, суть которого заключается в блокировке роста патологических клеток. Чаще всего одного вида препарата недостаточно для того, чтобы уничтожить все лейкозные клетки, поэтому применяются комбинации из следующих лекарственных средств:
- Винкристин;
- Цитарабин;
- Даунорубицин;
- Этопозид;
- L-Аспарагиназа;
- Тенипозид;
- Метотрексат.
Лучевая терапия. Лучевая терапия основана на применении высокоэнергетического излучения, убивающего раковые клетки. Главная цель такого метода лечения лейкоза заключается в удалении злокачественных клеток с минимальным повреждением окружающих их тканей.
Таргетная терапия. В ее основе лежат принципы целевого воздействия на фундаментальные молекулярные механизмы, которые вызывают то или иное заболевание. В отличие от классических методик лечения онкологии, таргетная терапия способствует уничтожению только раковых клеток, не оказывая неблагоприятного влияния на здоровые ткани организма.
Пересадка костного мозга. Трансплантация стволовых клеток, как правило, осуществляется, когда все другие методы лечения острого лимфобластного лейкоза не были эффективными.
Симптомы Лимфогранулематоза у детей:
Болезнь начинается незаметно. Сначала больной ребенок чувствует себя абсолютно нормально. Он находит на шее увеличенный, безболезненный, плотноватой консистенции лимфатический узел. Реже первыми реагируют узлы средостения, паховые или подмышечные. Еще реже лимфогранулематоз у детей проявляется с изолированного поражения желудка, селезенки, легких, кишечника, костей, костного мозга.
При абдоминальной форме гранулематоза, которая в принципе является очень редкой, сначала поражаются забрюшинные лимфоузлы. При пальпации любые узлы не вызывают болевых ощущений. Сначала они имеют плотноэластическую консистенцию, не спаяны между собой и кожей. Постепенно они становятся малоподвижными из-за сращений, уплотняются, не достигая однако степени каменистой плотности и никогда не спаиваясь с кожей.
Распространенный симптом гранулематоза у детей – поражение селезенки. Но для пальпации она доступна примерно в трети случаев. Важным симптомом выступает повышение температуры тела. Сначала лихорадка эпизодическая, потом она наступает волнами, не проходит при приеме ацетилсалициловой кислоты, антибиотиков, анальгина. Вместе с лихорадкой у ребенка появляется потливость, особенно в ночное время суток. Но ознобы не наблюдаются. Лихорадочный синдром наблюдается у 60 детей с данным диагнозом из 100.
В трети случаев болезнь начинается с зуда кожи, который становится все более упорным, его нельзя снять обычными средствами. Дети могут жаловаться на головную боль, скованность в суставах и мышцах, сердцебиение. В начале болезни, как правило, ребенок теряет массу тела, у него возникает слабость, может быть снижение аппетита. Но эти симптомы не называют специфическими. В части случаев бывает и гепатолиенальный синдром.
Иммунитет нарушается, потому часто присоединяются бактериальные и вирусные инфекции. У большинства детей изменен состав: относительная или абсолютная лимфоцитопения, нейтрофильный лейкоцитоз с умеренным палочко-ядерным сдвигом, повышение СОЭ. В начале заболевания тромбоциты в норме. Может быть эозинофилия, нормохромная анемия.
В терминальной стадии лимфогранулематоза симптомы общей интоксикации выражены больше, нарушается функция сердечно-сосудистой, дыхательной, нервной систем. При современных методах лечения больной может прожить 60—80 месяцев от начала заболевания. Но имеются сообщения о случаях полного выздоровления при лимфогранулематозе, когда была проведена адекватная химио- и лучевая терапия. В конце лимфогранулематоз перерождается в саркому в некоторых случаях, что утяжеляет состояние больного. Анемия и истощение прогрессируют быстрыми темпами, появляются тромбоцитопения и кровоточивость.
Абдоминальная форма лимфогранулематоза у детей протекает тяжело. У ребенка наблюдаются такие симптомы:
- проливной пот
- абдоминальные боли
- высокая лихорадка
- лейкопения
- высокая СОЭ
- резкий сдвиг формулы крови влево
Плохим прогностическим признаком служит поражение печени. Наилучший прогноз дают в тех случаях, когда СОЭ нерезко повышена и уровень лимфоцитов достаточен. неблагоприятный прогноз почти во всех случаях болезни детей.
Две формы болезни по скорости клинического течения:
- хроническая
- подострая
Формы негенерализированного лимфогранулематоза у детей:
- локальная
- регионарная
При локальной происходит поражение 1—2 смежных областей, а при регионарной вовлечены 2 и больше лимфатических узла несмежных зон по одну сторону от диафрагмы. Генерализованной стадии свойственно увеличение 2 и более групп лимфатических узлов, расположенных по обе стороны от диафрагмы, а также вовлечение в процесс селезенки.
Лабораторные признаки интоксикации:
- лимфоцитопения
- повышение СОЭ более 30 мм в час
- увеличение содержания С-реактивного белка
- увеличение содержания альфа-2- и гамма-глобулинов, сиаловых кислот
- увеличение содержания церулоплазмина, фибриногена
Этиопатогенез
Точные причины возникновения ОЛЛ неизвестны. Предполагают, что, как и в случае других злокачественных заболеваний, болезнь развивается в результате неблагоприятного сочетания воздействия окружающей среды, наследственной предрасположенности и шанса. Изучение этиологии ОЛЛ усложняется разнообразием подтипов болезни, каждый из которых может иметь свои причины.
Возникновение злокачественного клона
Считают, что в случае детского В-ОЛЛ предлейкозный клон возникает в организме ребёнка ещё в ходе внутриутробного развития. При В-ОЛЛ, ассоциированном с мутацией гена MLL, злокачественное перерождение B-клетки, по всей видимости, завершается до рождения. Это подтверждается тем, что если он возникает у одного из монозиготных близнецов с общей или монохориональной плацентой, то возникает и у второго с вероятностью практически 100 % и проявляется вскоре после рождения. Пик заболеваемости В-ОЛЛ с другими цитогенетическими характеристиками приходится на более поздний возраст — 2—5 лет. Эти виды лейкоза развиваются у обоих близнецов только в 10—15 % случаев. Это может говорить о том, что, хотя предлейкозный клон возникает во время внутриутробного развития, для его окончательной трансформации нужны дополнительные события.
Возможные причины и факторы риска
В качестве возможных причин ОЛЛ рассматривают:
- ионизирующую радиацию — ионизирующая радиация была выявлена как причина ОЛЛ и других видов лейкоза при изучении последствий атомных бомбардировок Японии. Повышенная частота развития ОЛЛ была обнаружена у людей, работавших с радиографическим оборудованием до установления современного уровня безопасности. Люди, прошедшие курс радиотерапии, имеют повышенный риск развития так называемых вторичных лейкозов, в том числе и ОЛЛ. Рентгеновская пельвиметрия во время беременности немного увеличивает риск развития ОЛЛ у ребёнка, при этом риск растёт пропорционально числу процедур. Некоторые исследователи предполагают, что естественная радиация и космическое излучение могут быть причинами ОЛЛ, но эта точка зрения является спорной;
- инфекции — возбудитель детского ОЛЛ до сих пор не был обнаружен. Существует несколько гипотез на этот счёт, но они сходятся в том, что развитие лейкоза является результатом аномального иммунного ответа на присутствие инфекционного агента. По гипотезе Кинлена, причиной детского ОЛЛ является неизвестный возбудитель, скорее всего вирус, к которому у большинства детей развивается естественный иммунитет, однако у небольшой части особенно чувствительных детей этот возбудитель вызывает лейкоз. По гипотезе Гривса, причиной детского ОЛЛ может быть множество неспецифических возбудителей (например, вирусы гриппа), которые вызывают спонтанные мутации в B-клетках детей, имевших мало контактов с патогенами на первом—втором годах жизни (например, не посещавших ясли);
- генетическую предрасположенность — мутации, вызывающие ОЛЛ с высокой пенетрантностью, пока не обнаружены. Однако широкомасштабные исследования генома заболевших выявили, что некоторые аллельные варианты генов IKZF1, ARID5B, CEBPE и CDKN2A ассоциированы с повышенным риском развития ОЛЛ. Такие аллели имеют аддитивный эффект. Продукты перечисленных генов вовлечены в дифференцировку и пролиферацию кровяных клеток. Также риск развития ОЛЛ резко повышен у больных синдромом Дауна — примерно в 40 раз у детей в возрасте до четырёх лет.
Паллиативная помощь
Для терапии острого лейкоза имеется большое количество методов лечения. Это может быть химиотерапия, таргетная терапия, иммунотерапия. Все эти методы могут привести к ремиссии даже после многократных рецидивов. Поэтому как таковая, паллиативная терапия назначается редко и, как правило, у возрастных пациентов, которые не могут перенести тяжелое лечение.
В этом случае используется химиотерапия, медикаментозная терапия и лучевая терапия.
Химиотерапия
Химиотерапия при паллиативном лечении проводится не с целью достижения ремиссии, а для удержания опухолевого клона от стремительного размножения. На этом этапе могут применяться стандартные цитостатические препараты в меньших дозировках, иммунотерапия, таргетная терапия и другие методы противоопухолевого лечения.
Лучевая терапия
Лучевая терапия может применяться для облегчения болевого синдрома при сильном поражении костей, а также при наличии внекостномозговых очагов.
Сопроводительная медикаментозная терапия
Устранение болевого синдрома
Для помощи пациентам с болевым синдромом применяют различные обезболивающие препараты, начиная от нестероидных противовоспалительных препаратов (тот же ибупрофен) и заканчивая легкими и/или тяжелыми наркотическими средствами. Уменьшить выраженность болевого синдрома помогает и лучевая терапия.
Профилактика инфекций
На терминальных стадиях у больных серьезно нарушено кроветворение, и, как следствие, нет полноценной защиты от всех видов инфекций — бактериальной, грибковой, вирусной, что может привести к гибели пациента. Инфекционные осложнения являются одной из ведущих причин смерти при терминальных стадиях лейкозов.
Для предотвращения заражения, рекомендуется тщательно соблюдать принципы гигиены — уход за полостью рта, антисептическая обработка рук как самого больного, так и ухаживающего персонала, назначение профилактических антибактериальных и противогрибковых препаратов.
Трансфузионная поддержка
При сильном угнетении кроветворения, развивается тяжелая анемия и тромбоцитопения. Для купирования этих состояний могут применяться трансфузии эритроцитарной и тромбоцитарной массы.
Тромбоцитарные трансфузии
Раньше тромбомассу переливали при снижении количества тромбоцитов ниже 20*109/л. Но потом появились рекомендации, согласно которым тромбоцитарные трансфузии проводят при падении уровня тромбоцитов ниже 10*109/л. При более высоких цифрах назначение тромбомассы не приводит к снижению риска развития кровотечения.
При появлении признаков геморрагического синдрома, тромбоцитарную трансфузию начинают немедленно и при необходимости увеличивают ее объем. Признаки геморрагического синдрома:
- Наличие петехиальных высыпаний, особенно в полости рта и других слизистых.
- Повышение температуры при отсутствии очагов инфекции.
- Наличие кровотечения.
- Возникновение инфекции.
Трансфузии эритроцит-содержащих сред
У терминальных больных желательно поддерживать целевой уровень гемоглобина не ниже 80 г/л
Особое внимание уделяется пациентам с тромбоцитопениями. При развитии тяжелых анемий показано переливание эритромассы до достижения целевого уровня
В настоящее время во всем мире принят принцип — если больного нельзя вылечить, это не значит, что ему нельзя помочь!
Запись на консультацию круглосуточно
+7 (495) 151-14-53+7 (861) 238-70-54+7 (812) 604-77-928 800 100 14 98
Причины и факторы риска
Конкретную взаимосвязь между определёнными воздействиями и появлением рака крови обнаружить пока не удалось, однако факторы риска, повышающие вероятность возникновения болезни, хорошо известны онкологам.
- Наследственность. Если в семье имеются случаи заболевания, то риск возрастает в 3-5 раз. Кроме того, существенным фактором риска являются генетические болезни.
- Радиация. Значительно чаще, чем обычно, симптомы лейкоза возникают у людей, подвергшихся радиационному воздействию.
- Химические вещества. Патогенным воздействием, провоцирующим мутацию клеток крови, обладают десятки химических соединений, с которыми люди контактируют в процессе профессиональной деятельности. В частности, к ним относятся пары бензина.
- Курение. У курящих людей в несколько раз возрастает риск острого миелобластного лейкоза.
Присутствие одного и даже нескольких перечисленных факторов не означает, что человек обязательно заболеет, однако вероятность онкопатологии крови у них существенно повышена.
К каким докторам следует обращаться если у Вас Острый лимфобластный лейкоз:
Гематолог
Терапевт
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Острого лимфобластарного лейкоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, изучат внешние признаки и помогут определить болезнь по симптомам, проконсультируют Вас и окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Online-консультации врачей
| Консультация специалиста по лечению за рубежом |
| Консультация кардиолога |
| Консультация иммунолога |
| Консультация нейрохирурга |
| Консультация гомеопата |
| Консультация массажиста |
| Консультация невролога |
| Консультация радиолога (диагностика МРТ, КТ) |
| Консультация педиатра |
| Консультация нарколога |
| Консультация косметолога |
| Консультация детского психолога |
| Консультация неонатолога |
| Консультация нефролога |
| Консультация психолога |
Новости медицины
Футбольные фанаты находятся в смертельной опасности,
31.01.2020
«Умная перчатка» возвращает силу хвата жертвам травм и инсультов,
28.01.2020
Назван легкий способ укрепить здоровье,
20.01.2020
Топ-5 салонов массажа в Киеве по версии Покупон,
15.01.2020
Новости здравоохранения
Глава ВОЗ объявил пандемию COVID-19,
12.03.2020
Коронавирус атаковал уже более 100 стран, заразились почти 120 000 человек,
11.03.2020
Коронавирус атаковал 79 стран, число жертв приближается к 3200 человек,
04.03.2020
Новый коронавирус атаковал 48 стран мира, число жертв растет,
27.02.2020
Основные риски для детей с острым лимфобластным лейкозом
При остром лимфобластном лейкозе есть определенные риски, которые могут повлиять на исход лечения. Они основаны на соотношении возраста и «дефектных» лейкоцитов при постановке диагноза.
За ребенком, страдающим ОЛЛ, должна ухаживать команда специалистов – то есть лечение производится только в условиях стационара. Крайне важны долгосрочные и регулярные повторные обследования
Лечение ОЛЛ может иметь долгосрочные последствия для памяти, способности к обучению и других аспектов здоровья. Помимо прочего это также может увеличить шансы развития иных онкологических заболеваний, особенно опухоли мозга.
ОЛЛ, как правило, очень быстро прогрессирует, если не приступить к лечению немедленно.
Как проявляется лейкоз
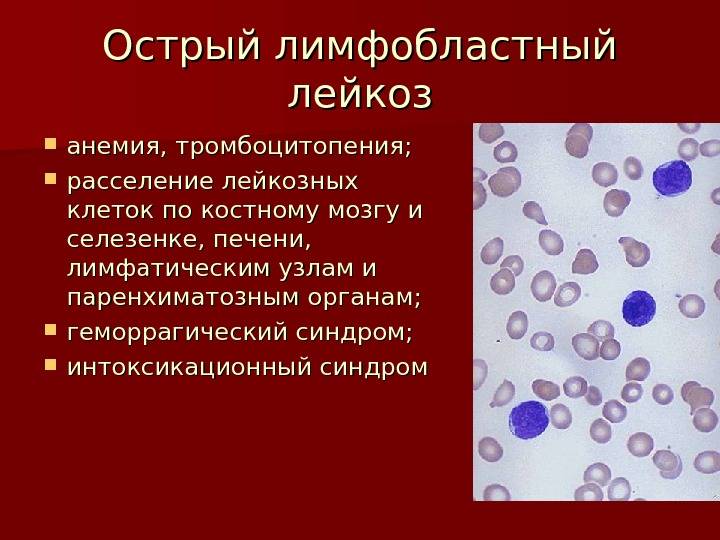
При лейкемии нарушается процесс формирования клеток крови. Нормальные лейкоцитарные клетки заменяются на патологически измененные, которые не могут выполнять свои функции. Больные клетки дольше живут по сравнению со здоровыми, но при этом не созревают до конца и бесконтрольно делятся, увеличивая свою популяцию. При лейкозе вытесняются нормальные лейкоциты, отмечается уменьшение количества тромбоцитов и эритроцитов. Из-за этого работа системы кроветворения нарушается.
Лейкемия поражает костный мозг, лимфоузлы, селезенку, печень, вызывает негативные изменения со стороны нервной системы. У пациентов с гемобластозами развивается анемия, появляется склонность к кровотечениям, снижается иммунитет из-за дефицита здоровых белых клеток крови. Для таких людей повышенную опасность представляют любые инфекционные заболевания. Из-за низкой сопротивляемости организма болезнь может приводить к серьезным осложнениям, включая летальный исход.
Клетки опухоли из костного мозга начинают распространяться по всему организму, вызывая нарушения в работе органов и тканей. В первую очередь страдают лимфоузлы, которые увеличиваются в размере. При попадании в печень и селезенку раковые клетки вызывают их гиперплазию — увеличение в размере. При проникновении лейкозных клеток в мозговые оболочки наблюдается различные нарушения в работе ЦНС. Пациент жалуется на головную боль, у него может возникнуть рвота, паралич зрительного и лицевого нерва. У людей зрелого возраста нередко возникает одышка и нарушения в работе сердца.
Причины возникновения острого лейкоза
Лейкозы возникают из-за мутации ГСК. При этом разные мутации проявляются на разных этапах гемопоэза. Следует сказать, что одного факта наличия мутации недостаточно. Вообще генетические поломки в клетках, в том числе и гемопоэтических, возникают регулярно, но существуют механизмы, которые либо уничтожают такие клетки, либо блокируют ее дальнейшее развитие. Чтобы развился лейкоз, нужны особые обстоятельства:
- Повторные мутации в уже мутировавшей ГСК.
- Ослабление иммунной защиты, при которой мутировавшая клетка остается нераспознанной и начинает активно размножаться. Такие промахи иммунитета могут возникнуть как в период внутриутробного развития, так и в процессе жизни взрослого человека.
Таким образом, к факторам риска развития острого лейкоза относят следующие:
- Наследственная предрасположенность.
- Вторичные и первичные иммунодефициты.
- Воздействие ионизирующего излучения — рентген, лучевая терапия и др.
- Некоторые химикаты.
- Некоторые лекарственные препараты, например, цитостатики, которые применяются для лечения злокачественных новообразований.
- Вирусы. В частности, доказана этиологическая роль вируса Эпштейна-Барр.
Лечение острого лейкоза
Назначается химиотерапия, направленная на уничтожение опухолевых клеток. Химиотерапия делится на 3 этапа: индукционная (вызывание ремиссии) (4–6 недель), закрепляющая (консолидирующая) (2–3 курса), поддерживающая (противорецидивная) терапия (до 5 лет). Одним из вариантов лечения является трансплантация костного мозга. При необходимости проводятся гемотрансфузии (переливание крови), антибактериальная терапия и лечение препаратами, стимулирующими кроветворение.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.
- Цитарабин (противоопухолевое средство, антиметаболит). Режим дозирования: в/в по 100 мг/м2/сут., две капельные инфузии по 3 ч каждая с интервалом 10 ч или непрерывно в течение 24 ч, курсовая доза 500-1000 мг. П/к по 20 мг/м2 2–3 раза в сутки. Курс — 4–7 дней (максимально до 10 дней).
- Даунорубицин (противоопухолевое средство). Режим дозирования: в/в, взрослым вводят в суточной дозе 30-60 мг/м2 (0,8-1,5 мг/кг) ежедневно в течение 3 дней или в дозе 20-40 мг/м2 (0,6-1 мг/кг) в течение 5 дней. Через 7-15 дней курс повторяют.
- Митоксантрон (противоопухолевое средство). Режим дозирования: в/в, при острых нелимфобластных лейкозах у взрослых для индукции ремиссии — в дозе 10-12 мг/м2 в/в медленно в течение 3–5 мин. или в/в капельно в течение 15-30 мин. ежедневно в течение 5 дней до суммарной дозы 50-60 мг/м2.
- Этопозид (противоопухолевое средство). Режим дозирования: в/в, путем 30-60-минутной инфузии. Дозы составляют 50-100 мг/м2/сут. в течение 5 дней, с повторением циклов каждые 3-4 нед. Также часто применяется режим введения этопозида через день — в 1, 3 и 5 дни.
- Амсакрин (противоопухолевое средство). Режим дозирования: в/в, при монотерапии препарат назначают в дозе 90 мг/м2 поверхности тела 1 раз в сутки в течение 5 дней (курсовая доза — 450 мг/м2 поверхности тела) при ежедневном контроле картины периферической крови.
- Винкристин (противоопухолевое средство). Режим дозирования: в/в, с интервалом между двумя инъекциями не менее 1 нед. Средняя доза для ребенка — 2 мг/м2, для взрослого — 1,4 мг/м2 (но не более 2 мг/м2 на одну инъекцию).
Острые лейкозы
– обширная гетерогенная группа опухолевых заболеваний системы крови, возникающие в результате мутаций (поломок) в генах, отвечающих за пролиферацию, дифференцировку и созревание нормальных кроветворных клеток. В результате этих событий в костном мозге происходит накопление лейкемических (бластных) клеток, что вызывает «вытеснение» нормального кроветворения опухолевым. В результате нарушается выработка форменных элементов крови и развивается цитопения. При развитии тромбоцитопении часто наблюдаются кровотечения; при снижении числа гранулоцитов – инфекции, эритроцитов — анемия.
Острые лейкозы распространены повсеместно, заболеваемость в разных странах составляет от 2 до 4 случаев на 100 000 населения в год. У взрослых 75-80% всех острых лейкозов составляют ОМЛ, 20-25% приходятся на долю ОЛЛ. Заболеваемость ОМЛ увеличивается с возрастом. Медиана возраста больных ОЛЛ — 14 лет, 60% заболевших моложе 14 лет, 24% — старше 45 лет. Мужчины и женщины заболевают с равной частотой.
Выделяют две большие принципиально различающиеся группы острых лейкозов: острые миелоидные лейкозы (ОМЛ) и острые лимфобластные лейкозы (ОЛЛ).
Диагноз острого лейкоза устанавливается только на основании обнаружения в периферической крови и костном мозге (иногда только в костном мозге) бластных (опухолевых) клеток. Пункцию костного мозга необходимо выполнять во всех случаях, независимо от процентного содержания бластных клеток в крови. При этом обязательными в диагностике является комплексное исследование костномозгового кроветворения: морфоцитохимическое, иммунофенотипическое, цитогенетическое. Такой комплекс диагностических исследований позволяет установить точный диагноз и определить вариант лейкоза. Это имеет принципиальное значение, поскольку различаются не только программы лечения ОЛЛ и ОМЛ, но и есть существенные, а иногда принципиальные отличия в терапии разных подвариантов как ОЛЛ, так и ОМЛ.
Острые лейкозы – являются потенциально излечимым заболеванием. Современная терапия позволяет получить полные ремиссии у 65-75% больных ОМЛ и у 75-90% больных ОЛЛ, но лишь в том случае, если лечение начато непосредственно после установления диагноза и проводится по программе, которая в настоящее время признается оптимальной для данного варианта лейкоза. При правильном лечении в среднем от 25 до 45% взрослых больных, у которых достигнуты полные ремиссии, остаются в этом статусе 5 лет и более, что для большинства случаев может расцениваться как выздоровление. Кроме того, острые лейкозы остаются основным показанием для выполнения аллогенной трансплантации гемопоэтических стволовых клеток, являющейся в большинстве случаев самым эффективным методом их лечения.
4.Диагностика и лечение
Чтобы узнать, есть ли у пациента лейкоз, врач задаст вопросы о симптомах заболевания и имеющихся проблемах со здоровьем. Кроме того, проводится и общий физический осмотр – врач посмотрит, не увеличены ли лимфатические узлы, печень или селезенка. В любом случае, при подозрении на лейкоз необходим анализ крови. Анализ крови при лейкемии покажет выской уровень лейкоцитов и низкий уровень других клеток крови.
Если результаты анализа крови отклоняются от нормы, врач может сделать биопсию костного мозга. Этот тест позволит изучить клетки костного мозга. Как правило, биопсия костного мозга дает возможность точно диагностировать лейкоз и его тип, и подобрать оптимальное лечение лейкоза.
Лечение лейкемии
То, как лечится лейкоз в каждом конкретном случае, зависит от многих факторов, в том числе, типа лейкемии, стадии заболевания, возраста и общего состояния здоровья пациента.
- В случае с острой лейкемией требуется быстрое лечение, чтобы остановить сильный рост лейкозных клеток. Во многих случаях правильное и своевременное лечение острого лейкоза позволяет добиться ремиссии заболевания. Обычно говорят именно о ремиссии лейкоза, а не о том, что болезнь вылечена, потому что есть риск, что лейкемия может вернуться снова. Но это совсем не обязательно;
- Хронический лейкоз редко удается вылечить полностью, но лечение поможет бороться с этой болезнью. Хронический лимфолейкоз, как правило, не лечат, пока не начнут появляться его симптомы. Но хронический миелолейкоз, вероятно, требует немедленной терапии.
Лечение лейкемии включает в себя несколько методов:
- Химиотерапия. Химиотерапи – основной метод лечения большинства типов лейкемии. В ходе этой процедуры погибают раковые клетки;
- Лучевая терапия. Радиационная терапия для лечения лейкоза использует высокие дозы рентгеновского излучения для уничтожения раковых клеток и уменьшения процесса роста лимфатических узлов и роста селезенки. Лучевая терапия также может проводиться перед трансплантацией стволовых клеток;
- Трансплантация стволовых клеток. Стволовые клетки могут восстановить процесс производства нормальных клеток крови и укрепить иммунную систему. Перед пересадкой стволовых клеток лучевая или химиотерапия разрушает клетки костного мозга и освобождает место для новых стволовых клеток. Или же эти процедуры позволяют ослабить иммунную систему так, что новые стволовые клетки смогут прижиться в организме;
- Биологическая терапия. Этот метод лечения использует специальные лекарства, которые повышают естественную защиту организма от рака.
Некоторые методы лечения лейкемии могут вызвать побочные эффекты. В любом случае, хороший врач поможет подобрать оптимальную схему лечения лейкоза и справиться с возможными побочными эффектами от лечения. Стоит отметить и то, что в настоящее время постоянно идет разработка новых методов лечения лейкемии. И в ходе клинических испытаний постоянно тестируются новые лекарственные средства и другие виды лечения лейкоза, которые дают шанс больным лейкемией победить болезнь!
Прогноз острого лимфобластного лейкоза
Прогностические факторы помогают более точно определить протокол лечения и его интенсивность. Благоприятными прогностическими факторами являются возраст от 3 до 7 лет, уровень лейкоцитов менее 25 000/мкл, FAB L1 вариант острого лимфобластного лейкоза, кариотип лейкозных клеток с наличием более 50 хромосом и t (12;21), отсутствие поражения центральной нервной системы на момент диагноза. Неблагоприятными факторами являются кариотип лейкозных клеток с нормальным числом хромосом, но аномальной морфологией (псевдодиплоидный) или наличие филадельфийской хромосомы t (9;22); пожилой возраст у взрослых и В-клеточный иммунофенотип с поверхностным или цитоплазматическим иммуноглобулином.
Несмотря на факторы риска, вероятность достижения первичной ремиссии у детей составляет более 95 % и у взрослых — 70-90 %. Приблизительно у 3/4 детей наблюдается значительная продолжительность без заболевания в течение 5 лет, и они считаются излеченными. В большинстве исследуемых протоколов для более интенсивного лечения выбирают больных с неблагоприятным прогнозом, поскольку увеличенный риск неэффективности лечения и впоследствии смерти перевешивает повышенный риск и токсичность терапии.
Как развивается острый лимфобластный лейкоз у детей
Клетки крови (лейкоциты, эритроциты, тромбоциты) производятся костным мозгом и затем разносятся по кровеносной системе.
Двумя основными типами лейкоцитов являются миелоидные и лимфоидные клетки. Они главным образом сконцентрированы в лимфатических узлах, селезенке, вилочковой железе (тимусе) и желудочно-кишечном тракте, обеспечивая наш иммунитет для борьбы с инфекциями.
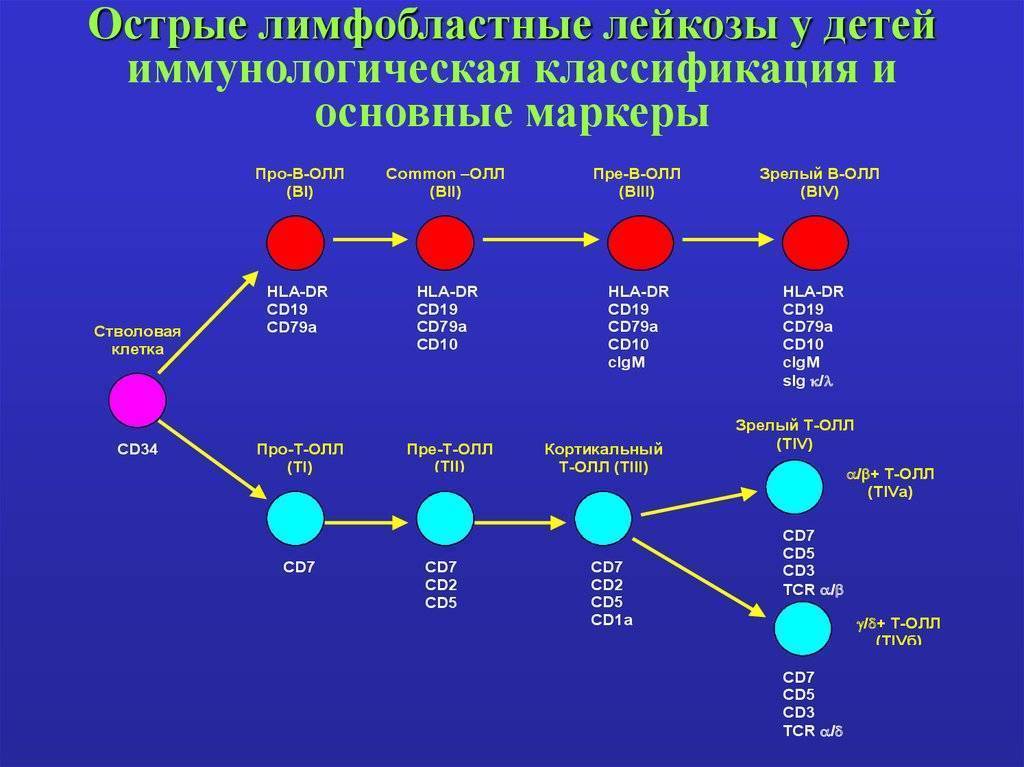
В норме костный мозг продуцирует три типа лимфоцитов, борющихся с инфекциями:
-
B-лимфоциты – они формируют антитела против болезнетворных микробов;
-
T-лимфоциты – уничтожают инфицированные вирусом или инородные клетки, раковые клетки. Они также помогают вырабатывать антитела;
-
Натуральные киллеры (NK-клетки) – их задача уничтожать вирусы и раковые клетки.
При ОЛЛ костный мозг начинает вырабатывать слишком много дефектных лимфоцитов. Эти клетки, называемые бластами, несут в себе аномальный генетический материал и не могут бороться с инфекциями так же эффективно, как обычные клетки. Кроме того, бласты довольно быстро делятся и вскоре начинают вытеснять здоровые лейкоциты, эритроциты и тромбоциты из крови и костного мозга. Как результат, развивается анемия, инфекции, или даже легкое кровотечение.
Аномальные лимфоциты, характерные для острого лимфобластного лейкоза, довольно быстро разносятся кровотоком и могут затронуть жизненно-важные органы: лимфоузлы, печень, селезенку, центральную нервную систему, половые органы (яички у мужчин или яичники у женщин).
Среди взрослых ОЛЛ – редкость, а вот дети совсем другое дело. Причем он может поразить ребенка любого возраста, включая и совсем малышей 2-4 лет.